메밀의 조직별 루틴분해효소 활성과 종실의 가열처리에 의한 효소 활성 억제
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Rutin is decomposed by rutin-degrading enzymes (RDE) during the processing of buckwheat groats, resulting in a decrease in rutin content and a further increase in the bitterness of processed products. Thus, the present study aimed to examine RDE activity in groats and various tissues of domestic buckwheat varieties and to develop a method to reduce the loss of rutin during the groat processing.
RDE activity and isozymes patterns were determined in Tartary and common buckwheat. RDE activity, measured by quercetin production rate, was 273 and 70 ㎍/g fresh weight/min in mature Tartary and common buckwheat groats, respectively. A total of six RDE isozymes were detected in mature groats of Tartary buckwheat on a non-denaturing gel. In Tartary buckwheat groats, RDE activity decreased by approximately 81 or 71% with roasting or steaming for 5 min respectively. As the roasting or steaming time increased to 30 min, RDE activity decreased by over 95%. These results indicated that RDE was inactivated in groats by roasting or steaming. When untreated Tartary buckwheat groats were kneaded with powder, RDE was activated and the quercetin production rate increased by 62%. However, when roasted groats were kneaded with powder, the quercetin production rate decreased by 93%, mainly due mainly to inactivation of RDE, as indicated by a decrease in band intensities of the six isozymes.
These results suggested that the loss of rutin, due to RDE activity during processing, may be reduced by 71 to 100% by roasting or steaming groats for 5 to 30 min, due in large part to the inactivation of RDE isozymes.
Keywords:
Groats, Inactivation, Isozymes, Roasting, Steaming서 언
메밀 (Fagopyrum esculentum Moench)은 마디풀과의 일년초로서 많은 기능성 성분을 포함하고 있어 식품영양학적으로도 유용한 작물이다.
메밀 내의 주요 플라보노이드로는 rutin, C-glycosyl-flavones (vitexin, isovitexin, orientin, isoorientin), quercetin 등이 있으며 페놀산으로는 chlorogenic acid 등 다수가 있다 (Watanabe and Ito, 2002). 특히 메밀에 풍부한 rutin은 quercetin에 rutinoside가 결합된 물질로서 혈관계 질환의 치료와 모세혈관 강화, 당뇨병 개선, 항산화 효과 등의 여러 가지 생리활성 기능을 가지고 있다고 보고되었다 (Choi et al., 1996; La Casa et al., 2000; Jiang et al., 2007). 또한 Hwang 등 (2006)은 발아 후 싹의 길이가 0 - 10㎜인 메밀 추출물의 항산화 활성이 합성항산화제의 활성보다 40 - 52% 높다고 보고하였다. Kim 과 Peck (2013)은 산화스트레스를 유발한 선충에 메밀 추출물을 처리할 경우 선충의 생존기간이 대조군에 비해 42.8% 증가하는 효과를 보여 메밀 추출물이 산화스트레스에 대한 저항성을 증가시킨다고 보고하였다.
메밀의 재배종은 쓴메밀 (F. tataricum)과 일반메밀 (F. esculentum)로 분류되는데, 쓴메밀은 일반메밀보다 영양성분 및 rutin의 함량이 높다는 것이 잘 알려져 있다. Han 등 (2014)은 메밀 추출물의 항산화력을 연구한 결과 쓴메밀과 일반메밀 추출물 모두 농도 의존적으로 DPPH 라디칼 소거능이 증가하였고, 추출물 농도 5㎕/㎖에서 DPPH 라디칼 소거능이 쓴메밀이 일반메밀보다 약 30% 높다고 보고하였다. 이러한 쓴메밀의 효능이 알려지면서 최근 서구화되어 가고 있는 식생활로 인해 나타나는 각종 성인병을 예방하고 치료하는데 쓴메밀을 이용하려는 관심이 높아지고 있다. 이에 따라 국내에서도 쓴메밀의 재배가 증가하고 있으며 메밀을 다양한 방법으로 가공하여 이용하고 있다 (Park et al., 2005; Cho et al., 2007; Morishita et al., 2007).
그러나 메밀을 가공하는 과정에서 메밀 내의 rutin이 루틴분해효소 (rutin-degrading enzymes, RDE)에 의해 분해되어 rutin 함량이 감소하게 되고 쓴 맛이 더욱 증가하게 된다. Lee 등 (2005)은 증자한 메밀가루에서 rutin의 함량이 114.9 ppm에서 12.6 ppm으로 감소하였고 증자 전에 검출 되지 않았던 quercetin 함량이 46 ppm으로 검출되었는데 이는 가공과정을 통해 rutin이 quercetin으로 변환된 것으로 보고하였다. Kim 등 (1991)은 메밀국수 조리과정에서 rutin이 분해되어 quercetin이 생성되는 것을 관찰하고 조리시간의 증가에 따라 rutin 함량이 감소한다고 보고하였다. Kreft 등 (2006)도 메밀가루를 이용하여 기능성 식품 제조시 국수에 있는 rutin 함량 (78㎎/㎏ D.W.)이 메밀가루에 들어있는 rutin 함량 (218㎎/㎏ D.W.) 보다 적다는 것을 발견하고 이러한 차이가 가공 중 효소분해 작용에 의한 것이라고 보고하였다. Yasuda 와 Nakagawa (1994)는 쓴메밀 종자의 rutin 함량이 일반메밀보다 100 배 정도 높으며, 쓴 메밀 종자에는 많은 RDE가 존재한다고 하였다.
RDE 활성은 HPLC 및 분광광도계를 이용하여 측정이 가능하나, 그 외의 간편한 측정 방법을 개발하는 연구가 이루어지고 있다 (Morishita et al., 1995; Chen and Gu, 2011). 생육 과정 및 다양한 처리에 의한 메밀 종실의 rutin 및 quercetin 함량 변화에 대한 연구는 많이 이루어졌으나 RDE에 관한 체계적인 연구는 미흡한 실정이다.
본 연구는 국내 메밀 품종의 종실을 비롯한 여러 조직 내의 rutin과 RDE 활성 수준을 조사하고 몇 가지 가공 처리를 통해 RDE 활성을 억제함으로써 가공 중 RDE에 의한 rutin의 손실을 감소시킬 수 있는 효과적인 방법을 개발하는데 필요한 기초자료를 얻고자 실시하였다. 또한 RDE 활성에 기여하는 동위효소의 종류와 동위효소별 활성을 검출하고, 각 동위효소의 활성이 RDE 활성에 기여하는 정도를 파악하고자 하였다.
재료 및 방법
1. 시험 재료
본 시험에서는 농촌진흥청에서 분양 받은 쓴메밀 (F. esculentum Moench) 품종 (대관 3-3호)과 일반메밀 품종 (대원 1호)을 사용하였다. 분양 받은 종자를 2015년도와 2016년도에 재배하여 수확한 메밀 조직 및 종실을 공시재료로 사용하였다.
2. 종실 가공 시료의 제조
메밀 종실의 찜 처리는 고압증기멸균기 (Hahnshin, Jeonju, Korea)를 이용하여 121℃에서 5, 10, 30 및 60 분간 처리하였으며, 볶음 처리는 80℃로 달궈진 스테인리스 용기에 5, 10, 30 및 60 분간 처리하였다. 처리가 완료된 종실은 상온에서 하루 동안 건조한 다음 미세분말 (50 mesh)로 분쇄하여 시험에 사용하였다.
메밀가루의 반죽은 볶지 않은 메밀 종실을 분쇄하여 얻은 분말에 물을 첨가 (메밀가루 :물 = 1 : 2) 하여 혼합하여 만들었으며, 제조된 반죽을 200 g씩 나누어 4℃에서 1 시간 숙성 처리하였다.
3. Rutin과 quercetin 함량 측정
메밀 종실 및 가공처리 시료 중의 rutin과 quercetin 함량은 건조시료 분말의 메탄올 추출액을 이용하여 측정하였다. 건조시료 분말 0.4 g을 methanol (10% phosphoric acid 포함) 8㎖에 균질화시킨 후 10,000 g에서 5 분간 원심분리 (Hanil, Model supra21K, Daejeon, Korea) 하여 얻은 상징액을 HPLC (Waters, Separation Module 2696, Photodiode Array Detector 996, Milford, MA, USA)를 이용하여 분석하였으며, HPLC 조건은 Table 1과 같다 (Table 1). 분리는 INNO column C18 (Young Jin Biochrom Co., Ltd., Seoul, Korea)을 사용하여 실시하였다. Rutin과 quercetin 정량에 사용한 분석용급 시약은 Merck (KGaA, Darmstadt, Germany)에서 구입하였다.
4. Rutin-degrading enzyme (RDE) 활성 측정
RDE 활성은 Chen 과 Gu (2011)의 방법을 응용하여 측정하였다. 메밀 시료 분말 0.4 g을 0.2 M acetate buffer (pH 4.0) 8㎖에 균질화 한 후 12,000 g에서 20 분간 원심분리하여 얻은 상징액을 활성 측정에 사용하였다.
효소 반응은 1.64 mM rutin 용액 (160㎕)과 메밀 효소 추출액 (40㎕, 단백질 양은 3.0 - 3.5㎍)을 혼합한 후 80℃에서 3 분간 진행한 다음 methanol (1,800㎕)을 첨가하여 반응을 종결시켰다. 반응이 종결된 혼합물을 10 분간 원심분리 (12,000 g)하여 얻은 상징액을 활성 측정에 이용하였다. RDE 활성은 기질로 제공한 rutin의 감소량 또는 반응액 중의 quercetin의 생성량을 시료 중량과 효소용액 중의 단백질 함량 단위로 표시하였다. Rutin과 quercetin은 HPLC로 분석하여 측정하였으며, HPLC 조건은 Table 2와 같다 (Table 2). RDE 활성의 측정 및 검출용 시약은 Merck (KGaA, Darmstadt, Germany)에서 구입하였다.
5. RDE 활성 검출
RDE 활성은 Li 등 (2013)의 방법을 응용하여 비변성 PAGE (polyacrylamide gel)과 전기영동장치 (Model Hoeffer SE600 and EPE301, Amersham Pharmacia Biotech, Piscataway, NJ, USA)를 이용하여 검출하였다. 효소 추출액은 시료 분말 0.8 g을 0.2 M acetate buffer (pH 4.0) 8㎖에 균질화한 뒤 12,000 g에서 20 분간 원심분리하여 얻은 상징액을 이용하였다.
효소 활성 염색을 위한 농축겔과 분리겔의 acrylamide농도는 각각 4%와 15% 이었으며, 각 시료의 효소 추출액 20㎕와 40% sucrose 20㎕, 0.005% bromophenol blue 20㎕를 함께 섞어 겔 (10 × 10 × 0.1㎝)의 홈에 20㎕씩 첨가하였다. 전기영동은 18 mA로 24 시간 실시하였으며, 전기영동이 종료된 겔을 0.2 M acetic acid buffer (4℃)에 40 분간 배양한 후에 30㎖ rutin solution (㎎/㎖)에 옮겨 50℃에서 5 분간 배양하고 증류수로 3 회 세척하였다. 세척이 완료된 겔에 365㎚ UV (Syngene, Frederick, MD, USA)를 조사하여 나타나는 활성 띠를 관찰하였다.
6. 통계분석
모든 실험은 3 반복으로 진행되었으며, 관측치의 통계처리는 Statistix program (Statistix 9.0, Tallahassee, FL, USA)을 이용하여 그룹 간의 통계적 유의성을 Duncan’s Multiple Range Test (DMRT)로 검정하였으며 유의성은 p < 0.05 수준에서 판단하였다.
결과 및 고찰
1. 메밀의 RDE isozyme 조성
비변성 PAGE 겔을 이용하여 분리된 단백질 중 RDE isozyme을 음성 염색하는 방법으로 검출한 결과, 쓴메밀 (Fagopyrum esculentum Moench) 완숙종실에서는 6 개의 isozymes이 검출되었다 (Fig. 1).
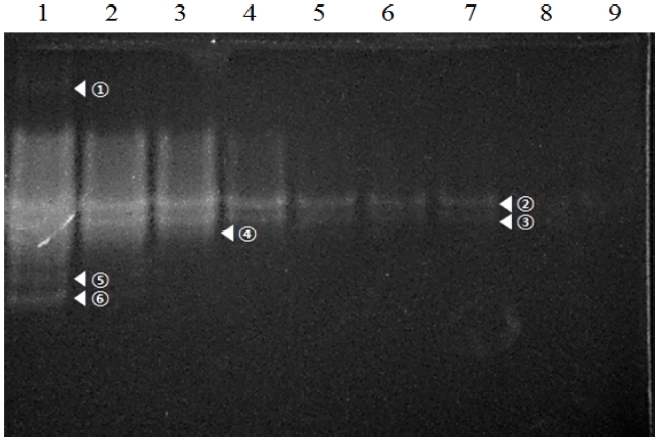
Isozymes of rutin-degrading enzymes (RDE) in Tartary buckwheat groats. Lanes 1 to 9 contain different amounts of total protein (3.44, 1.72, 0.86, 0.43, 0.215, 0.108, 0.054, 0.027 and 0.013 ㎍, respectively). Circled numbers denote each isozyme of RDE.
이들 isozyme들 중에서 2, 3, 4 번 isozyme은 1, 5, 6 번 isozyme에 비해 활성이 높았다. 음성 염색방법의 한계와 일부 isozyme의 낮은 활성으로 인해 제한된 isozyme 활성 띠의 분리능은 단백질 시료 양을 3.44 - 0.013㎍ 까지 순차적으로 조정함으로써 각 isozyme을 구분하여 검출할 수 있었다. 그러나 단백질의 농도가 낮아질 경우 1, 5, 6 번 isozyme은 활성 띠의 강도가 검출한계 이하로 저하되었다.
따라서 쓴메밀 종실에 존재하는 6 개의 RDE isozyme 중 2, 3 번 isozyme이 RDE 활성에 크게 기여하는 것으로 생각된다. Li 등 (2013)은 쓴메밀에서 5 개의 isozyme을 관찰하였다고 하였는데, 본 연구에서 관찰된 isozyme의 수와 다른 것은 메밀 품종에 따른 차이 때문이라 생각된다.
2. 메밀의 조직별 RDE 활성과 isozyme 발현 양상
Quercetin 생성량으로 측정한 식물체 조직별 RDE활성은 Fig. 2A와 같다. RDE 활성은 다른 조직에 비해 종실에서 매우 높았으며, 이러한 경향은 일반메밀과 쓴메밀에서 동일하게 나타났다. 쓴메밀 완숙종실의 RDE 활성 (273㎍/g·F.W./min)은 미숙종실보다 3 배 높았다. 일반메밀 완숙종실의 RDE활성 (70㎍/g·F.W./min)은 미숙종실보다 4 배 높았다. 단백질 양으로 측정한 식물체 조직별 RDE 활성은 Fig. 2B와 같다. 쓴메밀 완숙종실 (0.15㎍ protein/min)은 미숙종실보다 3 배 높았다. 일반메밀 완숙종실 (0.04㎍ protein/min)은 미숙종실보다 4 배 높았다.
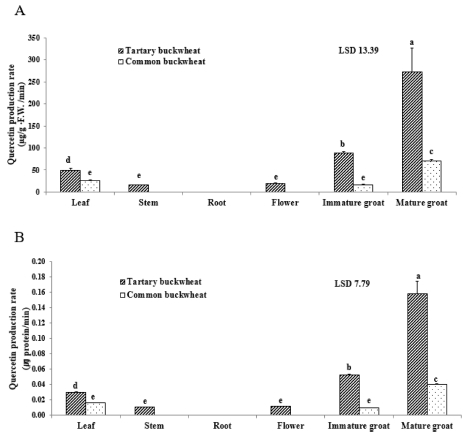
Rutin-degrading enzymes (RDE) activity in various buckwheat tissues expressed on the fresh tissue weight (A) and the amount of protein (B) bases. *Means within a column follwed by same letter are not significant based on the Duncan’s Multiple Range Test (DMRT) (p < 0.05).
두 품종에서 모두 잎은 줄기와 꽃에서보다 RDE 활성이 약간 높았으나, 미숙종실의 활성보다는 절반 이하로 낮았다. 뿌리에서는 RDE활성이 검출되지 않았다.
이상의 결과는 메밀의 종실은 다른 조직에 비해 RDE 활성이 매우 높아서 종실의 가공과정에서 RDE에 의해 rutin이 분해될 가능성이 매우 높을 것으로 생각된다.
메밀 조직별 RDE isozyme은 Fig. 3A 및 3B와 같다 (Fig. 3). 쓴메밀의 성숙종실에서는 6 개의 isozyme이 검출되었으며, 미숙종실에서는 2 번 isozyme의 활성 띠가 희미하게 관찰되었다 (Fig. 3A). 그러나 잎, 줄기, 꽃 및 뿌리 등에서는 isozyme이 관찰되지 않았다. 이러한 결과는 종실 이외의 조직에 존재하는 RDE 활성의 정도가 본 시험에서 사용한 RDE isozyme 검출 방법의 민감도에 의한 검출 한계보다 낮기 때문인 것으로 생각된다. 일반메밀의 성숙종실에서는 6 개의 isozyme이 검출되었으나, 기타의 조직에서는 검출되지 않았다 (Fig. 3B).
3. 볶음 및 찜 처리와 반죽을 한 메밀 종실의 rutin과 quercetin 함량
볶음 및 찜 처리한 메밀 종실의 rutin과 quercetin 함량은 Fig. 4와 같다 (Fig. 4). 쓴메밀 종실을 볶거나 찌는 경우 종실의 rutin 함량은 무처리 종실보다 각각 약 13% 증가하거나 33% 감소하였고, 무처리 종실가루를 반죽한 경우는 약 20% 감소하는 경향을 보였으나, 모든 처리구에서 통계적 유의차는 인정되지 않았다 (Fig. 4A).
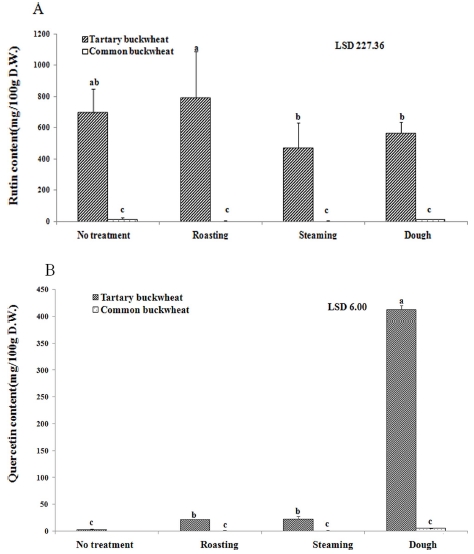
Rutin (A) and quercetin content (B) of heat-treated or kneaded buckwheat groats. Dough was prepared by mixing 1 volume of powder prepared from untreated buckwheat groats with 2 volume of distilled water. Dough was keep at 4℃ for 1 hour before analysis. *Means within a column follwed by same letter are not significant based on the Duncan's Multiple Range Test (DMRT) (p < 0.05).
Kim 등 (2012)은 쓴메밀 싹에 120℃로 원적외선처리를 할 경우 처리하지 않은 쓴메밀 싹에 비해 DPPH 라디컬 소거능이 89.5%로 높게 나타났지만 그 이상의 온도로 처리할 경우 소거능이 점점 낮아지며, 폴리페놀 및 플라보노이드 함량 측정 결과도 유사한 경향을 보였다고 보고하였다.
Lee 등 (2014)은 쓴메밀을 175℃에서 10 분간 볶은 처리를 할 경우 볶지 않은 쓴메밀에 비해 총 페놀성 화합물이 증가하였으나, 온도가 더 높아질수록 유의적으로 감소하였다고 보고하였다. Hong 등 (1998)도 치커리를 160℃에서 30 분 이하로 볶을 경우 페놀성 성분이 증가하는 경향을 보였으나, 볶음 온도와 시간이 길어질수록 오히려 감소한다고 하였다.
한편, quercetin 함량은 볶음, 찜 및 반죽처리 쓴메밀에서 대조구 (3㎎/100g D.W.)에 비해 각각 7 배, 7.5 배, 138 배 증가하였다. 일반메밀 종실에서도 볶음, 찜 및 반죽 처리에 의해 quercetin 함량이 각각 1.4㎎/100g D.W., 1.3㎎/100g D.W. 및 5.1㎎/100g D.W.으로 증가하였다 (Fig. 4B). 이러한 결과는 rutin의 분해에 의한 quercetin의 생성, 또는 quercetin의 새로운 합성 등에 의해 나타날 수 있을 것이다. Maeng 등 (1990)은 메밀 가공과정에서 rutin이 분해되어 quercetin 함량이 증가하였다고 보고한 바 있다. 따라서 본 연구에서 이용한 열처리 및 반죽처리에 의해 메밀 종실의 rutin이 quercetin으로 전환되었을 가능성을 배제할 수 없다. 특히 반죽처리에서는 활성화된 RDE에 의한 rutin의 분해와 이로 인한 quercetin의 생성이 가능하였을 것으로 생각된다.
이상의 결과는 가수처리나 반죽처리를 이용하는 메밀 종실의 가공 과정 중 RDE의 활성화 가능성을 의미하므로, 가수처리나 반죽 처리조건에 따른 RDE 활성 수준의 변화를 자세히 파악할 필요가 있다고 생각된다.
4. 볶음 및 찜 처리에 의한 RDE 활성 억제
열처리한 종실의 RDE 활성은 쓴메밀과 일반메밀에서 모두 현저히 감소하였다 (Fig. 5A). 종실을 볶거나 찌는 처리로 RDE활성이 크게 억제되어 quercetin 생성량이 감소하였으며, 볶거나 찐 쓴메밀 종실은 가열하지 않은 종실에 비하여 RDE활성이 각각 81% 와 85% 감소하였다. 일반 메밀의 경우도 볶거나 찐 종실은 가열하지 않은 종실에 비해 RDE 활성이 각각 71% 와 78% 감소하였다. 이러한 결과는 종실의 가열처리에 의해 RDE 활성이 크게 억제되었음을 나타낸다.
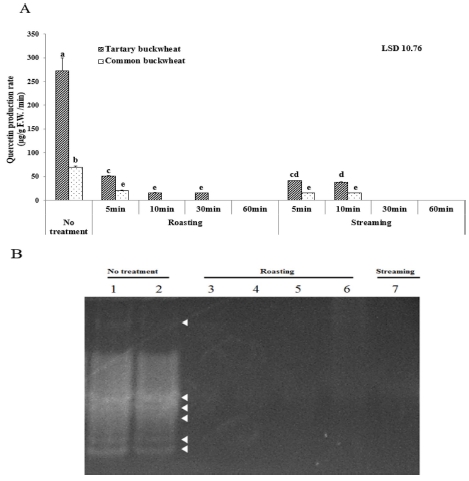
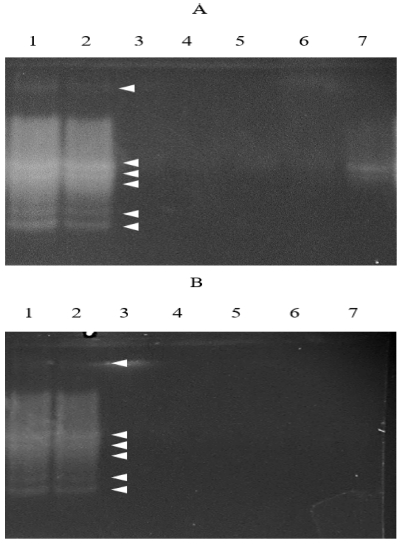
Inhibition of rutin-degrading enzymes (RDE) activity (A) and isozymes patterns of control, roasted and steamed mature groats (B). 1 and 2 indicate control and 1/2 dilution of control, respectively; 3, 4, 5 and 6 indicate 5, 10, 30 and 60 minutes of roasting, respectively. *Means within a column follwed by same letter are not significant based on the Duncan’s Multiple Range Test (DMRT) (p < 0.05).
RDE 활성은 열처리 시간이 증가할수록 감소 정도가 컸는데, 쓴메밀은 60 분 이상의 볶음처리로, 일반메밀은 10 분 이상의 볶음처리로 quercetin이 검출되지 않았으며, 30 분 이상 찔 경우 쓴메밀과 일반메밀 모두 quercetin이 검출되지 않았다.
열처리한 메밀 종실의 RDE isozyme은 Fig. 5B와 같다 (Fig. 5B). 열처리 한 쓴메밀 종실에서 RDE isozyme이 검출되지 않았는데, 이는 열처리에 의해 모든 isozyme의 활성이 검출한계 이하로 억제되었기 때문으로 생각된다. 열처리한 일반메밀의 종실에서도 모든 종류의 isozyme이 검출되지 않았다. 즉, 두 품종에서 모두 열처리에 대해 저항성을 보이는 isozyme은 존재하지 않았다.
이상의 결과로 메밀 종실이나 분말상태의 원재료를 이용하는 경우에는 볶음 및 찜 처리를 함으로써 가공 중 RDE에 의한 rutin 손실을 최소화할 수 있을 것으로 기대된다.
Acknowledgments
본 연구는 농촌진흥청 농업유전자원관리기관사업의 지원에 의해 이루어진 것으로 이에 감사드립니다.
REFERENCE
-
Chen, P, and Gu, J., (2011), A rapid measurement of rutin-degrading enzyme activity in extract of tartary buckwheat seeds, Food and Bioproducts Processing, 89, p81-85.
[https://doi.org/10.1016/j.fbp.2010.02.002]

- Cho, EJ, Kim, WJ, and Yang, MO., (2007), A study on quality properties of steamed cake added with common and tartary buckwheat flour, Journal of the East Asian Society of Dietary Life, 17, p219-226.
- Choi, BH, Kim, SL, and Kim, SK., (1996), Rutin and functional ingredients of buckwheat and their variations, Korean Journal of Crop Science, 41, p69-93.
-
Han, NK, Park, CM, Kwon, JC, Joung, MS, and Choi, JW., (2014), Whitening effect of Fagopyrum tataricum extract, Journal of the Society of Cosmetic Scientists of Korea, 40, p179-186.
[https://doi.org/10.15230/scsk.2014.40.2.179]

- Hong, MJ, Lee, GD, Kim, HK, and Kwon, JH., (1998), Changes in functional and sensory properties of chicory roots induced by roasting processes, Korean Journal of Food Science and Technology, 30, p413-418.
- Hwang, EJ, Lee, SY, Kwon, SJ, Park, MH, and Boo, HO., (2006), Antioxidative, antimicrobial and cytotoxic activities of Fagopyrum esculentum Möench extract in germinated seeds, Korean Journal of Medicinal Crop Science, 14, p1-7.
-
Jiang, P, Burczynski, F, Campbell, C, Pierce, G, Austria, JA, and Briggs, CJ., (2007), Rutin and flavonoid contents in three buckwheat species Fagopyrum esculentum, F. tataricum, and F. homotropicum and their protective effects against lipid peroxidation, Food Research International, 40, p356-364.
[https://doi.org/10.1016/j.foodres.2006.10.009]

- Kim, BN, Park, HK, Kwon, TB, and Maeng, YS., (1991), Analysis of rutin contents in buckwheat noodles, Korean Journal of Food and Cookery Science, 7, p61-66.
-
Kim, CK, and Perk, SK., (2013), Buckwheat extract increases resistance to oxidative stress and lifespan in Caenorhabditis elegans, Korean Journal of Medicinal Crop Science, 21, p1-6.
[https://doi.org/10.7783/kjmcs.2013.21.1.1]

- Kim, WW, Shin, DB, Jin, CW, and Cho, DH., (2012), Quantitative analysis of quercetin in tatary buckwheat(Fagopyrum tataricum Gaertn) by far infrared ray, 7(supplement 1), p251-252.
-
Kreft, I, Fabjan, N, and Yasumoto, K., (2006), Rutin content in buckwheat(Fagopyrum esculentum Moench) food materials and products, Food Chemistry, 98, p508-512.
[https://doi.org/10.1016/j.foodchem.2005.05.081]

-
La Casa, C, Villegas, I, de la Lastra, CA, Motilva, V, and Martín Calero, MJ., (2000), Evidence for protective and antioxidant properties of rutin, a natural flavone, against ethanol induced gastric lesions, Journal of Ethnopharmacology, 71, p45-53.
[https://doi.org/10.1016/s0378-8741(99)00174-9]

-
Lee, MH, Cho, JH, Kim, JC, and Kim, BK., (2014), Effect of roasting conditions on the antioxidant activities of tartary buckwheat, Korean Journal of Food Science and Technology, 46, p390-393.
[https://doi.org/10.9721/kjfst.2014.46.3.390]

- Lee, SJ, Kim, SJ, Han, MS, and Chang, KS., (2005), Changes of rutin and quercetin in commercial Gochujang prepared with buckwheat flour during fermentation, Journal of Korean Society of Food Science and Nutriton, 34, p509-512.
-
Li, Y, Deng, D, Zhang, X, Zhang, H, Wang, C, and Chen, P., (2013), Direct detection of rutin-degrading isozymes with polyacrylamide gel electrophoresis, Analytical Biochemistry, 443, p240-242.
[https://doi.org/10.1016/j.ab.2013.09.010]

- Maeng, YS, Park, HK, and Kwon, TB., (1990), Analysis of rutin contents in buckwheat and buckwheat foods, Korean Journal of Food Science and Technology, 22, p732-737.
- Morishita, T, Hajika, M, Sakai, S, and Tetsuka, T., (1995), Development of simple spectrophotometric assay for the rutin-degrading enzyme in buckwheat, Current Advances in Buckwheat Research, 6, p833-837.
-
Morishita, T, Yamaguchi, H, and Degi, K., (2007), The contribution of polyphenols to antioxidative activity in common buckwheat and tartary buckwheat grain, Plant Production Science, 10, p99-104.
[https://doi.org/10.1626/pps.10.99]

- Park, BJ, Kwon, SM, Park, JI, Chang, KJ, and Park, CH., (2005), Phenolic compounds in common and tartary buckwheat, Korean Journal of Crop Science, 50, p175-180.
-
Watanabe, M, and Ito, M., (2002), Changes in antioxidative activity and flavonoid composition of the extracts from aerial parts of buckwheat during growth period, Journal of the Japanese Society for Food Science and Technology, 49, p119-125.
[https://doi.org/10.3136/nskkk.49.119]

-
Yasuda, T, and Nakagawa, H., (1994), Purification and characterization of the rutin-degrading enzymes in tartary buckwheat seeds, Phytochemistry, 37, p133-136.
[https://doi.org/10.1016/0031-9422(94)85012-7]