β-glucosidase 활성 균주 발효에 의한 황기 Isoflavonoid 성분변화 및 생리활성
 ; Eun Soo Seong3
; Eun Soo Seong3 ; Jung Dae Lim4
; Jung Dae Lim4 ; Seon Kang Choi5
; Seon Kang Choi5 ; Chang Yeon Yu6
; Chang Yeon Yu6 ; Jae Geun Lee7, †
; Jae Geun Lee7, †
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
In this study, the radix of Astragalus membranaceus Bunge extract fermented by Saccharomyces cerevisiae, Weissella cibaria, and Pediococcus pentosaceus to increase the levels of isoflavonoid aglycone contents.
In order to change the in isoflavonoids, we fermented the radix of A. membranaceus extracts with microorganisms that have β-glucosidase activity. Besed on the β-glucosidase activity, we selected three strains, Weissella cibaria, Pediococcus pentosaceus, and Saccharomyces cerevisiae. HPLC analysis revealed that the levels of isoflavonoid aglycones were increased in all fermentation cases, and the extracts fermented by S. cerevisiae showed the highest levels of isoflavonoid aglycones. We evaluated the antioxidant activity, anti-wrinkle effects and whitening effects of the S. cerevisiae-fermented extracts using the DPPH assay, tyrosinase inhibition activity assay, and collagenase inhibition activity assay. We confirmed higher activity in S. cerevisiae-fermented extracts than in control, with the half maximal inhibitory concentration (IC50) value of 565.1 ± 59.1 ㎍/㎖ in DPPH radical scavenging activity, tyrosinase inhibition rate of 78.4 ± 0.9%, and collagenase inhibition rate of 83.8 ± 1.1%.
We selected three stains of microorganisms showing high β-glucosidase activity, W. cibaria, P. pentosaceus and S. cerevisiae. Isoflavonoid glycones in the radix of A. membranaceus were converted to isoflavonoid aglycones by fermentation. In addition, the fermented radix of A. membranaceus exhibited antioxidant activity, anti-wrinkle effect, whitening effect and radical scavenging activity.
Keywords:
Astragalus membranaceus Bunge, Anti-wrinkle, Calycosin, Fermentation, Formononetin, Pediococcus pentosaceus, Saccharomyces cerevisiae, Weissella cibaria, Whitening Effects서 언
황기 (Astragali Radix; Astragalus membranaceus Bunge)는 콩과에 속하는 다년생 초본식물인 단너삼의 뿌리로, 한국, 중국, 일본과 같은 극동아시아 지역에서 재배되고 있으며 (Im et al., 2010), 항종양 (Cho and Leung, 2007a), 항염 (Cho and Leung, 2007b), 간보호 (Park et al., 2013), 면역증강 (Lee et al., 2018b; Yang et al., 2016), 항산화, 미백, 항노화 (Goh et al., 2009; Kim et al., 2007) 등의 효능이 보고되었다.
황기의 주요성분은 isoflavonoid, triterpenoid, polysaccharide계열이며, isoflavonoid는 콩과 식물의 특이적인 phenylpropanoid pathway에 의한 것으로 알려져 있다. phenylalanine ammonia-lyase (PAL) 효소에 의해 phenylalanine이 cinnamate로 변환되고, naringenin과 liguiritigenin이라는 중간대사물질을 거쳐 daidzein, formononetin, calycosin, puerarin으로 변환되어, 최종적으로 배당체 glucoside가 결합된 형태로 생합성 된다 (Pan et al., 2007; Wang, 2011; Wang, 2016).
배당체, 비배당체 isoflavonoid 생리활성을 검정한 Kong 등 (2018)의 연구결과에 따르면, isoflavonoid는 에스트로겐의 유사역할을 하며, 비배당체 isoflavonoid에서 골다공증 효과가 증가되는 것을 확인하였고, 배당체 형태보다 체내에서 빠르게 흡수 되는 것으로 보고되었다 (Hirotani et al., 1994; Izumi et al., 2000; Lin et al., 2000; Shim et al., 2014). β-glucosidase는 배당체 isoflavonoid를 분해하여 무배당체 형태인 비배당체 isoflavonoid로 변환시키는 것으로 알려져 있으며 (Lee et al., 2018a), Kuo 등 (2006)은 β-glucosidase를 함유하는 균주 (Bacillus subtilis)로 검정콩을 12시간 발효하였을 때, 가장 높은 β-glucosidase 활성을 나타낸 동시에 isoflavone 중 배당체가 감소하고, 비배당체 isoflavonoid가 증가되었다고 보고하였다.
본 연구에서는 전통식품 유래 미생물 중 β-glucosidase 활성을 나타내는 균주를 선별한 후, 황기추출물을 액상발효하여, isoflavonoid 중 배당체 calycosin 7-O-glucoside, formononetin 7-O-glucoside와 비배당체 calycosin, formononetin 함량변화 비교분석과 생리활성평가 (항산화, 미백, 주름개선)를 실시하였다.
재료 및 방법
1. 재료
실험에 사용한 황기는 국내에서 재배된 4년근 (1bangherb, Geumsan, Korea)을 구입하였고, 선별된 미생물은 국내·외 전통식품 및 발효식품 유래 균주로 분리·동정된 것을 농촌진흥청 국립농업과학원 농업유전자원센터에서 분양받았으며, Saccharomyces cerevisiae (HLJG0703, KACC 83014BP)는 빵에서, Pediococcus pentosaceus (HLJG0702, KACC 81017BP)는 김치에서 분리된 균주를 분리·동정하여 사용하였다.
Isoflavonoid 표준품 calycosin 7-O-glucoside, formononetin 7-O-glucoside, calycosin, formononetin은 Sigma-aldrich (St. Louis, MO, USA)에서 구입하여 사용하였다 (Table 1).
2. β-glucosidase 활성
Esculin은 β-glucosidase에 의해 분해되어 esculetin을 생성하며, 배지성분의 ferric ammonium citrate와 결합하여 black complex를 형성한다 (Edberg et al., 1985). 정성시험은 Lindell과 Quinn (1975)의 esculin agar method를 변형하여 수행하였다.
48 시간동안 MRS broth 또는 YM broth에서 pre-incubation 시킨 균주 O.D. (optical density) 값을 UV-Vis spectrophotometer (Molecular Devices, San Jose, CA, USA) 600 ㎚에서 1.5로 보정한 후, 200 ㎕를 취하여 esculin agar에 도말하였다. 이후, 48 시간 동안 생성되는 균주 colony 주위의 black zone 유무를 통하여 β-glucosidase 활성을 균주별로 상대 비교하였다.
정량시험은 Ra 등 (2004) β-glucosidase activity assay 방법을 변형하여 수행하였다. 48 시간동안 MRS broth 또는 YM broth에서 pre-incubation시킨 균주의 O.D.값을 UV-vis spectrophotometer (Molecular Devices, San Jose, CA, USA) 600 ㎚에서 1.5로 보정한 후, 원심분리 (12,000 × g, 5 min, 4℃)하여 침전물을 50 mM sodium phosphate 완충용액 (pH 7.0)으로 2 회 세척하여 현탁하였다. 이후, sonication (5 min)하여 세포를 파쇄시키고, 세포 파쇄액을 원심분리 (12,000 × g, 5 min, 4℃)하여 상등액 (효소액)을 분리하였다.
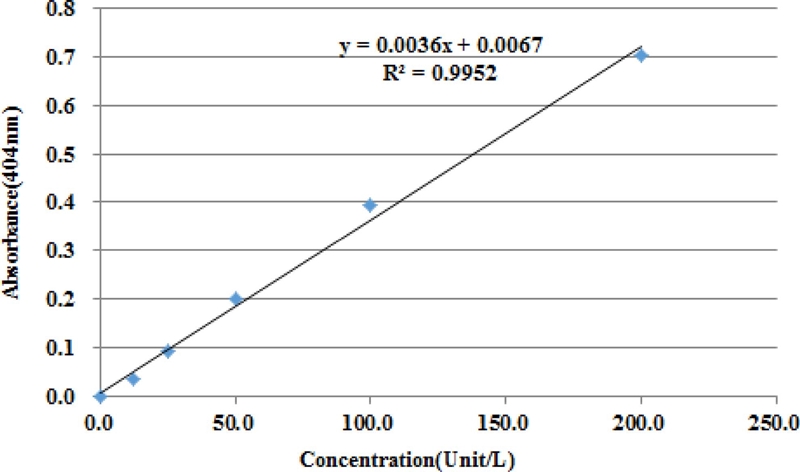
활성측정은 효소액과 50 mM sodium phosphate (pH 7.0)에 1 mM pNPG 용액을 각각 100 ㎕를 혼합하여 반응 (37℃, 20 min) 시킨 후, 0.4 M Na2CO3 용액 2 ㎖을 첨가하여 반응을 정지시킨 후, UV-Vis spectrophotometer (Molecular Devices, San Jose, CA, USA) 404 ㎚에서 측정하였으며, 표준품으로 산출된 검량선 방정식에 대입하여 계산하였다 (Fig. 1).
3. 황기추출물 액상 발효
액상발효를 수행하기 위해 황기를 50% EtOH로 상온에서 2 일 간 진탕추출하여, 추출물을 농축·동결 건조한 후, 정제수를 첨가하여 발효균이 성장할 수 있는 농도인 1 brix, 3 brix로 현탁액을 제조하였다. 이후, 48 시간 동안 MRS broth 또는 YM broth에서 pre-incubation 시킨 균주의 O.D.값을 600 ㎚에서 1.5로 보정한 균주 5% (v/w) 접종하여 1 일 - 3 일 간 조건적 혐기발효 (25℃, facultative anaerobe)를 실시하였다. 불활성화를 시키기 위해 수욕상에서 80℃, 1 시간 동안 처리하여 반응을 종료시켰으며, 동결건조하여 시료로 사용하였다.
4. Isoflavonoid 함량분석
시료 2 g을 정밀히 달아 50 ㎖ 부피 플라스크에 취하고, 완전하게 용해시키며 50% EtOH을 표선까지 채운 후, syringe filter (0.45 ㎛) 및 희석하였으며, 표준품은 3.124 ㎍/㎖, 6.250 ㎍/㎖, 12.500 ㎍/㎖ 농도로 희석하여 사용하였다. Isoflavonoid 함량분석은 high performance liquid chromatography (HPLC) Ulti-Mate 3000 (Thermo Scientific Inc., Waltham, MA, USA) 기기로 수행하였고, column은 Luna C18 (Phenomenex Inc., Torrance, CA, USA), 이동상은 0.1% acetic acid가 첨가된 acetonitrile과 water를 사용하였다.
시료 주입량 10 ㎕, 유속 0.8 ㎖/min, 온도 30℃, UV detector로 260 ㎚에서 table 2와 같은 이동상 조건으로 측정하였다. 시료의 정량값 측정은 피크면적을 검량선 방정식에 대입한 후 아래의 계산식에 의해 산출하였다. 검량선은 x축에 농도를 y축에 피크면적을 적용하여 최소자승법으로 계산하였다 (Table 2).
C: 시험용액 중 개별 isoflavonoid농도 (㎍/㎖)
a: 시험용액의 전량 (㎖)S: 시료 채취량 (g)
b: 희석배수1/1,000: 단위 환산 계수
5. 항산화 활성
DPPH radical scavenging은 Blois (1958)에 의해 실시된 방법을 변형하여 측정하였다. 시료 100 ㎕에 0.2 mM DPPH 100 ㎕를 혼합하여 상온, 암조건에서 30 분간 반응시킨 후, 517 ㎚에서 흡광도를 측정하였다. 시료의 활성은 IC50 (half maximal inhibitory concentration)으로 나타내었고, 양성대조군은 ascorbic acid를 사용하였다.
ABTS radical cation decolorization은 Re 등 (1999)에 의해 실시된 ABTS+ 라디칼 양이온 측정법을 변형하여 수행하였다. 7 mM 2,2'-Azino-bis (3-ethylbenzothiazoline-6-sulfonic acid)와 2.45 mM potassium persulfate를 1 : 1 비율로 혼합하여 상온, 암조건에서 24 시간동안 방치하여 라디칼을 형성시키고, UV-Vis spectrophotometer (Molecular Devices, San Jose, CA, USA)를 이용하여 732 ㎚에서 흡광도 값이 0.70 (± 0.02)이 되게 phosphate-buffered saline (PBS, pH 7.4)로 희석한 후, 희석용액 990 ㎕에 시료 10 ㎕를 가하여 10 분 간 반응시킨 후 흡광도를 측정하였다. 시료의 활성은 IC50으로 나타내었고, 양성대조군은 ascorbic acid를 사용하였다.
6. 미백, 주름개선 효과
Tyrosinase inhibition 활성은 Yagi 등 (1986)의 방법에 따라 수행하였다. 175 mM sodium phosphate buffer (pH 6.8) 0.5 ㎖에 10 mM L-DOPA 0.2 ㎖ 및 시험물질 0.1 ㎖ 혼합액에 tyrosinase (20 unit/㎖) 0.2 ㎖을 첨가하여 반응 (37℃, 30 min) 시킨 후, 흡광도 (475 ㎚)를 측정하였다. Tyrosinase 저해활성은 시료 첨가군와 무첨가군의 흡광도 감소율로 나타내었다.
Collagenase inhibition 활성은 Wünsch와 Heidrich (1963)의 방법에 따라 수행하였다. Tris-HCl buffer (100 mM, pH 7.5)에 4 mM의 CaCl2를 녹여 buffer를 제조하여 사용하였고, buffer에 collagenase와 기질액(4-phenylazobenzyloxycarbonyl-Pro-Leu-Gly-Pro-D-Arg)을 각각 0.2 ㎎/㎖, 0.3 ㎎/㎖ 농도로 제조하여 반응하였다. 시험물질을 250 - 2,500 ㎍/㎖ 농도로 조제한 후, 시험물질 50 ㎕, collagenase 75 ㎕, 기질액을 125 ㎕을 취하여 반응 (20℃, 20 min)시킨 후, ethyl acetate로 분획하여 상등액만 취하여 흡광도 (340 ㎚)를 측정하였다. Collagenase 저해활성은 시료 첨가군와 무첨가군의 흡광도 감소율로 나타내었다.
7. 통계처리
모든 실험은 3 회 반복으로 수행한 후, 평균과 표준편차로 나타내었고, 통계처리는 Prism 8 software (Graphpad software Inc., San diego, CA, USA)를 이용하여 이원분산분석 (Two-way ANOVA)으로 p < 0.05 수준에서 Dunnett’s Multiple Comparison Test에 의하여 시험물질 간 유의성을 검증하였다.
결과 및 고찰
1. β-glucosidase 활성
Esculin agar를 통한 정성분석 결과, P. pentosaceus 91.7 ± 2.9%, W. cibaria 90.7 ± 1.2%, S. cerevisiae 83.3 ± 5.8%, B. licheniformis 79.3 ± 6.7%, L. mesenteroides 79.0 ± 3.6% 순으로 black zone 형성율을 나타냈고, β-glucosidase activity를 통한 정량분석은 W. cibaria 39.3 ± 8.7 unit/ℓ, S. cerevisiae 30.5 ± 0.5 unit/ℓ, P. pentosaceus 27.5 ± 0.2 unit/ℓ, B. licheniformis 17.4 ± 1.7 unit/ℓ, L. bulgaricus 17.4 ± 2.3 unit/ℓ 순으로 정량값을 나타내었다. 20 종의 미생물 중 정성분석과 정량시험에 활성을 나타내는 W. cibaria, P. pentosaceus, S. cerevisiae를 발효시험 균주로 선발하였다 (Table 3).
2. Isoflavonoid 함량분석
Isoflvonoid 정량분석은 황기추출물을 대조군으로 W. cibaria, P. pentosaceus, S. cerevisiae로 발효한 발효추출물 (1 brix - 3 brix, 1 일 - 3 일)을 처리군으로 나누어 실시하였고, 발효공정에 따른 황기의 calycosin 7-O-glucoside, formononetin 7-O-glucoside, calycosin, formononetin 함량은 Table 4에 나타내었다. 대조군 대비 모든 처리군에서 배당체 calycosin 7-O-glucoside, formononetin 7-O-glucoside가 감소하고, 비배당체 calycosin, formononetin이 증가하였다. 이중 황기추출물을 1 birx로 희석하여, S. cerevisiae로 3 일간 발효시킨 처리군에서 calycosin 1.102 ± 0.008 ㎎/g, formononetin 1.482 ± 0.001 ㎎/g으로 최대 함량이 검출되었다.

The contents of isoflavonoids of A. membranaceus Bunge extracts fermented by the traditional foods strains.
Ibe 등 (2001)은 건조된 볏짚에서 분리한 50 여종의 미생물 중 β-glucosidase 활성이 높은 Bacillus subtilis (natto) 분리·동정한 후, 대두추출물을 발효하였을 때, 추출물에 함유된 isoflavonoid 배당체 daidzein과 genistin 함량이 감소하면서 비배당체 daidzein과 genistein이 증진되는 발효양상을 검증하였고, Kuo 등 (2006)은 검은콩 두유를 Bacillus subtilis로 24 시간 발효하였을 때, daidzein과 genistin이 탈탕화에 의해 비배당체 daidzein과 genistein으로 변환되었다고 보고하였다.
Im 등 (2010)은 황기를 에탄올로 추출한 후, 탄수화물 분해효소 viscozyme L, 셀룰로오스 분해효소 celluclast, 팩틴 분해효소 pectinex로 반응시킨 후, calycosin과 formononetin의 함량을 비교하였을 때, viscozyme L을 처리하였을 때, calycosin과 formononetin 함량이 4 - 5 배 증가하였고, viscozyme L에 함유된 arabanase, cellulase, β-glucanase가 deglycosylation에 관여하는 것을 확인하였다.
Hsu 등 (2018) 연구에 따르면 isoflavone은 3-phenylchrome 골격을 갖고 있는 화합물로 치환기에 부착된 성분에 따라 calycosin 7-O-glucoside, ononin, daidzein, genistin 등으로 구분되며, 미생물에 의해 생성되는 대사물질에 따라 deglycosylation, glycosylation, phosphrylation, succinylation 과정을 거쳐 화합물이 변환되는 것을 확인하였다.
본 실험에서는 deglycosylation 효소 중 glucoside 분해효소를 갖는 β-glucosidase 활성균주로 발효하였을 때, 황기 isoflavonoid 배당체 calycosin 7-O-glucoside와 formononetin 7-O-glucoside가 감소하고, calycosin과 formononetin이 증가하여, 미생물의 β-glucosidase 효소활성이 배당체 isoflavonoid 분해하는데 영향을 미치는 것을 확인하였지만, 배당체와 비배당체의 변환율을 비교하였을 때, calycosin 7-O-glucoside와 formononetin 7-O-glucoside 이외의 대사물질이 calycosin, formononetin 증가량의 상호적인 역할을 하는 것으로 사료되며, 추가적인 연구가 필요할 것으로 확인되었다.
3. 항산화 활성
생리활성평가는 황기추출물을 대조군으로 S. cerevisiae로 발효한 발효추출물 (1 brix - 3 brix, 1 일 - 3 일)을 처리군으로 나누어 실시하였고, 발효공정에 따른 황기의 항산화 활성을 DPPH 및 ABTS로 수행한 결과는 Table 5에 나타내었다. DPPH IC50 value은 대조군 1587.1 ± 30.9 ㎍/㎖, 처리군4 1327.1 ± 45.1 ㎍/㎖, 처리군1 1215.9 ± 36.4 ㎍/㎖, 처리군5 1056.1 ± 71.4 ㎍/㎖, 처리군2 945.1 ± 35.6 ㎍/㎖, 처리군6 671.5 ± 51.6 ㎍/㎖, 처리군3 565.1 ± 59.1 ㎍/㎖순으로 증가하였고, ABTS IC50 value은 대조군 1728.2 ± 32.4 ㎍/㎖, 처리군4 1597.1 ± 42.6 ㎍/㎖, 처리군1 1454.6 ± 129.0 ㎍/㎖, 처리군5 1114.6 ± 42.7 ㎍/㎖, 처리군2 942.1 ± 59.4 ㎍/㎖, 처리군6 791.1 ± 28.3 ㎍/㎖, 처리군3 678.2 ± 17.8 ㎍/㎖순으로 활성이 증가하였다.
Wang 등 (2014)은 황기추출물에서 formononetin, calycosin을 Sephadex LH-20 chromatography로 분리한 후, ABTS를 확인하였을 때, 7.468 ㎎/㎖, 0.159 ㎎/㎖의 IC50을 라디칼 소거능을 검증하였고, Park 등 (2019)은 황기의 볶음조건 (200℃, 30 분 간 1 회 - 3 회)에 따른 DPPH, ABTS 활성을 비교하였을 때, 대조구 대비 2 회 볶음에서 formononetin은 286.65 ± 2.51 ㎍/g에서 726.80 ± 3.45 ㎍/g, calycosin은 253.13 ± 1.23 ㎍/g에서 778.58 ± 2.72 ㎍/g으로 함량이 증가함에 따라 DPPH는 3125.1 ± 82.7 ㎍/㎖에서 564.6 ± 20.9 ㎍/㎖, ABTS는 1450.2 ± 114.3 ㎍/㎖에서 108.2 ± 3.1 ㎍/㎖으로 증가한다고 보고하였다.
4. 미백, 주름개선 효과
Tyrosinase inhibition rate를 측정한 결과, 처리군4 42.9 ± 8.6%, 대조군 50.1 ± 1.1%, 처리군5 54.2 ± 2.9%, 처리군1 56.0 ± 3.4%, 처리군2 56.9 ± 1.8%, 처리군6 74.9 ± 0.3%, 처리군3 78.4 ± 0.9%순으로 활성이 증가하였고, 처리군3에서 최대 저해율을 나타내었다 (Table 6).

Collagenase inhibitory rate and tyrosinase inhibition of A. membranaceus B. root extract fermeted by S. cerevisiae.
Kim 등 (2009)은 황기 calycosin의 mushroom tyroinase 억제효과를 실시한 결과, 38.4 ± 0.9 μM (100 ㎍)의 저해효과를 검정하였고, Wagle 등 (2019)은 칡에 함유된 isoflavonoid의 L-DOPA inhibition을 측정하였을 때, formononetin 0.31 ± 0.62%, calycosin 70.17 ± 1.08%, kojic acid 76.78 ± 3.34%의 L-DOPA 억제율을 확인하여, calycosin이 formononetin 대비 미백활성에 효과를 나타내는 것으로 보고하였다.
Collagenase inhibition rate를 측정한 결과, 처리군5 77.8 ± 0.9%, 대조군 78.1 ± 0.8%, 처리군2 79.9 ± 0.8%, 처리군1 80.1 ± 0.5%, 처리군4 80.8 ± 0.2%, 처리군6 82.0 ± 1.0%, 처리군3 83.8 ± 1.1%순으로 활성이 증가하였고, 처리군3에서 최대 저해율을 나타내었다 (Table 6).
Hsu 등 (2009)은 Bacillus subtilis로 황기를 발효하였을 때, calycosin과 formononetin 함량이 증가함에 따라, 인간진피 섬유아세포의 procollagen (type I, III) 합성량이 증가한다고 보고하였다.
본 시험에서는 대조군 대비 calycosin과 formononetin 함량이 증가된 처리군3에서 tyrosinase inhibition, collagenase inhibition 활성이 증가되는 것을 확인하였으며, 발효에 의해 증가된 비배당체 isoflavonoid와 미백과 주름개선 활성의 연관성이 있을 것으로 사료된다.
References
-
Blois MS. (1958). Antioxidant determinations by the use of a stable free radical. Nature. 181:1199-1200.
[https://doi.org/10.1038/1811199a0]

-
Cho WCS and Leung KN. (2007a). In vitro and in vivo anti-tumor effects of Astragalus membranaceus. Cancer Letters. 252: 43-54.
[https://doi.org/10.1016/j.canlet.2006.12.001]

-
Cho WCS and Leung KN. (2007b). In vitro and in vivo immunomodulating and immunorestorative effects of Astragalus membranaceus. Journal of Ethnopharmacology. 113:132-141.
[https://doi.org/10.1016/j.jep.2007.05.020]

-
Edberg SC, Trepeta RW, Kontnick CM and Torres AR. (1985). Measurement of active constitutive β-D-glucosidase(esculinase) in the presence of sodium desoxycholate. Journal of Clinical Microbiology. 21:363-365.
[https://doi.org/10.1128/JCM.21.3.363-365.1985]

- Goh EJ, Seong ES, Lee JG, Na JK, Lim JD, Kim MJ, Kim NY, Lee GH, Seo JS, Cheoi SD, Chung IM and Yu CY. (2009). Antioxidant activities according to peeling and cultivated years of Astragalus membranaceus roots. Korean Journal of Medicinal Crop Science. 17:233-237.
-
Hirotani M, Zhou Y, Lui H and Furuya T. (1994). Astragalosides from hairy root cultures of Astragalus membranaceus. Phytochemistry. 36:665-670.
[https://doi.org/10.1016/S0031-9422(00)89793-9]

-
Hsu C, Wu B, Chang Y, Chang C, Chiou T and Su N. (2018). Phosphorylation of isoflavones by Bacillus subtilis BCRC 80517 may represent xenobiotic metabolism. Journal of Agricultural and Food Chemistry. 66:127-137.
[https://doi.org/10.1021/acs.jafc.7b04647]

-
Hsu M and Chiang B. (2009). Effect of Bacillus subtilis natto-fermented radix astragali on collagen production in human skin fibroblasts. Process Biochemistry. 44:83-90.
[https://doi.org/10.1016/j.procbio.2008.09.021]

-
Ibe S, Kumada K, Yoshiba M and Onga T. (2001). Production of nattowhich contains a high level of isoflavone aglycons. Journal of the Japanese Society for Food Science and Technolgy. 48:27-34.
[https://doi.org/10.3136/nskkk.48.27]

- Im KR, Kim MJ, Jung TK and Yoon KS. (2010). Analysis of isoflavonoid contents in Astragalus membranaceus bunge cultivated in different areas and at various ages. Korean Society for Biotechnology and Bioengineering Journal. 25:271-276.
-
Izumi T, Piskula MK, Osawa S, Obata A, Tobe K, Saito M, Kataoka S, Kubota Y and Kikuchi M. (2000). Soy isoflavone aglycones are absorbed faster and in higher amounts than their glucosides in humans. Journal of Nutrition. 130:1695-1699.
[https://doi.org/10.1093/jn/130.7.1695]

-
Kim JH, Kim MR, Lee ES and Lee CH. (2009). Inhibitory effects of calycosin isolated from the root of Astragalus membranaceus on melanin biosynthesis. Biological and Pharmaceutical Bulletin. 32:264-268.
[https://doi.org/10.1248/bpb.32.264]

- Kim MJ, Lim KR, Jung TK and Yoon KS. (2007). Anti-aging effect of Astragalus membranaceus root extract. Journal of the Society of Cosmetic Scientists of Korea. 33:33-40.
-
Kong X, Wang F, Niu Y, Wu X and Pan Y. (2018). A comparative study on the effect of promoting the osteogenic function of osteoblasts using isoflavones from Radix Astragalus. Phytotherapy Research. 32:115-124.
[https://doi.org/10.1002/ptr.5955]

-
Kuo L, Cheng W, Wu R, Huang C and Lee K. (2006). Hydrolysis of black soybean isoflavone glycosides by Bacillus subtilis natto. Applied Microbiology and Biotechnology. 73:314-320.
[https://doi.org/10.1007/s00253-006-0474-7]

- Lee SH, Koo SC, Han JW, Lee WM and Hur M. (2018a). Selection of short stem Astragalus membranaceus lines by assessing agronomic characteristics and biological activity. Korean Journal of Medicinal Crop Science. 26:471-476.
- Lee SY, Lee HN, Go EJ, Park YC, Choi SK, Yu CY and Lim JD. (2018b). Effect of Astragalus membranaceus polysaccharides on improves immune response after exhaustive exercise rats. Korean Journal of Medicinal Crop Science. 26:72-81.
-
Lin L, He X, Lindenmaier M, Nolan G, Yang J, Cleary M and Cordell G. (2000). Liquid chromatography-electrospray ionization mass spectrometry study of the flavonoids of the roots of Astragalus mongholicus and A. membranaceus. Journal of Chromatography A. 876:87-95.
[https://doi.org/10.1016/S0021-9673(00)00149-7]

-
Lindell SS and Quinn P. (1975). Use of bile-esculin agar for rapid differentiation of enterobacteriaceae. Journal of Clinical Microbiology. 1:440-443.
[https://doi.org/10.1128/JCM.1.5.440-443.1975]

-
Pan H, Fang C, Zhou T, Wang Q and Chen J. (2007). Accumulation of calycosin and its 7-O-β-D-glucoside and related gene expression in seedlings of Astragalus membranaceus Bge. var. mongholicus(Bge.) Hsiao induced by low temperature stress. Plant Cell Reports. 26:1111-1120.
[https://doi.org/10.1007/s00299-006-0301-8]

-
Park JY, Lee JY, Kim HD, Jang GY and Seo KH. (2019). Changes in the constituents and UV-photoprotective activity of Astragalus membranaceus caused by roasting. Journal of Nutrition and Health. 52:413-421.
[https://doi.org/10.4163/jnh.2019.52.5.413]

-
Park YC, Lee JS, Kim DY, Son HY, Lee JW, Cheoi YS, Kim KK, Yu CY, Chung IM, Im MH, Lee KJ, Choi RN, Shim HS and Lim JD. (2013). A 90 day repeated dose-oral toxicity study of extracts from Astragalus membranaceus-aboveground parts in rats. Korean Journal of Medicinal Crop Science. 21:474-485.
[https://doi.org/10.7783/KJMCS.2013.21.6.474]

-
Ra KS, Oh SH, Kim JM and Suh HJ. (2004). Isolation of fibrinolytic enzyme and β-glucosidase producing strains from doenjang and optimum conditions of enzyme production. Journal Korean Society of Food Science and Nutrition. 33:439-442.
[https://doi.org/10.3746/jkfn.2004.33.2.439]

-
Re R, Pellegrini N, Proteggente A, Pannala A, Yang M and Rice-Evans C. (1999). Antioxidant activity applying an improved ABTS radical cation decolorization assay. Free Radical Biology and Medicine. 26:1231-1237.
[https://doi.org/10.1016/S0891-5849(98)00315-3]

-
Shim KS, Park GG and Park YS. (2014). Bioconversion of puffed red ginseng extract using β-glucosidase-producing lactic acid bacteria. Food Engineering Progress. 18:332-340.
[https://doi.org/10.13050/foodengprog.2014.18.4.332]

-
Wagle A, Seong SH, Jung HA and Choi JS. (2019). Identifying an isoflavone from the root of Pueraria lobata as a potent tyrosinase inhibitor. Food Chemistry. 276:383-389.
[https://doi.org/10.1016/j.foodchem.2018.10.008]

-
Wang F, Zhao S, Li F, Zhang B, Qu Y, Sun T, Luo T and Li D. (2014). Investigation of antioxidant interactions between radix Astragali and Cimicifuga foetida and identification of synergistic antioxidant compounds. Plos One. 9:87221. (cited by 2020 July 20).
[https://doi.org/10.1371/journal.pone.0087221]

-
Wang X, Fan R, Li J, Li C and Zhang Y. (2016). Molecular Cloning and Functional Characterization of a Novel (Iso)flavone 4′,7-O-diglucoside Glucosyltransferase from Pueraria lobata. Frontiers in plant science. 7:387. (cited by 2020 July 19).
[https://doi.org/10.3389/fpls.2016.00387]

-
Wang X. (2011). Structure, function, and engineering of enzymes in isoflavonoid biosynthesis. Functional Integrative Genomics 11:13-22.
[https://doi.org/10.1007/s10142-010-0197-9]

-
Wünsch E and Heidrich HG. (1963). Zur quantitativen bestimmung der kollagenase. Hoppe-Seyler´s Zeitschrift für physiologische Chemie. 333:149-151.
[https://doi.org/10.1515/bchm2.1963.333.1.149]

- Yagi A, Kanbara T and Morinobu N. (1986). The effect of tyrosinase inhibition for aloe. Planta Medica. 3981:517-519.
-
Yang SJ, Lee SY, Lee HN, Park YC, Choi SK, Yu CY, Chung IM and Lim JD. (2016). Adjuvant effect of polysaccharides from aboveground parts of Astragalus membranaceus. Korean Journal of Medicinal Crop Science. 24:408-419.
[https://doi.org/10.7783/KJMCS.2016.24.5.408]