건조 방법에 따른 환삼덩굴 추출물 중 Luteolin 유도체의 함량 변화
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
The main compounds in the Humulus japonicus extract prepared by drying for 12 h under hot air at 50℃ (50-12H), or 7 d, at room temperature at 25℃ (25-7D) were analyzed.
Three main compound peaks were identified in liquid chromatograph analysis using an ultraviolet detector. Additionally, mass spectrometer analysis was performed, and each peak was confirmed to either belong to luteolin 7-O-glucoside, luteolin 4'-O-glucoside, or luteolin through standard analysis. The 50-12H extract showed high contents of luteolin 7-O-glucoside and luteolin 4’-O-glucoside. Meanwhile, in the 25-7D extract, the luteolin 7-O-glucoside and luteolin 4’-O-glucoside contents reduced and the luteolin content increased, this is because luteolin 7-O-glucoside and luteolin 4’-O-glucoside decomposed into luteolin and glucose by the action of hydrolytic enzymes. In other words, a relatively slow drying speed provides enough time for hydrolytic enzyme to be activiated in H. japonicus, which increases the luteolin content.
Room temperature drying is suitable for increasing the luteolin content in H. japonicus extract, and a fast heat drying method is suitable for increasing the luteolin glycoside content.
Keywords:
Humulus japonicus, Liquid Chromatography, Luteolin Derivative, Mass Spectroscopy서 언
환삼덩굴 (Humulus japonicus)은 삼과의 한해살이풀로서 줄기에 존재하는 갈고리 모양의 가시를 이용하여 다른 물체나 식물에 붙어서 덩굴을 이루며 자라는 특성이 있다 (Hong et al., 2014). 이와 같은 특성과 함께 왕성한 번식력으로 주변 식물의 생존을 방해하는 생태계 교란 종으로 지정되어 있으며, 일정 시기에 꽃가루를 다량 발생시켜 사람에게 알레르기를 일으키기도 하는 것으로 보고되고 있다 (Kim et al., 2023a).
전초는 혈압을 낮추는 효과가 있으며, 열매는 이뇨작용이 있는 것으로 알려져 ‘율초 (葎草)’라는 명칭으로 오래전부터 약재로서 사용된 기록이 있으나 현재는 임상에서 활용도는 낮은 것으로 보고되고 있다 (Hwang et al., 2009).
환삼덩굴의 추출물을 이용한 활성 연구에서 항산화 활성 (Park et al., 2000; Chae et al., 2021; Wang et al., 2022b), 항염증 관련 활성 (Hwang et al., 2009)과 관절염 개선 효과 (Kang et al., 2020)를 나타내는 것으로 확인되었다. 또한 인지 장애나 신경염증 관련 개선 효과 (Go et al., 2022; Wang et al., 2022a) 뿐만이 아니라 Alzheimer나 Parkinson 질환 관련 활성 도 보고되었다 (Kang et al., 2022; Lee et al., 2019). 이와 함께 피부 관련 효과로서 광노화를 억제하는 효과 (Nam et al., 2020)와 아토피나 피부염 등 피부질환 관련 활성을 나타내는 것으로 확인되었다 (Park et al., 2019b; Kim et al., 2023b). 이 외에도 지방간 개선 효과 (Cho et al., 2023) 와 항결핵 효과 등에 대한 연구도 진행되었었다 (Hong et al., 2014).
환삼덩굴의 활성 성분에 대한 연구에서는 apigenin 7-O-glucoside와 같은 apigenin 배당체와 luteolin 7-O-glucoside와 같은 luteolin 배당체, 그리고 quercitrin, luteolin 등과 같은 flavonoid 성분들이 다양한 생리 활성에 관여하고 있는 것으로 보고되었다 (Park et al., 1995; Nam et al., 2020; Park et al., 2000; Lee et al., 2019; Wang et al., 2022a; Cho et al., 2023).
건조 과정은 식물의 성분이나 활성에 영향을 미치는 요소 중 하나이며, 목적하는 수분 함량 수준을 달성하기 위하여 적용할 가열온도와 시간, 그리고 건조 방법 등이 검토된다. 함초의 항혈전 활성 관련 일부 연구를 제외하면 (Sung et al., 2017), 일반적으로 가장 열에 노출이 적은 동결건조가 성분이나 활성 유지에 적합한 방법으로 보고되고 있으나 비용이나 시간적인 측면에서 비교적 고가의 약용 자원이나 연구목적의 건조에만 적용되는 한계가 있다 (Lee, 2018; Youn et al., 2019; Yun and Kang, 2021).
따라서 산업적인 목적에는 상온에서 이루어지는 자연건조나 열풍을 이용하는 가열건조 방법이 보다 적합하며, 식물 소재 별 특성을 반영한 조건 설정 및 적용이 필요하게 된다.
본 연구에서는 건조 방법을 달리한 환삼덩굴 추출물의 성분 변화를 확인하고 주요 성분에 대한 함량 변화를 확인하기 위하여 25℃의 상온건조와 50℃의 가열건조 방법을 적용한 추출물을 제조하여 액체크로마토그래프 (liquid chromatograph; LC) 분석으로 주요 성분의 변화를 확인하였다. LC 분석에서 확인된 변화 성분에 대한 질량분석을 실시하여 1차적인 성분 검토를 실시하였으며, 확인된 성분의 표준품을 활용한 대조 분석을 실시하여 정확한 함량 변화 수준을 확인하였다.
재료 및 방법
1. 식물재료 및 시약
환삼덩굴 (Humulus japonicus) 시료는 전남 장흥 지역에서 자생하는 것을 지상부 기준 600 g을 채집하여 사용하였다. 시료는 균일하게 혼합 및 분배하여 25℃의 상온에서 7 일간 음건한 것 (25-7D)과 50℃의 건조기에서 12 시간 동안 가열 건조한 것 (50-12H)으로 구분하였다. Luteolin, luteolin 7-O-glucoside, luteolin 4’-O-glucoside 표준품은 Sigma-Aldrich (St. Louis, MO, USA)에서 구입한 것을 사용하였다.
2. 추출물 제조
조건별로 건조된 환삼덩굴 시료는 동일한 입자 크기로 분쇄를 실시하였으며, 분쇄된 각 시료 5 g에 메탄올 100 ㎖를 혼합하여 분당 180 회의 속도를 적용한 진탕추출을 24 시간 동안 실시하였다. 건조 조건별로 3회 실시된 추출액의 상등액 일정량을 0.45 ㎛ syringe filter (Whatman, Maidstone, England) 로 여과를 실시한 후 4℃ 이하로 냉장 보관하면서 분석에 사용하였다.
3. 환삼덩굴 추출물의 성분 분석
환삼덩굴 추출물의 성분 분석을 위해 Gemini NX-C18 (4.6 ㎜ × 150 ㎜, 3 ㎛, Phenomenex, Torrance, CA, USA) column을 장착한 LC-30A (Shimadzu, Kyoto, Japan) 액체크로마토그래피 (liquid chromatograph; LC) 시스템을 사용하였다.
시료 주입량은 5 ㎕, column oven은 40℃를 유지하였으며, 이동상으로 0.1% formic acid (A)와 acetonitrile (B)을 사용하여 유속은 0.6 ㎖/min으로 유지하였다. 이동상은 초기 5 분까지 20% B, 5 분에서 22 분까지 20% B에서 65% B가 되도록 하였고, 이후 26 분까지 65% B에서 100% B가 되도록 하였으며, 32 분까지 100% B를 유지한 후 다시 20% B로 낮춰서 40 분간 측정 및 분석을 실시하였다.
주요 peak의 UV spectra는 215 ㎚ − 400 ㎚ 범위에 측정하였으며, 정량분석을 위한 검출기 (SPD-10Avp, Shimadzu, Kyoto, Japan) 파장은 350 ㎚로 설정하였다. 정량분석을 위한 luteolin 표준품 용액은 2.0 ㎎/㎖, 0.5 ㎎/㎖, 0.1 ㎎/㎖, 0.02 ㎎/㎖ 농도로 조제하였으며, luteolin 7-O-glucoside와 luteolin 4’-O-glucoside 표준품 용액은 1.0 ㎎/㎖, 0.25 ㎎/㎖, 0.05 ㎎/㎖, 0.01 ㎎/㎖ 농도로 조제하여 분석에 사용하였다.
4. 주요 변화 성분의 LC-MS/MS 분석
건조 방법에 따른 주요 변화 성분 peak에 대한 질량분석은 LC-30A (Shimadzu, Kyoto, Japan) 액체크로마토그래피와 연동된 LCMS-8050 (Shimadzu, Kyoto, Japan) 질량분석기 (mass spectrometer; MS)를 사용하였으며, LC 분석 조건과 동일한 분리 조건을 적용하였다.
MS 분석을 위한 interface와 desolvation line, 그리고 heat block 온도는 각각 300℃, 250℃, 350℃로 설정하였으며, nebulizing gas, drying gas, heating gas는 각각 3 ℓ/min, 9 ℓ/min, 9 ℓ/min으로 공급하였다. MS2 분석을 위한 collision-induced dissociation gas인 argon은 270 kPa의 압력으로 공급하였으며, positive와 negative mode에서 100 m/z - 1,000 m/z의 범위의 MS scan 분석을 실시한 후 확인된 모분자량을 적용하여 추가로 MS2 분석을 실시하였다.
결과 및 고찰
1. LC profile 분석 결과
약용 식물의 경우 건조를 통해 수분 함량을 낮춤으로써 저장기간 동안 성분 변화나 변질을 줄일 수 있으며, 이로 인해 저장 기간을 연장시키는 데 필수적인 과정으로 활용되고 있다. 또한 건조를 통해 식물 원료의 분쇄를 쉽게 하며, 추출 과정에서 수율을 증진시키는 등의 효과를 얻을 수 있다 (Choi et al., 2016; Hur et al., 2018; Choi et al., 2022).
약용 식물의 건조 방법으로서 기본적인 상온건조와 함께 열풍건조 등 가열건조 방법이 상업적으로 가장 빈번하게 이용되고 있으며, 연구 목적이나 고가의 원료의 건조에 진공건조나 동결건조 방법이 사용되고 있다 (Lee. 2018; Youn et al., 2019; Yun and Kang, 2021).
국내에서의 상온건조는 계절이나 환경적인 영향에 따라 편차가 있을 수는 있지만 25℃ 내외의 온도로 원료의 수분이 목적하는 수준까지 도달시키는 단순한 과정으로 이루어지며, 건조 공간의 상대습도나 기류의 영향을 받게 된다.
건조 대상의 크기나 모양, 성분 등에 따라 건조에 필요한 시간이 다양하지만 환삼덩굴과 같은 경우 3 일 − 5 일 수준의 건조 시간이 소요된다. 반면, 통상 40℃ 이상의 고온을 사용하는 가열건조는 상온 건조에 비해 건조시간이 짧으며, 열풍건조와 같이 부가적인 기류를 사용하는 가열건조 방법은 건조 시간을 더욱 단축시킬 수 있다.
상온건조와 마찬가지로 건조 대상 원료 특성에 따라 다르지만 환삼덩굴을 기준으로 50℃ 열풍건조 방법을 적용하면 8 시간 − 12 시간 수준의 건조 시간이 소요된다. 건조 시간을 단축시키기 위해 가열 온도를 높일 수 있지만 온도에 민감한 성분의 변화가 나타날 수 있으므로 일반적인 가열 건조는 60℃ 이하의 조건이 우선적으로 검토되고 있다 (Eom et al., 2009; Kim et al., 2013; Jeong et al., 2015).
50℃의 열풍으로 12 시간 건조한 환삼덩굴 시료 (50-12H)와 25℃의 상온에서 7 일간 건조한 시료 (25-7D)의 메탄올 추출물의 자외선 (ultraviolet; UV) 검출기를 적용한 액체크로마토그래프 (liquid chromatogrraph; LC) 분석을 실시한 결과, Fig. 1과 같이 머무름 시간 9.64 분, 11.86 분, 16.12 분에 나타난 peak a, b, c의 변화가 확인되었다.
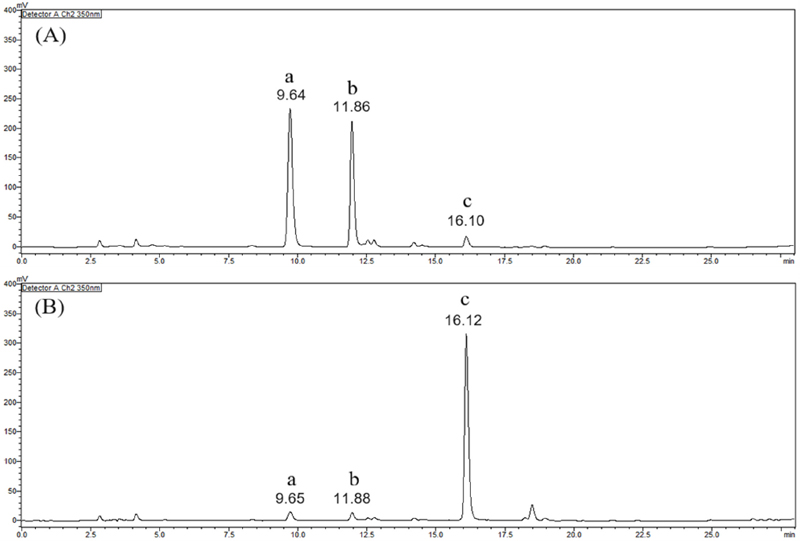
LC chromatograms of Humulus japonicus extract by drying method.(A) Chromatogram of extracts using hot air drying method (50℃, 12 hours), (B) Chromatogram of extracts using room temperature drying method (25℃, 7 days). Different superscripts are major peaks.
구체적으로는 50-12H 추출물에서는 peak a와 b가 특징적으로 큰 peak 면적을 나타냈으며, peak c는 현저히 적은 peak 면적을 나타냈다. 25-7D 추출물에서 peak a와 b의 peak 면적은 급격히 적어졌으며, peak c의 면적은 반대로 커진 것을 확인할 수 있었다.
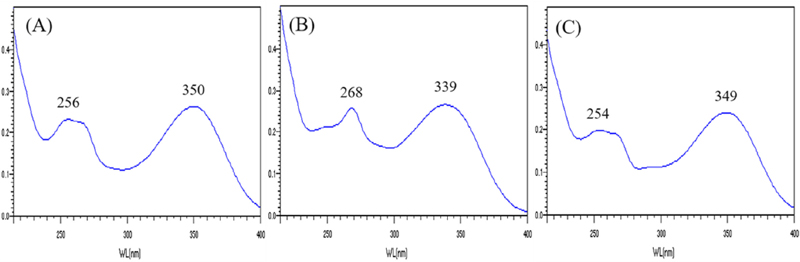
확인된 주요 peak의 성분 특성 관련 정보를 추가로 확보하기 위하여 각 peak의 UV spectrum 측정하였으며, Fig. 2와 같은 결과를 확인할 수 있었다.
2. 주요 peak의 LC-MS 분석
Peak a, b, c에 해당하는 성분에 대한 정성 분석과 함께 건조 방법에 따른 성분 변화의 유형을 검토하기 위해서 LC 분석과 동일한 분리 조건을 적용한 질량분석기 (mass spectrometer; MS) 분석을 실시하였다.
Scan mode의 MS 분석 결과를 제시한 Fig. 3과 Fig. 4에서 peak a와 b는 positive mode와 negative mode에서 각각 [M+H]+와 [M-H]-의 형태인 449.1 m/z와 447.1 m/z가 확인되었으며, positive mode에서는 추가로 [M+Na]+ 형태인 471.1 m/z가 나타났다. Peak a와 b의 MS2 분석에서는 positive mode와 negative mode에서 각각 287 m/z와 285 m/z가 특징적으로 나타났으며, 나머지 조각 ion들의 패턴에서도 유사한 부분이 확인되었다.
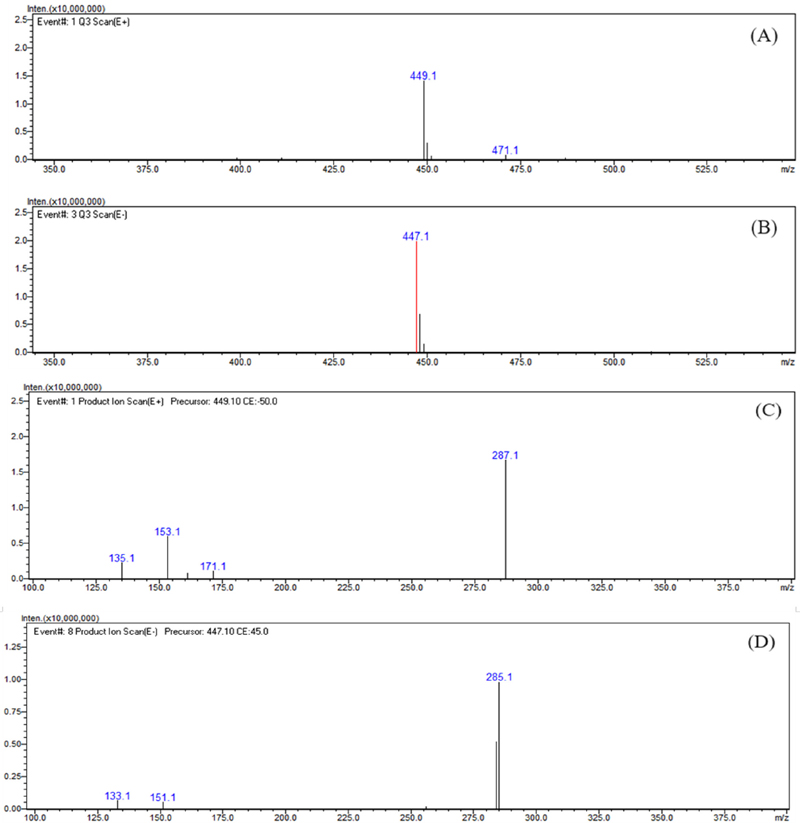
LC-MS analysis results of the major peak a.(A) positive mode MS spectra of the major peak a, (B) negative mode MS spectra of the major peak a, (C) positive mode MS2 spectra of 449.1 m/z ([M+H]+), (D) negative mode MS2 spectra of 447.1 m/z ([M-H]-).
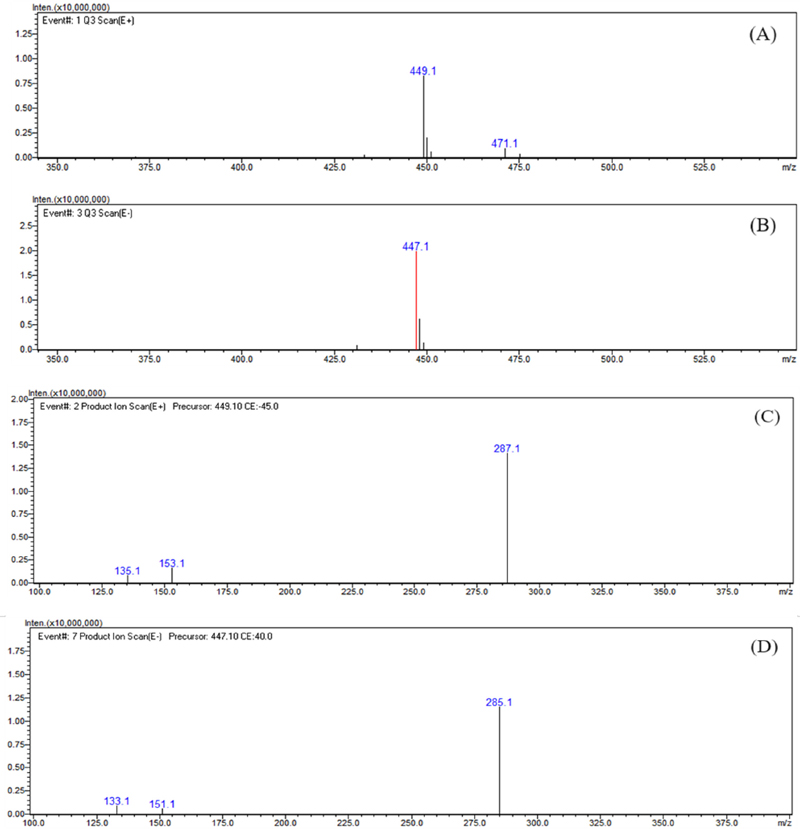
LC-MS analysis results of the major peak b.(A) positive mode MS spectra of the major peak b, (B) negative mode MS spectra of the major peak b, (C) positive mode MS2 spectra of 449.1 m/z ([M+H]+), (D) negative mode MS2 spectra of 447.1 m/z ([M-H]-).
Fig. 5에 제시한 peak c의 MS 분석 결과에서 positive mode와 negative mode에서 각각 [M+H]+와 [M-H]-의 형태인 287.1 m/z와 285.1 m/z가 확인됨에 따라 분자량이 286인 성분으로 추정할 수 있었다. MS2 분석에서는 positive mode에서 153 m/z, 135 m/z, 171 m/z 등의 조각 ion들이 확인되었다. Negative mode에서는 133 m/z가 강하게 나타났으며, 175 m/z, 151 m/z 등의 조각 ion이 확인되었다. 이와 같은 MS 및 MS2 분석 결과는 기존 문헌 검토를 통해 luteolin 성분에서 나타나는 형태임을 알 수 있었다 (Shin et al., 2018; Xu et al., 2022). 또한 Fig. 2에 제시한 peak c의 UV spectrum에서도 기존의 연구보고들에서 제시하고 있는 luteolin의 UV spectrum과 동일 또는 유사함을 확인하였다 (Lech et al., 2014; Iwashina et al., 2020).
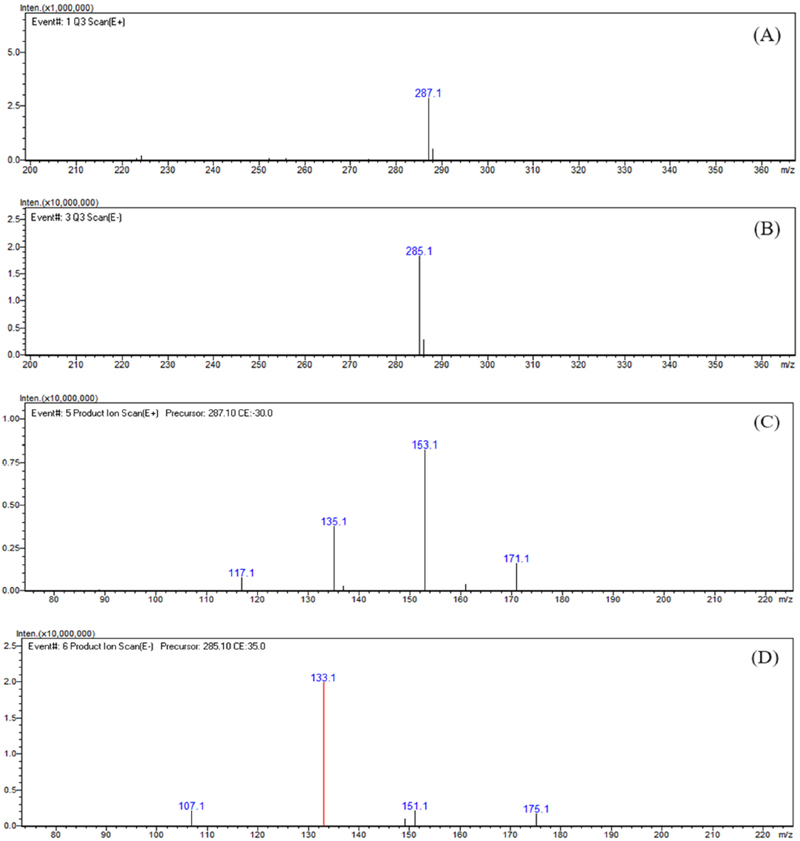
LC-MS analysis results of the major peak c.(A) positive mode MS spectra of the major peak c, (B) negative mode MS spectra of the major peak c, (C) positive mode MS2 spectra of 287.1 m/z ([M+H]+), (D) negative mode MS2 spectra of 285.1 m/z ([M-H]-).
한편, peak a와 b의 MS2 분석에서 positive mode의 287 m/z와 negative mode의 285 m/z가 공통적으로 확인된 결과는 peak c 성분으로 검토되는 분자량 286의 luteolin 구조가 peak a와 b 성분에 포함되었다는 판단을 가능케 하였다.
결과적으로 peak a, b는 분자량 448을 가지며, luteolin을 aglycone으로 포함하는 성분이므로 glucose와 같은 hexose를 포함하는 것으로 추정이 가능하였다. 관련된 문헌 검토를 통해 Fig. 2에 제시한 것과 같은 UV spectrum을 나타내는 성분으로서 luteolin 7-O-glucoside와 luteolin 4’-O-glucoside로 확인하고 표준품을 확보하여 대조 분석을 실시하였다 (Yuan et al., 2018; Iwashina et al., 2020).
3. 환삼덩굴 추출물 주성분 함량 비교 분석
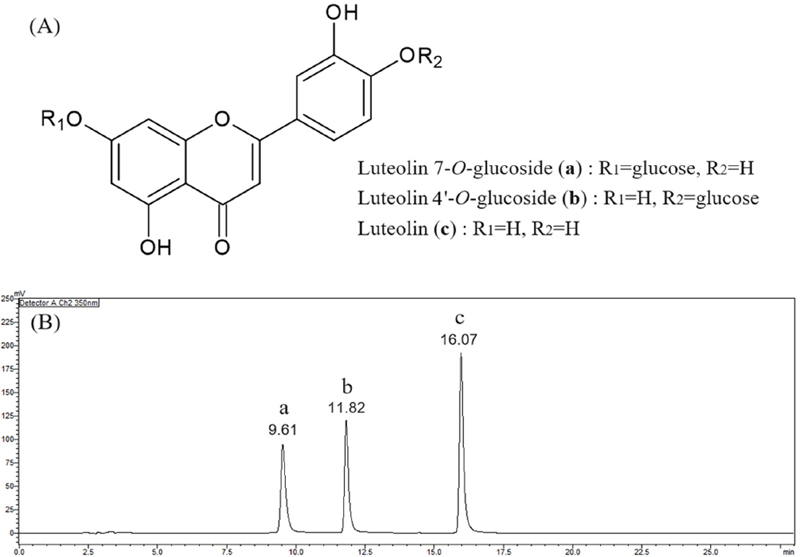
LC 및 LC-MS 분석 결과를 바탕으로 실시한 표준품 대조 분석 결과에서 peak a, b, c가 Fig. 6에 제시한 것과 같이 각각 luteolin 7-O-glucoside, luteolin 4’-O-glucoside, luteolin임을 확인하였다.
Luteolin은 환삼덩굴을 포함한 다양한 식물에서 발견되는 flavone 구조의 성분으로서 다양한 생리활성을 나타내는 것으로 알려져 있다 (Sung et al., 2015; Xu et al., 2022). 대표적인 활성으로서 항산화와 다양한 항염증 관련 효과가 있으며 (Sung et al., 2015; Wang et al., 2022a; Xu et al., 2022; Kim et al., 2023b), 고요산혈증과 통풍성 관절염 치료 효과나 Parkinson 질환 관련 활성도 나타내는 것으로 보고되고 있다 (Lin et al., 2018; Lee et al., 2019).
Luteolin 7-O-glucoside는 cynaroside나 luteoloside로 불리기도 하는 성분으로서 환삼덩굴뿐만이 아니라 다양한 식물에서 발견되고 있으며 (Xu et al., 2022; Ryu and Ma, 2023), luteolin과 같이 항산화 활성이나 Parkinson 질환 관련 활성을 나타내는 것으로 알려져 있다 (Sung et al., 2015; Lee et al., 2019). 또한 피부의 광노화 억제 효과나 알콜로 인한 간 손상을 예방하는 효과에 대한 보고도 있었다 (Nam et al., 2020; Cho et al., 2023).
Luteolin 4’-O-glucoside는 떡쑥 (Gnaphalium affine)이나 매듭풀 (Kummerowia striata) 등의 식물에 존재하는 것으로 보고되는 luteolin 배당체로서 항산화 활성과 함께 interleukin (IL)-5 억제를 통한 알레르기 염증 억제 효과와 통풍성 관절염 관련 치료 효과 등이 있는 것으로 보고되고 있다 (Park et al., 1999; Lin et al., 2018; Xu et al., 2022).
각 표준품의 농도별 용액을 조제하여 환삼덩굴 추출물 분석조건과 동일한 조건에서 분석을 실시한 후 작성한 검량선 정보를 Table 1에 제시하였다. 정량분석 결과의 정확성을 위하여 농도별 표준품 용액 분석을 추출물 시료들의 분석 이전과 이후에 2회 측정하여 평균값을 적용하는 협차 검량법 (bracket calibration)을 적용하였으며, 분석이 실시된 농도 범위에서 세 가지 성분 모두 우수한 직선성을 나타내었다. 또한 Fig. 6(B) 에 제시한 것과 같이 각 성분간 간섭 현상도 나타나지 않아 세 가지 성분의 동시 분석에도 문제가 없음을 확인하였다.
Table 2에 제시한 건조 방법별 환삼덩굴 추출물에 대한 정량 분석 결과에서 상대적으로 고온에서 단시간 건조를 실시한 50-12H 추출물에서는 luteolin 7-O-glucoside, luteolin 4’-O-glucoside의 함량이 각각 0.480 ㎎/㎖와 0.318 ㎎/㎖로 나타났으며, luteolin 함량은 0.030 ㎎/㎖ 수준으로 확인되었다. 반면, 상온에서 장시간 건조를 실시한 25-7D 추출물에서는 luteolin 7-O-glucoside, luteolin 4’-O-glucoside의 함량이 각각 0.058 ㎎/㎖와 0.043 ㎎/㎖로 50-12H보다 낮게 나타났으며, luteolin 함량은 0.663 ㎎/㎖로 50-12H보다 높게 나타났다.
한편, 추출에 사용된 건조 환삼덩굴 시료량 (5 g)과 추출용 매의 부피 (100 ㎖)를 감안하면 50-12H 건조 시료 중의 luteolin 7-O-glucoside와 luteolin 4’-O-glucoside의 함량이 각각 9.60 ㎎/g, 6.36 ㎎/g 수준이며, 25-7D 건조 시료 중의 luteolin 함량 수준이 13.26 ㎎/g임을 알 수 있었다.
본 연구에서 확인된 환삼덩굴의 주요 성분 중 peak a와 peak b에 해당하는 luteolin 7-O-glucoside와 luteolin 4’-O-glucoside는 Fig. 6(A)에 나타낸 바와 같이 구조적으로 β-glucosidase와 같은 가수분해 효소의 작용으로 peak c의 luteolin과 glucose로 분해될 수 있다. 환삼덩굴과 같은 식물소재는 채취나 수확 이후에도 일정 시간 동안 생명 현상이 지속되며, 이러한 생명 현상의 하나로 자체 효소 작용으로 인한 성분이나 색상 등의 변화가 나타난다. 이러한 변화 자체가 바람직한 경우도 있지만, 반대로 억제되어야 할 경우도 있는데, 산업화 및 품질관리 측면에서는 목적하는 방향으로 일정하게 관리할 필요가 있다.
자체 효소의 작용에 영향을 미치는 다양한 요인 중에서 특히 온도와 수분 이 중요한 것으로 알려져 있으며, 특히 가수분해 (hydrolysis)와 관련된 경우에는 수분 함량이 결정적인 영향을 주기도 한다. 효소에 의한 flavonoid glycoside의 분해 및 전환은 다양한 식물 소재에서 다뤄지고 있으며, 대부분은 가수분해의 과정을 거치는 것으로 보고되고 있다 (Slámová et al., 2018; Yuan et al., 2018; Hwang et al., 2023).
국내에서도 flavonoid 성분 함량이 높은 것으로 알려진 감귤류 유래의 소재를 중심으로 효소 작용으로 나타나는 flavonoid 배당체와 비배당체의 함량 변화에 대한 연구가 있었으며, 본 연구의 결과와 같이 가수분해 효소 작용에 의한 flavonoid 비배당체 함량이 증가되는 것으로 보고하고 있다 (Ahn et al., 2005; Park et al., 2019a; Shin et al., 2020).
따라서 식물 소재가 가지고 있는 자체 효소에 의한 가수분해를 제어하기 위해서는 건조 과정에서의 건조 속도와 같은 수분 변화 양상을 검토할 필요가 있다. Table 2의 결과와 병행하여 검토하면 상온에서 상대적 느린 건조 속도로 건조 과정이 수행되면 환삼덩굴 자체에 포함된 가수분해 효소의 작용 가능 시간이 그만큼 증가하게 되며, 이로 인해 luteolin 배당체가 분해되어 luteolin으로 전환되는 비율이 증가되는 것으로 판단할 수 있다.
한편, 효소의 작용에는 온도 역시 중요한 요인이며, 가열 수준에 따라 수분 함량과 관계없이 효소의 비활성화가 성분변화에 영향을 나타낼 수 있으므로 본 연구를 통해 확인된 기본적인 건조 방법에 따른 성분 변화 차이 외에도 가열 온도나 시간 등 보다 다양한 변수들을 적용한 추가적인 연구가 환삼덩굴의 산업적 이용을 위해서 이루어질 필요가 있을 것이다.
References
- Ahn SC, Kim MS, Lee SY, Kang JH, Kim BH, Oh WK, Kim BY and Ahn JS. (2005). Increase of bioactive flavonoid aglycone extractable from Korean citrus peel by carbohydrate-hydrolysing enzymes. Korean Journal of Microbiology and Biotechnology. 33:288-294.
- Chae JW, Jo HS, Yeom HJ and Lee JY. (2021). Antioxidation and functional cosmetics activity of Humulus japonicus Sieboid & Zucc. according to collection time and extraction solvent. Journal of Korean Society of Forest Science. 110:254-265.
-
Cho WJ, Park SY, Oh H, Abd El-Aty AM, Hacimüftüoğlu A, Kim DS, Jung, TW and Jeong JH. (2023). Humulus japonicus extract ameliorates hepatic steatosis through the PPAR α-mediated suppression of alcohol-induced oxidative stress. Journal of Medicinal Food. 26:193-200.
[https://doi.org/10.1089/jmf.2022.K.0093]

-
Choi JS, Kong MH, Yeo SH, Choi HS and Jeong ST. (2016). Effects of pretreatments and storage temperature on the quality of lotus leaves. Korean Journal of Food Preservation. 23:155-161.
[https://doi.org/10.11002/kjfp.2016.23.2.155]

-
Choi SY, Chae HB, Hwang IJ, Hyun JE, Seo WD and Kim SR. (2022). Effects of different drying methods and storage conditions on the reduction of Escherichia coli and the quality parameters of barley sprouts. Korean Journal of Food Preservation. 29:1047-1058.
[https://doi.org/10.11002/kjfp.2022.29.7.1047]

- Eom HJ, Kim SM, Pyo BS and Lee KI. (2009). Changes of physiological activity by drying temperature in leaf of Eriobotrya japonica. Korean Journal of Pharmacognosy. 40:178-183.
-
Go J, Park HY, Lee DW, Maeng SY, Lee IB, Seo YJ, An JP, Oh WK, Lee CH and Kim KS. (2022). Humulus japonicus attenuates LPS-and scopolamine-induced cognitive impairment in mice. Laboratory Animal Research. 38:21. https://labanimres.biomedcentral.com/articles/10.1186/s42826-022-00134-3, (cited by 2023 Sep 16).
[https://doi.org/10.1186/s42826-022-00134-3]

-
Hong MS, Son ES, Lee SJ, Lee SK, Lee YJ, Song SD, Cho SN, Barry CE and Eum SY. (2014). Anti-mycobacterial effects of the extract of Humulus japonicus. Korean Journal of Food Science and Technology. 46:94-99.
[https://doi.org/10.9721/KJFST.2014.46.1.94]

- Hur YJ, Kim GJ, Song DH, Yoon JA, Chung KH and An JH. (2018). Effects of drying methods on the quality characteristics and antioxidant activity of pumpkin(Cucurbita moschata Duch.). The Korean Journal of Food And Nutrition. 31:933-939.
-
Hwang JT, Kim HJ, Ryuk JA, Jung DH and Ko BS. (2023). Efficiency of the enzymatic conversion of flavone glycosides isolated from carrot leaves and anti-inflammatory effects of enzyme-treated carrot leaves. Molecules. 28:4291. https://www.mdpi.com/1420-3049/28/11/4291, (cited by 2023 Oct 14).
[https://doi.org/10.3390/molecules28114291]

- Hwang SY, Jo MJ, Kim SC and Jee SY. (2009). Anti-inflammatory effects of the MeOH extract of Humulus japonicus in vitro. The Journal of Korean Oriental Medical Ophthalmology and Otolaryngology and Dermatology. 22:92-103.
- Iwashina T, Mizuno T and Devkota HP. (2020). Further identification of flavonoids deposited in the National Museum of Nature and Science in Japan - Flavonoids isolated from Cirsium Taxa and Carduus nutans (Asteraceae). Bulletin of the National Museum of Nature and Science, Series B, 46:195-214.
-
Jeong DW, Park YK, Nam SS and Han SK. (2015). Effect of hot-air drying temperature on antioxidative activity of sweet potato leaves. Korean Journal of Food Preservation. 22:708-713.
[https://doi.org/10.11002/kjfp.2015.22.5.708]

-
Kang CM, Bang JS, Park SY, Jung TW, Kim HC, Chung YH and Jeong JH. (2022). The aqueous extract of Humulus japonicus ameliorates cognitive dysfunction in Alzheimer’s disease models via modulating the cholinergic system. Journal of Medicinal Food. 25:943-951.
[https://doi.org/10.1089/jmf.2021.K.0197]

-
Kang E, Kim HJ, Choi JH, Noh JR, Kim JH, Lee IB, Choi YK, Choi DH, An JP, Oh WK, Kim YH and Lee CH. (2020). Humulus japonicus extract ameliorates collagen-induced arthritis in mice through regulation of overall articular inflammation. International Journal of Molecular Medicine. 45:417-428.
[https://doi.org/10.3892/ijmm.2019.4417]

- Kim SJ, Kim MG, Boo KH and Kim CS. (2023a). Comparative evaluation of biological activities and active compounds of some invasive alien plants. Korean Journal of Plant Resources. 36:264-274.
-
Kim YB, Kang EJ, Noh JR, An JP, Park JT, Oh WK, Kim YH and Lee CH. (2023b). Humulus japonicus ameliorates irritant contact dermatitis by suppressing NF-κB p65-dependent inflammatory responses in mice. Experimental and Therapeutic Medicine. 26:446. https://www.spandidos-publications.com/10.3892/etm.2023.12145, (cited by 2023 Sep 16).
[https://doi.org/10.3892/etm.2023.12145]

-
Kim YS, Choi SK, Yun KW, Seo YN and Seo KS. (2013). Studies on the production and optimal drying condition of Curcuma longa L. Korean Journal of Plant Resources. 26:450-456.
[https://doi.org/10.7732/kjpr.2013.26.4.450]

-
Lech K, Witkoś K and Jarosz M. (2014). HPLC–UV–ESI MS/MS identification of the color constituents of sawwort(Serratula tinctoria L.). Analytical and Bioanalytical Chemistry. 406:3703- 3708.
[https://doi.org/10.1007/s00216-013-7589-3]

-
Lee HJ, Dhodary B, Lee JY, An JP, Ryu YK, Kim KS, Lee CH and Oh WK. (2019). Dereplication of components coupled with HPLC-qTOF-MS in the active fraction of Humulus japonicus and it's protective effects against Parkinson's disease mouse model. Molecules. 24:1435. https://www.mdpi.com/1420-3049/24/7/1435, (cited by 2023 Sep 16).
[https://doi.org/10.3390/molecules24071435]

-
Lee JM. (2018). Comparison of nutritional components and antioxidant activities of Eclipta prostrata(L.) L. using different drying methods. Korean Journal of Community Living Science. 29:59-68.
[https://doi.org/10.7856/kjcls.2018.29.1.59]

-
Lin Y, Liu PG, Liang WQ, Hu YJ, Xu P, Zhou J, Pu JB and Zhang HJ. (2018). Luteolin-4′-O-glucoside and its aglycone, two major flavones of Gnaphalium affine D. Don, resist hyperuricemia and acute gouty arthritis activity in animal models. Phytomedicine. 41:54-61.
[https://doi.org/10.1016/j.phymed.2018.02.002]

-
Nam EJ, Yoo GH, Lee JY, Kim MS, Jhin CH, Son YJ, Kim SY, Jung SH and Nho CW. (2020). Glycosyl flavones from Humulus japonicus suppress MMP-1 production via decreasing oxidative stress in UVB irradiated human dermal fibroblasts. BMB Reports. 53:379-384.
[https://doi.org/10.5483/BMBRep.2020.53.7.253]

-
Park GH, Park JY and Chang YH. (2019a). Changes in flavonoid aglycone contents and antioxidant activities of citrus peel depending on enzyme treatment times. Journal of the Korean Society of Food Science and Nutrition. 48:542-550.
[https://doi.org/10.3746/jkfn.2019.48.5.542]

- Park HS, Kim YM and Kim HT. (2019b). A clinical study for the efficacy and safety of functional cosmetics containing Humulus japonicus extract in patients with dry skin due to mild atopic dermatitis. The Journal of Korean Medicine Ophthalmology and Otolaryngology and Dermatology, 32:24-58.
-
Park KY, Lee SH, Min BK, Lee KS, Choi JS, Chung SR, Min KR and Kim YS. (1999). Inhibitory effect of luteolin 4'-O-glucoside from Kummerowia striata and other flavonoids on interleukin-5 bioactivity. Planta Medica. 65:457-459.
[https://doi.org/10.1055/s-2006-960812]

- Park SW, Chung SK and Park JC. (2000). Active oxygen scavenging activity of luteolin-7-O-β-D-glucoside isolated from Humulus japonicus. Journal of the Korean Society of Food Science and Nutrition. 29:106-110.
- Park SW, Kim SH and Chung SK. (1995). Antimutagenic effects and isolation of flavonoids from Humulus japonicus extract. Korean Journal of Food Science and Technology. 27:897-901.
- Ryu GH and Ma CJ. (2023). Neuroprotective Activity of Cynaroside Isolated from Lysimachia christinae. Korean Journal of Pharmacognosy. 54:9-15.
-
Shin H, Park Y, Jeon YH, Yan XT and Lee KY. (2018). Identification of Polygonum orientale constituents using high-performance liquid chromatography high-resolution tandem mass spectrometry. Bioscience, Biotechnology, and Biochemistry. 82: 15-21.
[https://doi.org/10.1080/09168451.2017.1415124]

-
Shin KS, Chang HJ and Lee JH. (2020). Effect of commercial carbohydrases on the hesperetin and narigenin contents of citrus fruits. Korean Journal of Food Preservation. 27:446-456.
[https://doi.org/10.11002/kjfp.2020.27.4.446]

-
Slámová K, Kapešová J and Valentová K. (2018). “Sweet flavonoids”: Glycosidase-catalyzed modifications. International Journal of Molecular Sciences. 19:2126. https://www.mdpi.com/1422-0067/19/7/2126, (cited by 2023 Oct 14).
[https://doi.org/10.3390/ijms19072126]

-
Sung BK, Chung JW, Bae HR, Choi JS, Kim CM and Kim ND. (2015). Humulus japonicus extract exhibits antioxidative and anti-aging effects via modulation of the AMPK-SIRT1 pathway. Experimental and Therapeutic Medicine, 9:1819-1826.
[https://doi.org/10.3892/etm.2015.2302]

-
Sung HJ, Kim DH and Sohn HY. (2017). Effect of different drying methods on anti-oxidation and anti-thrombosis activities of Salicornia europaea. Korean Journal of Food Preservation. 24:658-665.
[https://doi.org/10.11002/kjfp.2017.24.5.658]

-
Wang F, Cho BO, Shin JY, Hao S and Jang SI. (2022a). Anti-neuroinflammatory activity of Humulus japonicus extract and its active compound luteolin on lipopolysaccharide-induced inflammatory response in SIM-A9 microglia via NF-κB and MAPK signaling pathways. Food Science and Technology. 42:e78621. https://www.scielo.br/j/cta/a/sW9PfJLkHP7mgt6hRyVgrzC/?format=html&lang=en, (cited by 2023 Sep 16).
[https://doi.org/10.1590/fst.78621]

-
Wang F, Shin JY, Cho BO, Hao S, Park JH and Jang SI. (2022b). Antioxidative stress effects of Humulus japonicus extracts on neuronal PC12 cells. Food Science and Technology. 42:e101921. https://www.scielo.br/j/cta/a/6y8vXYFqwFmVts6TKRZBvbQ/, (cited by 2023 Sep 16).
[https://doi.org/10.1590/fst.101921]

-
Xu T, Wang C, Jiang S, Yang T and Wu X. (2022). Glycosylation of luteolin in hydrophilic organic solvents and structure-antioxidant relationships of luteolin glycosides. RSC Advances. 12:18232-18237.
[https://doi.org/10.1039/D2RA03300C]

-
Youn KS, Park EH and Yoon KY. (2019). Quality characteristics and antioxidant activity of bitter melon(Momordica charantia L.) dried by different methods. Korean Journal of Food Preservation. 26:185-193.
[https://doi.org/10.11002/kjfp.2019.26.2.185]

-
Yuan S, Yin S, Liu M and Kong JQ. (2018). Isolation and characterization of a multifunctional flavonoid glycosyltransferase from Ornithogalum caudatum with glycosidase activity. Scientific Reports. 8:5886. https://www.nature.com/articles/s41598-018-24277-3, (cited by 2023 Oct 14).
[https://doi.org/10.1038/s41598-018-24277-3]

-
Yun JM and Kang DW. (2021). Antioxidant activity and qualitative and quantitative HPLC analyses of five types of apple blossoms prepared by two different drying methods. Korean Journal of Food Preservation. 28:780-789.
[https://doi.org/10.11002/kjfp.2021.28.6.780]