
InDel과 SSR 마커를 이용한 국내 작약 유전자원의 유전적 다양성 분석
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Paeonia lactiflora Pall. exhibits diverse pharmacological activities, including anti-inflammatory and antioxidant effects. It is mainly cultivated for medicinal purposes in Korea and as an ornamental plant. However, the large and complex genome of P. lactiflora has limited the development of molecular markers, and previous studies have primarily employed RAPD, ITS, or chloroplast-based analyses. However, comparative genetic studies integrating Korean herbaceous and Dutch ornamental accessions remain limited.
Genetic diversity was analyzed in 95 P. lactiflora accessions using nine nuclear InDel markers and six selected simple sequence repeat (SSR) markers screened from 36 previously reported SSRs. Three pairs of Korean accessions (PL011–PL089, PL028–PL167, and PL107–‘Taebaek’) exhibited identical genotypes across both marker types, whereas the remaining 89 accessions, including Dutch ornamental lines, were clearly differentiated.
This study establishes a foundation for objectively evaluating genetic differences in P. lactiflora regardless of cultivation purpose or environment. These results are expected to serve as valuable resources for the efficient management of P. lactiflora genetic resources and the development of new cultivars.
Keywords:
Paeonia lactiflora, InDel Marker, Gel Electrophoresis, SSR Marker, Variety Identification서 언
작약 (Paeonia lactiflora Pall.)은 항염증, 항산화, 항암, 항우울증, 보혈, 진정, 해열, 통경, 소염, 강장, 진경, 진통 등 다양한 효능을 가지고 있어 국내에서는 주로 생약용으로 재배되고 있다 (Takagi and Harada, 1969; Ministry of Food and Drug Safety, 2008; Choi, 2009; He and Dai, 2011; Jin et al., 2016; Xiang et al., 2020; Zhang et al., 2022). 반면, 유럽, 북미, 일본 등에서는 주로 관상용 품종 개발에 집중하여 약 2,000여 품종이 등록되어 있으며 (Yang et al., 2020), 그중에서도 ‘Sarah Bernhardt’가 널리 재배되고 있다 (Kamenetsky and Dole, 2012). 약용 작약의 품종 육성은 상대적으로 더디게 진행되어 왔으나, 최근 중국에서 내습성 및 내고온성 품종인 ‘Hang Baishao’, ‘Zi Xin’ 등이 개발되었다 (Zhang et al., 2017; Wang et al., 2022). 국내에서도 품종보호등록은 이루어지지 않았지만, ‘의성’ (1993), ‘태백’ (1995), ‘사곡’ (1997), ‘거풍’ (2000), ‘대청’ (2003) 등의 뿌리 다수성 및 화훼겸용으로 선발된 계통이 직무육성 신품종 선정 심의회를 통과하여 일부 지역 보급 및 재배된 바 있다 (Rural Development Administration, 2008). 그러나 재배현장에서는 주로 재래종을 자가채종하여 사용하고 있다 (Kim et al., 2001; Choung et al., 2003; Lee et al., 2020).
작약은 자가수분 (autogamy) 시 결실률이 5% 미만으로 매우 낮아 자연 상태에서는 충매에 의한 타가수분 (xenogamy) 이 우세하다 (Zhou, 1999; Wang, 2019; Yang et al., 2020). 꽃 구조는 다수의 꽃잎과 많은 수의 수술, 그리고 3-5개의 이생 심피 (apocarpous)로 이루어져 있어 곤충 접근성이 높고, 개화 시 강한 향기를 발산하여 수분 매개체를 적극적으로 유인한다 (Peng et al., 2017). 이러한 생식·개화 특성은 개체 간 교잡 가능성을 높여 높은 이형접합도 유지와 자원 간 유전적 변이 축적에 기여한다.
작약은 재배 지역과 이용 목적이 다양할 뿐 아니라, 유전적 배경이 복잡하여 형태적 형질만으로는 정확한 유전자원 판별이 어렵다 (Pan et al., 2007; Gao et al., 2020). 특히 동일한 종 내에서도 표현형이 환경요인에 따라 변할 수 있기 때문에, 약용·관상용 자원이 병행되어 활용되는 경우 객관적인 분자 수준의 판별기법이 요구된다. 이러한 이유로 작약을 포함한 여러 약용식물에서는 분자마커 기반의 유전적 다양성 분석이 육종, 자원관리, 품종식별 등 다양한 연구에 활용되고 있다. 기존의 작약속 (Paeonia spp.)을 대상으로 한 분자마커 연구는 대부분 제한된 범위에서 수행되어 왔다. Lim 등 (2013)이 개발한 품종 판별용 RAPD (Random Amplified Polymorphic DNA) 마커는 비교적 간단한 절차로 다형성을 검출할 수 있으나, 밴드 패턴의 재현성이 낮아 실험 간 일관된 결과 확보가 어렵다 (Penner et al., 1993; Kumari and Thakur, 2014). 또한, 다수 보고된 엽록체 및 ITS (Internal Transcribed Spacer) 염기서열 기반 마커는 모계 유전 정보에 기초하므로 핵 유래 다형성 정보를 충분히 반영하지 못하며 종 간 식별 수준에 머무는 경우가 대부분이다 (Zhu et al., 2015; Gao et al., 2020; Wu et al., 2021; Lee et al., 2022). 이에 비해, 핵 유전체 기반으로 개발된 마커는 부계 및 모계 양측의 유전정보를 포함하므로 개체 간 유연관계 분석이나 유전자원의 다양성 평가에 보다 적합하다.
SSR (Simple Sequence Repeat) 마커는 짧은 반복서열의변이를 활용하여 공우성 (co-dominant) 특성과 높은 다형성을 지녀 유전자원 간의 세밀한 관계 분석과 집단구조 평가에 유용하지만 (Guo et al., 2023), 증폭 불량이나 밴드 명확성, 재현성 등의 문제로 인해 실제 활용 가능한 마커 수가 제한되는 경우가 많다. InDel (Insertion and Deletion) 마커의 경우 PCR (Polymerase chain reaction) 기반에서 삽입·결실 변이에 의한 명확한 검출이 가능하고, 비용 대비 효율성과 재현성이 높다는 장점을 지니지만, 상대적으로 다형성이 낮아 복잡한 집단 간 변이를 충분히 반영하기 어렵다 (García-Lor et al., 2012; Pacurar et al., 2012). 이러한 이유로, 단일 마커 체계만으로는 유전자원의 다양성과 구조를 포괄적으로 해석하기 어렵기 때문에, 서로 다른 특성과 변이 유형을 지닌 마커를 병행하여 활용하는 것이 바람직하다. 실제로 표고버섯 [Lentinula edodes (Berk.) Pegler]을 대상으로 한 연구에서는 InDel과 SSR 마커를 함께 적용함으로써 단일 마커 분석보다 더 높은 다형성과 집단 간 구분력을 확보하였으며, 이를 통해 유전적 구조를 보다 명확히 규명할 수 있었다 (Xiang et al., 2016). 또한, 참깨 (Sesamum indicum L.)를 대상으로 한 연구에서도 InDel 마커를 단독으로 사용하는 것보다 SSR 마커를 함께 적용했을 때 상호보완적인 유전형 해석이 가능하여, 개량된 참깨 품종이 육종 과정에서 발생한 유전적 부동이나 선택의 영향으로 재래종에 비해 유전적 기반이 더 좁으며 개량품종과 재래종뿐만 아니라 서로 다른 시기에 개발된 품종들 간에도 유전적 분화가 나타났음을 확인하였다 (Wu et al., 2014). 이 외에도 해바라기 (Helianthus annuus L.), 고추 (Capsicum annuum L.), 고추속 (Capsicum spp.), 양배추 (Brassica oleracea var. capitata L.) 등의 작물에서 InDel과 SSR 마커를 함께 분석에 활용한 바 있다 (Talia et al., 2010; Lv et al., 2014; Tan et al., 2015; Zhang et al., 2016). 이러한 마커 병행 활용은 각 마커의 한계를 상호 보완하여 보다 안정적이고 정밀한 유전적 다양성 분석을 가능하게 할 것으로 판단된다 (García-Lor et al., 2012).
국내 약용 작약의 효율적인 육종과 자원 활용을 위해서는 재래종을 포함한 유전자원 수준의 유전적 다양성을 명확히 파악할 필요가 있다. 유전자원은 작물 육종의 근간으로서, 품종 개발에 필요한 유전적 변이를 제공한다. 농촌진흥청 국립농업과학원에서는 농업유전자원의 효과적인 보존, 관리, 활용을 위해 IT 번호를 부여하고 서비스 시스템을 운영하여 연구자들에게 ‘자원검색’, ‘자원분양’, ‘자원기탁’, ‘정보공개’ 등의 서비스를 제공하고 있다. 전 세계적으로 다양한 작물 유전자원이 수집·보존되고 있으나, 자원의 규모가 커질수록 중복 보존과 평가의 비효율성이 문제가 되고 있다 (Li et al., 2004). 따라서 유전자원의 유전적 다양성 분석은 육종 소재의 선발, 교배조합 설정, 그리고 품종 간 유전적 관계 규명을 위한 필수 과정으로 인식되고 있다.
Jeong 등 (2025)은 InDel 마커를 개발해 ‘의성’, ‘태백’, ‘사곡’, ‘거풍’, ‘대청’을 구분한 바 있으나, 실제 재배지에서 수집된 폭넓은 자원을 기반으로 한 분석은 아직 제한적이다. 이에 본 연구는 기존 연구의 범위를 확장하여, 국내 여러 지역에서 재배 중인 재래종과 품종을 포함하고, 나아가 유럽의 네덜란드에서 도입된 관상용 자원을 함께 비교 분석하였다. 네덜란드는 세계적인 화훼산업 중심지로서 재배환경과 육종배경이 한국과 상이하며, 이러한 이질적 배경의 자원을 포함함으로써 재배 목적과 육종계통에 따른 유전적 차이를 다층적으로 평가할 수 있다. 또한, 기존의 SSR 마커 관련 연구들은 대부분 국외 관상용 품종을 대상으로 수행된 바 있다. Ji 등 (2014)은 핵 유전체 기반 SSR 15종을, Gilmore 등 (2013)은 Illumina 플랫폼을 이용해 21종의 SSR 마커를 개발하였으며, 모두 관상용 및 절화용 작약 자원을 중심으로 보고되었다. 이러한 점에서 본 연구는 국가에서 관리되는 IT 자원을 포함하여, 서로 다른 용도와 육종 배경의 작약 유전자원을 통합적으로 비교·평가했다는 데 의의가 있다.
본 연구에서는 국내에서 수집된 총 95개의 작약 유전자원을 대상으로, 핵 기반 9개의 InDel 마커와 6개의 SSR 마커를 병용하여 유전적 다양성과 집단구조를 분석하였다. InDel 마커의 높은 재현성과 SSR 마커의 높은 분해능을 결합함으로써, 기존의 단일 마커 체계가 지닌 한계를 보완하고 작약 자원의 유전적 기반을 입체적으로 해석하고자 하였다. 이를 통해 용도가 다른 작약 자원을 통합적으로 조명하고, 향후 작약 육종과 자원 관리에서 활용 가능한 실질적 유전정보를 제공하는 것을 목표로 하였다.
최근 작약은 약리적 효능뿐 아니라 건강기능식품 시장 확대에 따라 수요가 꾸준히 증가하고 있으며, 2023년 기준 국내 생산량은 1,987톤에 이르고 있다 (Ministry of Agriculture, Food and Rural Affairs, 2024). 이러한 산업적 성장과 함께, 재배 환경 및 자원의 다양성에 기초한 분자수준의 유전정보 확보는 향후 작약 자원의 품종개량, 품질 표준화, 국내외 시장 경쟁력 강화를 위한 필수적인 기반이 될 것으로 기대된다.
재료 및 방법
1. 시험 재료 및 genomic DNA 추출
국립원예특작과학원 인삼특작부 특용작물육종과 시험포장 (36.9433°N, 127.7497°E)에서 보존하고 있던 국·내외 작약 유전자원 중 형태적 다양성, 용도, 수집 지역 등의 대표성을 고려하여 사전에 선발한 95개의 유전자원으로부터 신초를 채취하여 동결 건조시킨 뒤, 막자사발에 액체질소를 넣고 분말화하였다. 하였다. 보관된 식물 시료로부터 gDNA (genomic DNA)는 GeneAll Biotechnology (Seoul, Korea)의 GeneAll® Exgene™ Plant SV mini kit를 이용하여 제조사의 매뉴얼에 따라 추출하였다. 추출된 DNA의 농도와 순도는 NanoDrop One 분광광도계 (Thermo Scientific, Waltham, MA, USA)를 이용하여 제조사의 매뉴얼에 따라 측정하였다. DNA의 농도 및 순도는 NanoDrop One 분광광도계 (Thermo Scientific, Waltham, MA, USA)를 이용하여 측정하였다 (Table 1).
2. InDel 마커 분석
유전적 다양성 분석을 위해 Jeong 등 (2025)이 개발한 InDel 마커 9개를 이용하였다. 해당 마커는 ‘의성’, ‘태백’, ‘사곡’, ‘대청’, ‘거풍’ 간 삽입·결실에 따른 서열 길이 차이를 이용해 PCR 및 아가로스 겔 전기영동만으로도 이들의 유전자형을 구분할 수 있다. 각 마커의 프라이머 서열 및 증폭 산물의 크기 범위는 선행 논문에 기술된 방법을 따랐으며, 선정된 InDel 좌위의 실제 변이 존재 여부와 프라이머의 증폭 특이성을 검증하기 위해, PCR은 Bio-Rad사의 C1000 Touch Thermal Cycler (Hercules, CA, USA)를 사용하여 수행하였다. 총 반응 부피는 20 μL로 구성하였으며, 반응액에는 주형 DNA 2 μL (20 ng/μL), Exel TB 2× Taq Premix with dye (Inclone™ Exel, Inclonebiotech Co., Korea) 10 μL, forward 프라이머와 re ve rse 프라이머 각 2 μL (5 μM), 그리고 멸균 증류수를 첨가하였다. PCR 조건은 95℃에서 5분간 초기 변성을 진행한 후, 95℃ 30초, 각 마커의 annealing temperature에서 40초, 72℃ 30초의 과정을 38회 반복하였다. 마지막으로 72℃에서 5분간 최종 신장을 수행하였다. 증폭된 산물은 −20℃에서 보관하였다. InDel 마커의 증폭 패턴과 peak의 정확성을 검증하기 위해 5개 시료를 선별하여 추가 PCR을 실시하였고, 생성된 산물은 Fragment Analyzer™ 시스템 (Advanced Analytical Technologies, Ames, IA, USA)을 이용하여 분석하였다. 분석은 제조사 매뉴얼에 따라 수행하였으며, PCR 산물은 TE buffe r와 분석용 시약 (dsDNA 905 Gel, dsDNA 930 Inlet Buffer, intercalating dye, size marker, Capillary Conditioning Solution 등)을 혼합한 뒤 96-well plate에 로딩하여 전기영동하였다. DNA 단편은 35-400 bp 범위의 DNA ladder (Agilent Technologies, Santa Clara, CA, USA)를 기준으로 자동 검출되었으며, PROSize™ 소프트웨어 (version 3.0; SoftGenetics LLC, State College, PA, USA)를 사용하여 밴드 크기를 산출하였다.
3. SSR 마커 선발
유전적 다양성 분석에 사용할 다형성 SSR 마커 선발을 위해, Gilmore 등 (2013) 및 Ji 등 (2014)이 개발한 SSR 마커 36종을 사용하였다. 각 마커는 작약 자원 중 ‘태백’을 대상으로 해당 논문에서 제시한 PCR 및 전기영동 조건에 따라 예비 검증을 수행하였으며, 명확하고 단일한 밴드 패턴을 형성하는 마커 32종을 1차로 선별하였다. 이후 선별한 SSR 마커를 활용하여 앞서 수행한 InDel 마커 분석 결과 유연관계가 먼 것으로 확인된 작약 자원 6점 (PL-014, PL-016, PL-057, PL-151, PL-157, PL-190)을 대상으로 PCR 반응 용액 15 μL에 DNA (10 ng), M13-tailed forward 프라이머 (10 μM) 0.06 μL, reverse 프라이머 (10 μM) 0.3 μL와 6-FAM labeled M13 프라이머 (5’-TGTAAAACGACGGCCAGT-3’) 0.3 μL, 2X Taq mix (Dongshengbio Co., Guangdong, China) 7.5 μL 및 멸균 증류수를 더해 반응 부피를 맞춘 뒤, ABI 2720 thermal cycler (Applied Biosystems, MA, USA)를 이용하여 PCR을 수행하였다. PCR 반응은 95℃에서 5분간 열변성을 실시한 후, 95℃ 30초, 각각의 annealing temperature에서 30초, 72℃ 30초 조건의 18사이클과 94℃ 30초, 각각의 annealing temperature에서 30초, 72℃ 30초 조건의 23사이클을 연속하여 수행하였으며, 마지막으로 72℃에서 30분간 최종신장을 진행하였다. PCR 증폭 산물은 1.2% 아가로스 젤에서 전기영동을 통해 증폭 여부를 확인한 후, 희석한 0.2 μL의 PCR 증폭산물을 9.8 μL의 Hi-Di formamide (Applied Biosystems, MA, USA), 0.2 μL의 GeneScanTM 500 LIZ® size standard (Applied Biosystems, MA, USA)와 혼합하였다. 혼합물을 95℃에서 5분간 변성시킨 후 4℃에서 냉각하고, 50 ㎝ 모세관이 장착된 ABI 3730 DNA analyzer (Applied Biosystems, MA, USA) 상에서 모세관 전기영동을 통해 증폭된 DNA 절편들을 분리하였다. 대립유전자들의 크기는 GeneMapper 소프트웨어 (ver. 4.0; Applied Biosystems, MA, USA)를 사용하여 결정하였다. 이후 PCR에는 M13 tail 프라이머 시스템을 적용하여 다형성과 peak 패턴을 확인하였다. 이 시스템은 forward 프라이머의 5′ 말단에 M13 서열 (5’-TGTAAAACGACGGCCAGT-3’)을 부착하고, 형광 표지된 공통 M13 프라이머 (FAM, NED, PET 등)를 함께 사용하는 PCR을 수행하는 3-primer 방식이다. 이를 통해 형광 프라이머의 일괄 사용이 가능해져 분석 비용을 절감할 수 있으며, capillary 전기영동 분석에도 적합하다 (Boutin-Ganache et al., 2001). 검증 기준은 (i) 기대 증폭 크기 범위 내에서 명확한 단일 peak가 형성될 것, (ii) peak 분리 또는 다중 peak가 나타나지 않을 것, (iii) 비특이적 신호가 주요 peak 판독을 방해하지 않을 것 등으로 최종적으로, 6개의 자원에서 명확한 증폭과 예측이 가능한 다형성 패턴을 보인 6종의 SSR 마커를 기존의 2-primer PCR 방식으로 증폭하여 활용하였다 (Table 3).
4. SSR 마커 분석
SSR 분석을 위한 PCR은 주형 DNA를 멸균 증류수에 10 ng/μL 농도로 희석한 후, 반응액 총량 15 μL 조건에서 수행하였다. 반응 혼합물은 10–20 ng의 DNA, 10 μM 농도의 forward 및 reverse 프라이머 각 0.5 μL, 2X Taq premix (Dongshengbio Co., Guangdong, China)를 포함하였으며, ABI 2720 Thermal Cycler (Applied Biosystems, MA, USA)를 사용하였다. PCR 반응은 초기 변성 95℃에서 5분, 35회 반복 사이클 (95℃ 30초 – 각각의 annealing temperature 30초 – 72℃ 30초), 최종 신장 단계는 72℃에서 30분간 수행하였다. PCR 증폭 산물의 증폭 여부는 1.2% (w/v) 아가로스 젤 전기영동을 통해 1차 확인하였다. 이후, 분석용 형광 표지 프라이머인 FAM (6-carboxyfluorescein), NED, PET을 사용하여 PCR을 수행하였으며, 그중 3개의 마커 산물을 희석하여 혼합하였다. 각 조합에서 사용된 형광 표지는 프라이머 염기 서열 앞에 표기하였다 (Table 2). 혼합된 0.1 μL의 PCR 산물을 9.9 μL의 Hi-Di™ formamide (Applied Biosystems, MA, USA) 및 0.1 μL의 GeneScan™ 500 LIZ® size standard와 혼합한 뒤, 95℃에서 5분간 변성시킨 후 4℃에서 3분간 냉각하였다. 변성된 시료는 ABI 3730 DNA Analyzer (Applied Biosystems, USA)의 50 cm 모세관을 이용한 모세관 전기영동으로 분리하였고, 대립유전자의 크기 판독은 GeneMapper 소프트웨어 (ver. 4.0; Applied Biosystems, MA, USA)를 사용하여 수행하였다. SSR 산물의 유전형 판정은 모세관 전기영동에서 얻은 raw fragment size와 peak height를 기준으로 수행하였다. Table 3에서 제시한 각 마커의 amplicon size 범위 내에서 검출된 peak 중 신호 강도가 뚜렷한 주요 peak만을 유효 allele로 인정하였으며, stutter peak나 낮은 신호의 minor peak는 비특이적 산물로 간주하여 제외하였다. 범위 내 peak는 ±1–2 bp 허용오차를 기준으로 인접한 크기군 (size cluster)으로 묶어 allele을 정의하였다. 형광 PCR 및 절편 분석 등은 장비 부재로 인해 ㈜바이오메딕 생명과학연구소 (Life Sciences Research Institute, Biomedic Co., Ltd.)에 의뢰하여 진행하였다.
5. 유전 다양성 및 유연관계 분석
PowerMarker ver. 3.25 (Liu and Muse, 2005)를 통해, 자원 간 유전적 관계를 시각화하기 위한 각 개체 간 유전적 거리인 Shared Allele Distance를 기준으로 공유 대립유전자 거리 (Shared Allele Distance) 방식으로, 주요 유전학적 매개변수인 주요 대립유전자 빈도 (major allele frequency, MAF), 대립유전자 수 (number of alleles, NA), 기대이형접합도 (expected heterozygosity, He), 관찰이형접합도 (observed heterozygosity, Ho), 다형성 지표인 PIC (polymorphism information content)을 산출하였으며, MEGA 소프트웨어 (ver. 5.2; Arizona State University, Tempe, AZ, USA)를 활용하여 UPGMA (Unweighted Pair Group Method with Arithmetic Mean) 방법으로 계통수를 작성하였다 (Tamura et al., 2007).
결과 및 고찰
1. InDel 마커 다형성 평가
선행연구에서 개발된 InDel 마커의 적용과 유전적 다양성을 분석하기 위해, 총 95점의 작약 유전자원을 대상으로 PCR을 수행하였으며, 정량적인 분석은 Fragment Analyzer™를 사용하여 진행하였다 (Fig. 1). 기대이형접합도 (He)는 전체 집단 내에서 임의로 추출된 두 개체가 서로 다른 대립유전자를 가질 확률로, 유전변이의 폭을 나타내는 지표이다 (Nei, 1973). 본 연구에서 선발·적용한 InDel 마커의 기대이형접합도 (He)는 0.25에서 0.50 사이로 평균 0.40을 보였으며, 이 중 PLID8-2K 마커가 0.50으로 가장 높은 수준을 나타냈다 (Table 4). 이는 오이 (Cucumis sativus L.) 육성계통에서 보고된 InDel 마커의 기대이형접합도 (He) 0.22–0.60, 평균 0.40과 비슷한 수준으로 (Adedze et al., 2021), 작약과 같은 유전적으로 복잡한 종에서도 InDel 마커를 다형성 마커로 활용할 수 있음을 시사한다.

Fragment analysis of the InDel marker PLID5-2K across 60 samples (subset).Lanes 1-30 correspond to the following samples: ES, TB, , DC, SG, GP, PL001, PL002, PL003, PL004, PL007, PL008, PL009, PL010, PL011, PL012, PL013, PL014, PL015, PL016, PL017, PL018, PL019, PL020, PL021, PL022, PL023, PL024, PL025, PL026 and PL027. Lanes 31-60 correspond to PL028, PL029, PL030, PL031, PL032, PL033, PL034, PL035, PL036, PL037, PL038, PL039, PL040, PL041, PL042, PL043, PL044, PL045, PL046, PL047, PL048, PL049, PL050, PL051, PL052, PL053, PL054, PL055, PL056 and PL057. Lane M: 35-400 bp DNA Ladder (Agilent Technologies, Santa Clara, CA, USA).
관찰이형접합도 (Ho)는 개체 단위에서 두 대립유전자가 서로 다를 확률을 의미하며, 개체 수준의 유전적 다양성을 반영한다 (Nei and Roychoudhury, 1974). 본 연구에서는 0.27에서 0.97까지 다양하게 나타났으며 평균 0.57을 나타냈고, PLID16-2 마커가 0.97로 가장 높은 값을 보여 다양한 대립유전자 조합의 구분에 유리한 마커로 확인되었다 (Table 4). 이는 이형접합성이 높은 작약과 같은 종의 유전형 분석에 특히 적합한 특성이다.
PIC는 각 마커가 유전형 구분에 제공하는 정보의 양을 수치화한 값으로, 마커의 유용성을 평가하는 지표이다 (Botstein et al., 1980). PIC 값은 각 좌위에서 관찰된 대립유전자의 빈도를 기반으로 산출하였다. 대립유전자 빈도를 계산한 뒤, 모든 대립유전자 빈도의 제곱합을 구하고, 이를 1에서 차감하여 PIC 값을 얻는 표준식을 사용하였다. 이러한 방식은 각 마커가 제공하는 유전형 구분력의 크기를 정량적으로 평가하는 데 활용된다.
본 연구에서의 PIC 값은 0.22에서 0.37의 범위로 평균 0.32였으며, PLID1-5, PLID8-2K, PLID16-2, PLID18-2 마커가 가장 높은 0.37의 값을 기록하였다 (Table 4). 이는 Ji 등 (2014)이 보고한 작약 SSR 마커의 평균 PIC 값 0.6보다는 낮았으나 Hechanova 등 (2021)이 보고한 벼 InDel 마커의 PIC 값 범위 (0.080–0.461)와 비슷한 수준이었다 (Ji et al., 2014; Hechanova et al., 2021). 일반적으로 InDel 마커는 반복 길이가 짧고 돌연변이율이 낮아 SSR보다 다형성이 낮은 것으로 알려져 있으며 (Pacurar et al., 2012), 본 연구의 결과도 이와 일치하는 경향을 보였다. 이러한 이유로 Fig. 2에 제시된 유연관계 분석 결과에서도 일부 자원 간 구분이 명확하지 않았으며, 다수의 자원이 동일 그룹에 속하는 양상을 보였다 (Fig. 2). 이는 사용된 InDel 마커의 다형성이 상대적으로 낮기 때문으로 판단된다. 그럼에도 불구하고 InDel 마커는 특정 자원의 유전형 구분이나 집단 간 유전적 다양성 평가에 있어 충분히 활용 가능한 수준의 다형성을 제공하였다. 예를 들어, SSR 마커만을 이용한 군집도에서는 구분되지 않았던 PL140과 PL158, PL200과 PL209, PL003과 PL093, PL030과 PL088, PL142와 PL119와 PL138, PL102와 PL120, PL135와 ‘거풍’과 PL061이 InDel 마커만을 이용한 군집도에서는 구분되는 것으로 확인되었다 (Fig. 2 and 3). PLID1-5, PLID8-2K, PLID16-2, PLID18-2와 같이 비교적 높은 PIC 값을 나타낸 마커는 향후 작약 유전자원의 핵심 집단 설정 및 품종 판별에 유용할 것으로 기대된다.

Phylogenetic analysis of herbaceous peony germplasm analyzed using 9 InDel markers.Blue labeled samples indicate accessions that were not distinguishable when using only InDel markers.

Preliminary screening of 36 SSR markers.Lanes 1–24 correspond to the following SSR markers: Sy1, Sy2, Sy3, Sy4, Sy5, Sy6, Sy7, Sy8, Sy9, Sy10, Sy11, Sy12, Sy13, Sy14, Sy15, Pdel06, Pdel07, Pdel29b, AT8051F, AG8073, ATG9706, PCA1, P06, and P05. Lanes 25–36 correspond to Pae03, Pae06, Pae07, Pae12, Pae25, Pae28, Pae43, Pae65, Pae100, Pae102, Pae110, and Pae115. The Four markers (Sy5, Pdel06, Pdel07, and P06) were excluded at this stage due to inconsistent or absent amplification. Lane M: 100 bp DNA ladder (Dongshengbio Co., Guangdong, China). Arrowheads indicate six SSR markers (Sy2, Sy7, Sy9, Pae100, Pae 03 and Pae65) showing clear and reproducible polymorphisms, which were selected for further genetic diversity analysis.
2. SSR 마커 선발
유전적 다양성 분석용 SSR 마커를 선발하기 위해 Gilmore 등 (2013)과 Ji 등 (2014)이 보고한 36종의 SSR 프라이머를 ‘태백’을 대상으로 스크리닝하여 전기영동 밴드의 증폭 상태를 확인하여 밴드가 형성되지 않거나 증폭이 불안정한 마커 4종 (Sy5, Pdel06, Pdel07, P06)을 제외하고 1차적으로 32종을 선별하였다 (Fig. 3). 이후 앞서 InDel 마커 분석에서 유연관계가 먼 것으로 확인된 작약 자원 6점 (PL-014, PL-016, PL-057, PL-151, PL-157, PL-190)을 대상으로 선별된 프라이머를 M13-tail 시스템을 적용한 PCR 후 GeneScan Analysis를 통해 다형성 peak 패턴을 확인하였으며 (Fig. 4), 이 가운데 뚜렷한 증폭·재현성을 보인 6종의 SSR 프라이머를 최종 선정하였다 (Table 3).

Genotyping of six genetically distant herbaceous peony germplasm using selected SY9 markers with M13-tailed primer system.Fluorescent-labeled alleles were separated by capillary electrophoresis and analyzed with GeneMapper software. From top to bottom: PL014, PL016, PL057, PL151, and PL157, respectively.
3. SSR 마커 다형성 평가
최종 선발된 다형성 SSR 마커의 효율성을 평가하기 위해, 선발된 6쌍의 프라이머를 작약 유전자원 95점에 적용하였다. 전체 자원에서 기대이형접합도 (He)는 0.41-0.80으로 평균 0.64였으며, 관찰이형접합도 (Ho)는 0.29-0.78로 평균 0.59로 나타났다 (Table 5). PIC 값은 0.36-0.78 범위였으며, 평균 0.60으로 분석되었다. 특히, 6개 마커 중 3개에서 PIC 값이 0.7 이상으로 매우 우수한 다형성을 보이는 것으로 판단되며, 이는 향후 작약 자원의 식별 및 유전자원 관리에 유용할 것으로 평가된다 (Botstein et al., 1980; Anderson et al., 1993). 한편, 6개 SSR 마커 중 일부에서는 결측값이 발생하였으며, 특히 Pae100 마커는 전체 95개 자원 중 55개 (Availability = 0.57)에서만 유효한 데이터를 확보하였다. 그럼에도 불구하고 본 마커는 기대이형접합도 (He = 0.78) 및 PIC 값 (0.75)이 높아, 정보력 높은 유전자형 분리 마커로서의 활용 가능성을 지닌다고 판단된다. SSR 마커를 이용한 유연관계 분석에서는 전반적으로 InDel 분석보다 다형성이 높고 분지 구조가 세분화되었으나, 여전히 많은 자원이 InDel 분석 결과와 마찬가지로 동일 그룹으로 묶이는 경향을 보였으며, 이는 마커 수의 한계로 인한 분해능 (resolution) 부족에 기인한 것으로 판단된다 (Fig. 5). InDel 마커를 이용한 군집도에서는 PL107과 ‘태 백’만 동일한 유전자형으로 나타난 반면, SSR 마커 분석에서는 PL094 역시 동일한 유전자형으로 포함되었다. 향후 분석 에서는 결측률을 고려한 보완 분석이나 마커 대체가 요구될 수 있다.

UPGMA cluster dendrogram of herbaceous peony germplasm analyzed using 6 SSR markers.Blue labeled samples indicate accessions that were not distinguishable when using only SSR markers.
InDel 마커와 비교하면, 앞서 선발한 9개 InDel 마커의 평균 기대이형접합도 (He)는 0.40, PIC는 0.32로, SSR 마커 (He = 0.64, PIC = 0.60)에 비해 다형성 및 유전적 다양성 수준이 낮았다 (Table 4 and 5). 이는 InDel이 주로 biallelic 변이를 반영하기 때문으로, 일반적으로 다대립형 (multi-allelic)인 SSR 보다 변별력이 떨어진다는 선행 보고와 일치한다 (Pacurar et al., 2012). 그럼에도 불구하고 InDel 마커인 PLID1-5 (He = 0.48, PIC = 0.37), PLID18-2 (He= 0.49, PIC = 0.37), 반영하기 때문으로, 일반적으로 다대립형 (multi-allelic)인 SSR 보다 변별력이 떨어진다는 선행 보고와 일치한다 (Pacurar et al., 2012). 그럼에도 불구하고 InDel 마커인 PLID1-5 (He = 0.48, PIC = 0.37), PLID18-2 (He = 0.49, PIC = 0.37), PLID16-2 (He = 0.50, PIC = 0.37), PLID8-2K (He = 0.50, PIC = 0.37)는 SSR 마커인 Sy2 (He = 0.41, PIC = 0.36)보다 높은 정보력을 보였다. Zhu 등 (2015)은 Poncirus 자원에서 일부 InDel이 SSR보다 PIC 값이 높았다고 보고하였으며, 이는 표적 유전자나 종 특성에 따라 InDel이 우수한 다형성을 제공할 수 있음을 시사한다. 또한, SSR 마커 분석에서 관찰이형접합도 (Ho)가 기대이형접합도 (He)보다 낮은 경향은 95점의 선발된 유전자원 중 일부가 동일 계통에서 유래되었거나, 형질 중심으로 선발된 자원이 포함되어 집단 내 유전적 유사성이 높았기 때문으로 해석된다. 이는 자원의 구성과 선발 기준이 유전 구조에 영향을 줄 수 있음을 의미한다.
본 연구 결과는 InDel 마커도 적절한 좌위를 선정할 경우 일부 SSR에 준하는 수준의 변별력을 가질 수 있음을 확인하였다. InDel은 젤 전기영동만으로 간편하게 스코어링이 가능하여 저비용·고효율 분석이 가능하고, 현장 적용에도 유리하다는 점에서 SSR 대비 실용성이 높다. 반면 SSR은 형광 표지 프라이머 및 모세관 전기영동 기반의 분석이 필요해, 장비·비용 면에서 제약이 따를 수 있다. 따라서 InDel–SSR의 병행 활용은 각각의 장단점을 보완하며, 유전자원 다양성 평가 및 자원 선별의 정확도를 높이는 데 기여할 수 있을 것으로 생각된다.
4. InDel과 SSR 마커 활용 유연관계 분석
InDel과 SSR 마커 유전자형 데이터를 하나의 데이터셋으로 통합한 것을 UPGMA 방법으로 유연관계를 분석한 결과는 Fig. 6에 나타내었다. 두 마커를 모두 적용한 군집도에서 동일 유전자형으로 확인된 자원쌍 (PL011-PL089, PL028과 PL167, PL107-‘태백’)은 실제로 표현형으로도 동일하였다. PL011과 PL089는 연한 분홍색의 홑꽃형 (single type)을 나타냈고, PL028과 PL167은 진한 분홍색의 홑꽃형이었다. 또한 PL107과 ‘태백’은 분홍색, 백색, 분홍색으로 이어지는 화색을 보이고 겹꽃형 (double type)을 나타내어 개화 형태와 화색 모두에서 차이가 없었다 (Fig. 6 and 7). 이를 통해 InDel과 SSR 마커를 병행 활용하는 것이 유효함을 확인할 수 있었다. 네덜란드 관상용 자원을 포함한 나머지 89개 자원은 모두 서로 다른 개별 가지 (branch)에 독립적으로 위치하였으며 유전거리 0인 조합이 검출되지 않아, 국내 약용자원과 네덜란드 도입 자원 간 뚜렷한 유전적 분화를 확인할 수 있었다. 이러한 결과는 재배 목적과 환경의 차이가 유전적 다양성에도 반영된다는 점을 시사하며, 향후 작약의 교배 육종에서 유전적 기반 정보를 제공할 수 있을 것으로 판단된다. 한편, 밀에서 SSR 마커를 활용해 핵심집단을 설정하고 유전적 다양성을 효율적으로 평가한 사례가 보고된 바 있으며 (Min et al., 2021), 본 연구의 결과를 통해 작약 자원의 핵심집단 선발, 체계적 자원 관리를 위한 기반 자료로 활용될 수 있을 것으로 판단된다.
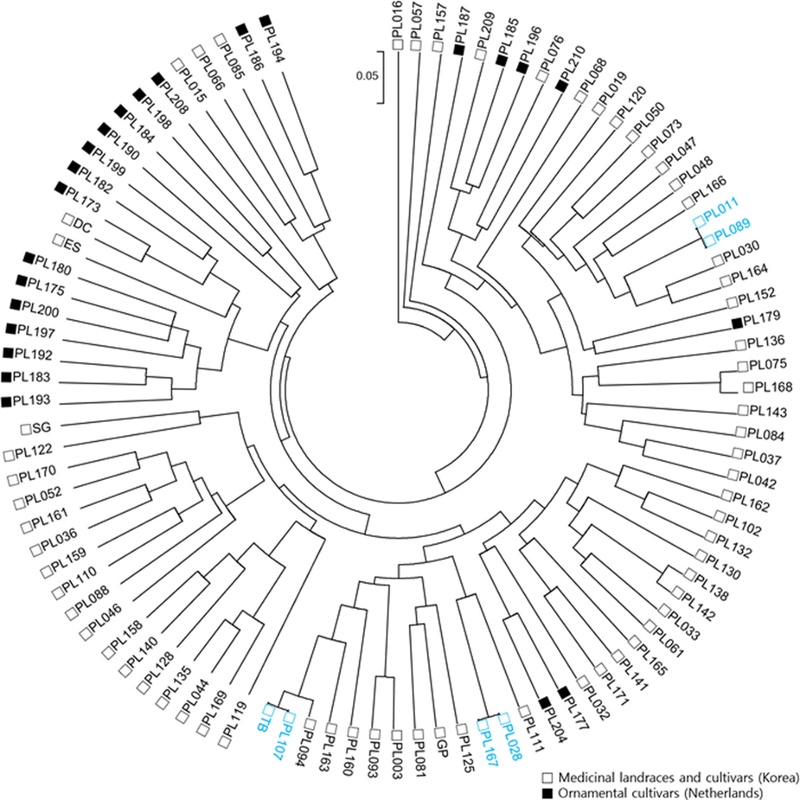
UPGMA cluster dendrogram of herbaceous peony germplasm analyzed using 9 InDel and 6 SSR markers.Blue labeled samples indicate accessions that were distinguishable only when both InDel and SSR markers were combined. Three pairs of samples (PL011-PL089, PL028-PL167, and PL107-‘Taebaek’) were identified as having identical genotypes in the dendrogram constructed using both InDel and SSR markers.

Comparison of floral morphology among herbaceous peony germplasm identified as genetically identical based on InDel and SSR marker genotyping.A–B: PL011 and PL089; C–D: PL028 and PL167; E–F: PL107 and ‘Taebaek’.
Wu 등 (2014)은 참깨 자원 130점에 대한 연구에서 SSR이 평균 allele 수·PIC 값이 높지만 InDel도 유사한 수준을 보여 두 마커 조합이 집단구조 해석에 상호 보완적임을 강조하였으며 본 연구에서도 통합 분석을 통한 정확도 있는 판별이 가능하게 되었다. InDel과 SSR 마커 결과를 통합하여 UPGMA 분석한 결과를 통해 작약 유전자원 간 유전적 다양성을 시각화했으며, 자원 관리, 핵심집단 구축 및 교배 설계에 활용될 기초자료를 제공할 수 있을 것으로 보인다. 특히 PL061이나 PL208 같은 자원은 다른 자원들에 비해 상대적으로 유연관계가 멀기 때문에 이러한 자원과의 교배를 통해 유전적 폭을 넓히는 육종 전략 수립이 필요할 것으로 사료된다.
Acknowledgments
본 연구는 농촌진흥청 연구 사업 (사업번호: PJ01732205)의 지원에 의해 이루어진 결과로 이에 감사드립니다.
References
-
Adedze YMN, Lu X, Xia Y, Sun Q, Nchongboh CG, Alam MA, Menghua L, Yang X, Zhang W, Deng Z, Li W and Si L. (2021). Agarose-resolvable InDel markers based on whole genome re-sequencing in cucumber. Scientific Reports. 11:3872.
[https://doi.org/10.1038/s41598-021-83313-x]

-
Anderson JA, Churchil GA, Autrique JE, Tanksley SD and Sorrells ME. (1993). Optimizing parental selection for genetic linkage maps. Genome. 36:181-186.
[https://doi.org/10.1139/g93-024]

-
Boutin-Ganache I, Raposo M, Raymond M and Deschepper CF. (2001). M13-tailed primers improve the readability and usability of microsatellite analyses performed with two different allele-sizing methods. Biotechniques. 31:24-28.
[https://doi.org/10.2144/01311bm02]

- Botstein D, White RL, Skolnick M and Davis RW. (1980). Construction of a genetic linkage map in man using restriction fragment length polymorphisms. American Journal of Human Genetics. 32:314-331.
- Choi SG. (2009). Herbal medicinal crop production: Special Part. Shinkwang Press, Seoul, Republic of Korea, p.186.
- Choung MG, An YN, Kang KH, Cho YS and Kim JH. (2003). Comparison on the Extract Content by Different Processing Method in Peony(Paeonia lactiflora Pall.) Root. Korean Journal of Medicinal Crop Science. 11:201-206.
-
Gao C, Wang Q, Ying Z, Ge Y and Cheng R. (2020). Molecular structure and phylogenetic analysis of complete chloroplast genomes of medicinal species Paeonia lactiflora from Zhejiang Province. Mitochondrial DNA Part B. 5:1077-1078.
[https://doi.org/10.1080/23802359.2020.1721372]

-
García-Lor A, Luro F, Navarro L and Ollitrault P. (2012). Comparative use of InDel and SSR markers in deciphering the interspecific structure of cultivated citrus genetic diversity: A perspective for genetic association studies. Molecular Genetics and Genomics. 287:77-94.
[https://doi.org/10.1007/s00438-011-0658-4]

-
Gilmore B, Bassil N, Nyberg A, Knaus B, Smith D, Barney DL and Hummer K. (2013). Microsatellite marker development in peony using next generation sequencing. Journal of the American Society for Horticultural Science. 138:64-74.
[https://doi.org/10.21273/JASHS.138.1.64]

-
Guo Q, Xue X, Hu X,, He Y, Wei S, Liu S, Zhao G, Wang Z and Hou X. (2023). Genetic Diversity and Population Structure Analysis of Tree Peony(Paeonia Section Moutan DC.) Germplasm Using Sixteen Functional SSR Markers. Forests. 14:1945. https://www.mdpi.com/1999-4907/14/10/1945, (cited by 2025 Nov 30).
[https://doi.org/10.3390/f14101945]

-
Hechanova SL, Bhattara, K, Simon EV, Clave G, Karunarathne P, Ahn E K Li CP, Lee JS, Kohli A, N. Ruaraidh SH, Jose EH, Glenn BG, Ksirod KJ, An G and Kim SR. (2021). Development of a genome-wide InDel marker set for allele discrimination between rice(Oryza sativa) and the other seven AA-genome Oryza species. Scientific Reports. 11:8962.
[https://doi.org/10.1038/s41598-021-88533-9]

-
He DY and Dai SM. (2011). Anti-inflammatory and immunomodulatory effects of Paeonia lactiflora Pall., a traditional Chinese herbal medicine. Frontiers in Pharmacology. 2:10. https://www.frontiersin.org/journals/pharmacology/articles/10.3389/fphar.2011.00010/full, (cited by 2025 Nov 30).
[https://doi.org/10.3389/fphar.2011.00010]

-
Jeong JT, Kim LK, Lee JH, Kim EH, Jang SY, Kim M, Oh TY, Lee MS, Koo SC, Hur M, Park WT, Kim HW, Park JW, Ahn WS and Lee Y. (2025). Development of InDel Markers for the Identification of Herbaceous Peony Varieties. Korean Journal of Medicinal Crop Science. 33:308-317.
[https://doi.org/10.7783/KJMCS.2025.33.5.308]

-
Ji LJ, Teixeira da Silva JA, Zhang JJ, Tang ZJ and Yu XN. (2014). Development and application of 15 novel polymorphic microsatellite markers for sect. Paeonia(Paeonia L.). Biochemical Systematics and Ecology. 54:257-266.
[https://doi.org/10.1016/j.bse.2014.02.009]

-
Jin ZL, Gao N, Xu W, Xu P, Li SQ, Zheng YY and Xue M. (2016). Receptor and transporter binding and activity profiles of albiflorin extracted from Radix Paeoniae Alba. Scientific Reports. 6:33793.
[https://doi.org/10.1038/srep33793]

- Kamenetsky R and Dole JM. (2012). Herbaceous peony(Paeonia): genetics, physiology and cut flower production. Floriculture and Ornamental Biotechnology. 6:62-77.
- Kim JH, Park SD, Kim JC and Park JH. (2001). Growth characteristics and paeoniflorin content in introduced peony varieties. Korean Journal of Medicinal Crop Science. 9:139-145.
-
Kumari M and Thakur A. (2014). Randomly amplified polymorphic DNA - a brief review. American Journal of Animal and Veterinary Sciences. 9:6-13.
[https://doi.org/10.3844/ajavsp.2014.6.13]

-
Lee ES, An TJ, Park WT, Jeong JT, Lee YJ, Hur M, Han JW, Han SH, Kim YG, Park CG, Chang JK and Kim YI. (2020). A trend analysis of the cultivation status of medicinal crop farmers in Korea. Korean Journal of Agricultural Science. 47:139-161.
[https://doi.org/10.7744/kjoas.2020007]

-
Lee, MS, Jeong HJ, Park SH, Chung H, Jeong JT, Kim MK and Lee Y. (2022). Development of a chloroplast-based InDel marker that discriminates between Paeonia suffruticosa and P. lactiflora. Korean Journal of Medicinal Crop Science. 30:430-439.
[https://doi.org/10.7783/KJMCS.2022.30.6.430]

-
Lim MY, Jana S, Sivanesan I, Park HR, Hwang JH, Park YH and Jeong BR. (2013). Analysis of genetic variability using RAPD markers in Paeonia spp. grown in Korea. Korean Journal of Horticultural Science and Technology. 31:322-327.
[https://doi.org/10.7235/hort.2013.12210]

-
Li Y, Shi Y, Cao Y and Wang T. (2004). Establishment of a core collection for maize germplasm preserved in Chinese National Genebank using geographic distribution and characterization data. Genetic Resources and Crop Evolution. 51:845–852.
[https://doi.org/10.1007/s10722-005-8313-8]

-
Lv H, Wang Q, Zhang Y, Yang L, Fang Z, Wang X Liu Y, Zhuang MZ, Yu H and Liu B. (2014). Linkage map construction using InDel and SSR markers and QTL analysis of heading traits in Brassica oleracea var. capitata L. Molecular Breeding. 34:87-98.
[https://doi.org/10.1007/s11032-014-0019-1]

-
Min KD, Kang YN, Kim CS, Choi CH and Kim JY. (2021). Genetic diversity and population structure of Korean common wheat(Triticum aestivum) using SSR markers. Korean Journal of Breeding Science. 53:277–288.
[https://doi.org/10.9787/KJBS.2021.53.3.277]

- Ministry of Agriculture, Food and Rural Affairs(MAFRA). (2024). Final results of the 2023 census of agriculture, forestry and fisheries. Ministry of Agriculture, Food and Rural Affairs. Sejong, Republic of Korea. pp.107-110.
- Ministry of Food and Drug Safety(MFDS). (2008). The Korea pharmacopoeia. Ministry of Food and Drug Safety. Shinilbooks. Seoul, Republic of Korea. p.969.
-
Nei M. (1973). Analysis of gene diversity in subdivided populations. Proceedings of the National Academy of Sciences USA. 70:3321-3323.
[https://doi.org/10.1073/pnas.70.12.3321]

-
Nei M and Roychoudhury AK. (1974). Sampling variances of heterozygosity and genetic distance. Genetics. 76:379-390.
[https://doi.org/10.1093/genetics/76.2.379]

-
Pacurar DI, Pacurar ML, Street N, Bussell JD, Pop TI, Gutierrez L and Bellini C. (2012). A collection of InDel markers for map-based cloning in seven Arabidopsis accessions. Journal of Experimental Botany. 63:2491-2501.
[https://doi.org/10.1093/jxb/err422]

-
Pan J, Zhang D and Sang T. (2007). Molecular phylogenetic evidence for the origin of a diploid hybrid of Paeonia (Paeoniaceae). American Journal of Botany. 94:400-408.
[https://doi.org/10.3732/ajb.94.3.400]

-
Peng M, Huang FL, Meng FJ, Hu BZ, Chen XF, Luo R, Li N, Wang RF, Zhao Y, Zou QW, Wu CT and Dai JL. (2017). Reproductive biology of Chinese herbaceous perennial peony (Paeonia lactiflora Pall.) using the paraffin method. Phyton. International Journal of Experimental Botany. 86:296-305
[https://doi.org/10.32604/phyton.2017.86.296]

-
Penner GA, Bush A, Wise R, Kim W, Domier L, Kasha K, Laroche A, Scoles G and Molnar S. (1993). Reproducibility of random amplified polymorphic DNA(RAPD) analysis among laboratories. Plant Molecular Biology Reporter. 11:17-27.
[https://doi.org/10.1101/gr.2.4.341]

- Rural Development Administration(RDA). (2008). Comprehensive catalogue of medicinal crop cultivars. Department of Medicinal Crops. NIHHS, RDA. pp.106-109.
-
Takagi K and Harada M. (1969). Pharmacological studies on herb paeony root. II. Anti-inflammatory effect, inhibitory effect on gastric juice secretion, preventive effect on stress ulcer, antidiuretic effect of paeoniflorin and combined effects with licorice component FM 100. Yakugaku Zasshi. 89:887-892.
[https://doi.org/10.1248/yakushi1947.89.7_887]

-
Talia P, Nishinakamasu V, Hopp HE, Heinz RA and Paniego N. (2010). Genetic mapping of EST-SSR, SSR and InDel to improve saturation of genomic regions in a previously developed sunflower map. Electronic Journal of Biotechnology. 13:7-8.
[https://doi.org/10.2225/vol13-issue6-fulltext-14]

-
Tamura K, Dudley J, Nei M and Kumar S. (2007). MEGA4: molecular evolutionary genetics analysis(MEGA) software version 4.0. Molecular Biology and Evolution. 24:1596–1599.
[https://doi.org/10.1093/molbev/msm092]

-
Tan S, Cheng JW, Zhang L, Qin C, Nong DG, Li WP, Tang X, Wu ZM and Hu KL. (2015). Construction of an interspecific genetic map based on InDel and SSR for mapping the QTLs affecting the initiation of flower primordia in pepper(Capsicum spp.). PloS one. 10:e0119389.
[https://doi.org/10.1371/journal.pone.0119389]

-
Wang SQ. (2019). Inbreeding and inbreeding depression of Paeonia decomposita(Paeoniaceae), a threatened endemic plant to China. Botanical Studies 60:28.
[https://doi.org/10.1186/s40529-019-0276-8]

- Wang XB, Zhang D, Shi XH, Li DQ, Zhang RL, Shao LM, Xu T, Xia YP and Zhang JP. (2022). A new Paeonia lactiflora cultivar ‘Purple Heart’. Acta Horticulturae Sinica. 49:115-116.
-
Wu K, Yang M, Liu H, Tao Y, Mei J and Zhao Y. (2014). Genetic analysis and molecular characterization of Chinese sesame(Sesamum indicum L.) cultivars using Insertion-Deletion (InDel) and Simple Sequence Repeat(SSR) markers. BMC Genetics. 15:35.
[https://doi.org/10.1186/1471-2156-15-35]

-
Wu L, Nie L, Wang Q, Xu Z, Wang Y, He C, Song J and Yao H. (2021). Comparative and phylogenetic analyses of the chloroplast genomes of species of Paeoniaceae. Scientific Reports. 11:14643.
[https://doi.org/10.1038/s41598-021-94137-0]

-
Xiang X, Li C, Li L, Bian Y, Kwan HS, Nong W, Cheung MK, Lee HH, and Xiao Y. (2016). Genetic diversity and population structure of Chinese Lentinula edodes revealed by InDel and SSR markers. Mycological Progress. 15:37.
[https://doi.org/10.1007/s11557-016-1183-y]

-
Xiang YJ, Zhang Q, Wei SJ, Huang C, Li ZS and Gao YX. (2020). Paeoniflorin: A monoterpene glycoside from plants of Paeoniaceae family with diverse anticancer activities. Journal of Pharmacy and Pharmacology. 72:483-495.
[https://doi.org/10.1111/jphp.13204]

-
Yang Y, Sun M, Li S, Chen Q, Teixeira da Silva JA, Wang A, Yu X and Wang L. (2020). Germplasm resources and genetic breeding of Paeonia: A systematic review. Horticulture Research. 7:107.
[https://doi.org/10.1038/s41438-020-0332-2]

-
Zhang HH, Wang J, Lang W, Liu HL, Zhang ZQ, Wu TL, Li HQ and Bai LY. (2022). Albiflorin ameliorates inflammation and oxidative stress by regulating the NF-κB/NLRP3 pathway in methotrexate-induced enteritis. International Immunopharmacology. 109:108824.
[https://doi.org/10.1016/j.intimp.2022.108824]

-
Zhang JP, Li DQ, Shi XH, Zhang D, Qiu S, Wei J, Zhang J, Zhou JH, Zhu KY and Xia YP. (2017). Mining and expression analysis of candidate genes involved in regulating the chilling requirement fulfillment of Paeonia lactiflora ‘Hang Baishao’. BMC Plant Biology. 17:262.
[https://doi.org/10.1186/s12870-017-1205-1]

-
Zhang XF, Sun HH, Xu Y, Chen B, Yu SC, Geng SS and Wang Q. (2016). Development of a large number of SSR and InDel markers and construction of a high-density genetic map based on a RIL population of pepper(Capsicum annuum L.). Molecular Breeding. 36:92.
[https://doi.org/10.1007/s11032-016-0517-4]

-
Zhou SL, Hong DY and Pan KY (1999) Pollination biology of Paeonia jishanensis T. Hong & W.Z. Zhao(Paeoniaceae), with special emphasis on pollen and stigma biology. Botanical Journal of the Linnean Society 130:43-52.
[https://doi.org/10.1111/j.1095-8339.1999.tb00781.x]

-
Zhu S, Yu X, Wu Y, Shiraishi F, Kawahara N and Komatsu K. (2015). Genetic and chemical characterization of white and red peony root derived from Paeonia lactiflora. Journal of Natural Medicines. 69:35-45.
[https://doi.org/10.1007/s11418-014-0857-5]

