
냉이 종자의 발아율과 발아 균일성 향상을 위한 종자 전처리 방법
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Capsella bursa-pastoris is a globally distributed weed that has long been used both as a food and medicinal resource. However, despite its potential applications, its germination conditions and related cultivation methods have not yet been well-established. When seeds are sown mixed with sand, as commonly practiced by farmers, the germination rate remains very low and the germination period is prolonged, making cultivation difficult.
In this study, we subjected seeds from four accessions of C. bursa-pastoris (CB-8, CB-9, CB-10, and CB-16), collected from different regions of the Republic of Korea, to various priming treatments to improve germination rate and speed. Under moist treatment at a low temperature (4°C for 3 days), germination rates varied among the accessions, ranging from 20% to 60%. Half-scarification enhanced germination, resulting in germination rates between 87% and 100%. Among the chemical treatments, soaking in 50% H2SO4 for 30 min yielded germination rates of 57%–90%, whereas soaking in 30% NaOH for 5 min completely inhibited germination (0%). To synchronize seed germination, we applied moisture treatment for different durations (3, 5, or 7 days) prior to half-scarification, and compared the germination speed. Under the condition of 7 days of moist treatment before half-scarification, the time required for all seeds to complete germination was shortened to within 2 days.
C. bursa-pastoris displayed variation in germination rates among accessions, and germination was improved by half-scarification and soaking in 50 % H2SO4 for 30 min. Pretreatment with moist treatment at 4 °C before half-scarification further enhanced germination rates accession-dependently. Extending the duration of the low-temperature moist treatment to 5 or 7 days increased germination speed, and in the 7-day treatment, all accessions completed germination within 2–4 days, allowing for uniform seedling production.
Keywords:
Capsella bursa-pastoris (L.) Medik., Shepherd’s Purse, Germination, Priming, Seed Dormancy서 언
Capsella bursa-pastoris (L.) Medik. (냉이)는 십자화과에 속하는 일년생의 초본 식물로 북쪽의 극지방, 아프리카 사막, 남쪽의 케르겔렌 제도에 이르는 지구상에서 가장 널리 분포한 식물 중 하나이다 (Penin et al., 2024). 냉이는 오래전부터 민간요법으로 이용되어 왔는데 유럽에서는 지혈제나 생리통 완화제로 사용되었으며, 중국과 일본에서는 출혈 억제, 해열, 백내장 치료 등 약용 목적으로 활용되었다는 기록이 남아있다. 대한민국에서도 요리 및 약용 식물로 널리 쓰였으며, 『임업경영총서』에 냉이 뿌리는 혈액 순환 개선에, 씨앗은 눈 건강에 사용된다고 적혀있다. 또한, 항염증, 항산화, 항암, 간 보호, 콜레스테롤 저하, 백내장 치료 등 약리적 효과가 있음이 증명되었다 (Ha et al., 2023).
발아는 종자가 수분을 흡수하면서 배의 휴면이 타파되고, 대사작용이 활발하게 되면서 생장이 재개되어 유근이 종피를 뚫고 나오는 일련의 과정을 의미하는데, 냉이가 채소나 약재로서 널리 이용됨에도 불구하고 냉이의 발아와 재배에 관한 표준화된 방법은 알려져 있지 않다. 냉이는 같은 개체에서 수확된 종자도 종자 색에 따라 연한 갈색의 점액질 (myxospermous seeds) 종피 종자와 짙은 갈색의 비점액질 (non-myxospermous) 종피 종자로 나눠진다 (Toorop et al., 2012). 점액질 (myxospermous seeds) 종피를 가진 냉이 종자의 경우, 종자가 수분을 흡수한 후, 식물 세포벽 다당류인 펙틴, 헤미셀룰로오스, 셀룰로오스로 구성된 부피감 있는 점액질 덮개를 형성하고, 이는 발달 중인 종피 세포에 의해 침착된다. 종자의 점액질은 발아 시 토양 입자에 대한 종자의 부착력 증가와 수분 유지, 그리고 빠른 수분 흡수를 통해, 건조한 환경에서의 생존에 유리하여 발아율 향상에 기여한다 (Deng et al., 2012; Deng et al., 2015). 그러나, 점액질 종피 종자와 비점액질 종피 종자의 발아율을 비교했을 때, 비점액질 종피 종자의 발아율이 더 높았다 (Toorop et al., 2012). 이는 종자의 점액질은 사막이나 극지방 등 척박한 환경을 극복하는데 유리하지만 (Deng et al., 2012), 발아에 적절한 환경에서는 종자의 수분 흡수를 저해하여 오히려 발아율을 낮출 수 있음을 보여준다.
종자 휴면은 환경에 대한 식물의 적응 메커니즘 중 하나로, 생장에 적합한 환경조건이 조성될 때까지 발아를 억제하는 역할을 한다 (Park et al., 2019). 종자 휴면은 휴면 메커니즘에 따라 크게 다섯 가지로 분류된다. 종피의 불투과성으로 인해 발아가 억제되는 물리적 휴면, 종자 내 억제 물질로 인해 발아가 억제되는 생리적 휴면, 배 미성숙으로 발아하지 않는 형태적 휴면, 생리적 휴면 상태에서 형태적 휴면 요인이 복합된 형태·생리적 휴면, 물리적 휴면 요인이 복합된 조합 휴면이다 (Baskin and Baskin, 2004). 종자의 휴면은 종 (species) 특이적이지만, 동일한 분류학적 계급 (과 및 속) 내에서도 종의 지리적 분포와 생태학적 배경에 따라 휴면의 유형과 정도가 달라질 수 있다 (Han et al., 2014). 종자 프라이밍 (seed priming)은 종자의 휴면은 타파하고 발아되지 않을 정도의 수분을 종자에 흡수시키는 파종 전처리 기술로, 효소 활성, 저장양분 분해 및 에너지 대사, 단백질 합성, 세포 복구 등 생화학적 활성과 항산화 방어 시스템 활성 향상을 통해 발아에 필요한 생리적인 준비를 갖추게 유도하여 발아와 초기 유묘의 발달을 촉진시킴으로써 발아속도와 균일성을 향상시킬 수 있다. 수분 프라이밍 (hydro priming), 화학 프라이밍 (chemical priming), 삼투 프라이밍 (osmotic priming), 생물 프라이밍 (bio priming), 물리 프라이밍 (physical priming), 등 여러 프라이밍 방법이 연구되었고, 다양한 원예 작물 및 식량 작물에 적용되고 있다 (Han et al., 2014; Hassan et al., 2023). 수분 프라이밍은 물을 이용한 방법으로 종자를 일정 시간 동안 물에 침지시킨 후 특정 수분 수준까지 건조시키는 방법으로, 파종 전 발아력을 향상시키는 데 효과적이다 (Harris, 1992). 이 방법은 벼, 해바라기와 같은 작물에서 발아 능력과 유묘 출현의 균일성을 개선하는 데 효과적으로 사용되어 왔다 (Fu et al., 2024). 화학 프라이밍은 종자의 종피를 일부 제거시키거나 부식시켜 종자의 투수성을 높이고 발아를 촉진시키는 방법으로 황산 (H2SO4), 수산화칼슘 (Ca(OH)2), 차아염소산나트륨 (NaOCl) 등의 화학약품이 사용되고 있다 (Han et al., 2014). Sabina vulgaris와 Adansonia digitata의 경우 H2SO4 처리하면 종피 조직이 연화되어서 배의 수분 흡수를 촉진시키고, 종자 휴면이 타파되어 종자 발아율이 향상되었다 (Hassan et al., 2023). 염처리 (Halo) 프라이밍은 화학 프라이밍 방법 중 하나로 파종 전 염류 (NaCl, NaNO3, MgCl2, KNO3 등)가 포함된 용액에 종자를 침지하여 불량환경에서 발아율과 유묘 발생을 향상시키기 위한 방법이며, 삼투 프라이밍은 PEG (polyethylene glycol) 용액으로 수분 퍼텐셜을 조절하여 한계 수분 처리하는 방법이다 (Han et al., 2014; Hassan et al., 2023). 바이오프라이밍은 종자를 미생물이 포함된 용액에 침지처리하는 방법으로, 미생물은 식물 생장을 촉진하며, 발아 이후에도 뿌리 표면에 붙어 식물 생장을 보조한다. 대표적인 미생물로는 Pseudomonas, Enterobacter, Xylaria와 Bacillus가 있다. 물리프라이밍은 종자에 비화학적 (물리적) 자극이나 환경 조건을 이용해 종자의 생리적 상태를 변화시키는 방법이다. 종피를 깎거나 긁어 발아를 방해하는 물리적 장벽을 제거하는 기계적 가사(mechanical scarification)와 고체 미세 분말, 물, 종자를 일정비율로 혼합하여 종자의 수분 흡수를 조절함으로써 발아력을 향상시킬 수 있는 고체 매트릭스 프라이밍 (solid matrix priming) 처리 등 다양한 방법이 있다 (Lee et al., 2011; Han et al., 2014; Fu et al., 2024).
양영택 (2017)에 따르면 냉이 재배 농가에서는 종자를 모래와 1:1 비율로 혼합하여 파종하는데, 발아율이 30% 이하로 낮으며 파종 시기에 따라 발아까지 최대 1개월이 소요되고 개체마다 발아 시기가 균일하지 않다. 이는 냉이의 재배와 수확 시기를 예측하기 어렵다는 것을 보여준다. 그러나 이전 연구들에서 저온·습윤 처리 (moist stratification, wet pre-chilling), GA3 및 KNO3 등 다양한 프라이밍 방법을 적용하였을 때 최소 10%에서 최대 48.51%의 발아율을 보였다 (Toorop et al., 2012; Rezvani et al., 2014). 이는 저온 습윤 처리 및 프라이밍 방법 최적화로 국내 재배용 냉이 계통들의 낮은 종자 발아율과 불균일한 발아세를 개선할 수 있고, 이를 통해 자연채집 의존도와 재배 안정성의 불균형을 해소하여 냉이의 약리성분에 대한 대사체 연구와 식·의약 산업에서의 수요에 효과적으로 대응할 수 있음을 시사한다.
이에 본 연구에서는 다양한 프라이밍 기법과 저온 처리 기간 변화가 국내 지역별 냉이 계통들의 발아율 및 발아 속도에 미치는 영향을 비교·분석하였으며, 이를 통해 냉이의 재배 안정성 증진을 위한 냉이 종자 전처리 방법을 제시하고자 하였다.
재료 및 방법
1. 종자 준비
본 연구에 사용된 종자는 전라북도, 충청남도, 경기도, 경상북도에서 채집한 Capsella bursa-pastoris (L.) Medik. [K281355 (CB-8), K281356 (CB-9), K281357 (CB-10), K281363 (CB-16)]의 종자이다 (Fig. 1). 종자 상태에 의한 실험 결과 변이 최소화를 위해, 국립농업과학원 농업유전자원센터 (National Agrobiodiversity Center, NAC)로부터 각 자원의 종자를 분양받아 2024년 9월에 표면 소독한 종자를 발아 배지에 치상 후 4℃에서 저온 습윤 처리 (3일, 암조건)하였다 (Toorop et al., 2012). 저온 습윤 처리된 종자는 양영택 (2017)에서 가장 발아율이 높았던 (27%) 20℃ 조건에서 재배하였다 (Young Taek Yang., 2017). 식물생장상 (HB-302S-2, Hanbaek Scientific Technology, Korea)을 사용하여 장일 조건 (16시간 광주기/8시간 암주기)에서 2주 경과 후 발아된 개체들을 원예용 상토로 이식하여 재배하였다. 2025년 1월에 일시에 수확하여 종자 상태를 균일화하였고 이 종자들을 실험에 사용하였다.
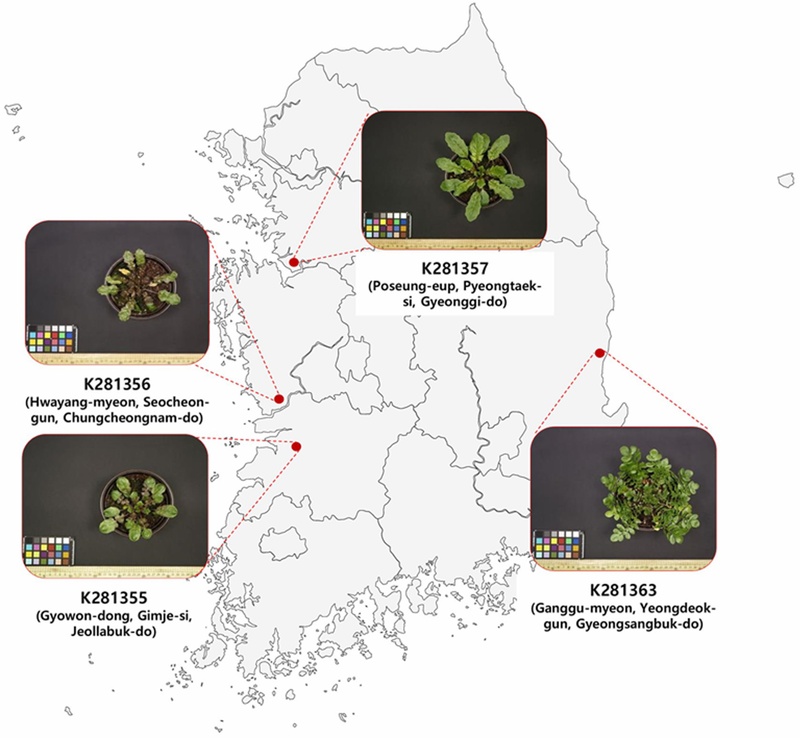
Accession numbers and collection sites of Capsella bursa-pastoris.The four accessions obtained from the National Agrobiodiversity Center (NAC), Rural Development Administration were originally collected from natural habitats in Jeollabuk-do (CB-8; K281355, 35°47′10″N, 126°51′42″E), Chungcheongnam-do (CB-9; K281356, 36°03′05?N, 126°47′10″E), Gyeonggi-do (CB-10; K281357, 36°59′25″N, 126°51′27″E), and Gyeongsangbuk-do (CB-16; K281363 36°22′53″N, 129°22′04″E) provinces in South Korea. Plant images were captured using a digital camera with a color chart and a scale bar included in the frame.
2. 종자 소독 및 생육 조건
종자는 0.01% Tween 20을 첨가한 1% NaOCl 용액에 5분간 침지 후, 멸균수로 3회 세척하여 표면을 소독하였다. 소독된 종자는 pH 5.7 조건에서 1% plant agar (Duchefa Biochemie, Haarlem, Netherland)와 1/2 MS (Murashige and Skoog) (with vitamin, Duchefa Biochemie, Haarlem, Netherland)로 제조한 발아 배지에 치상하여 20℃, 장일 조건 (16시간 광/8시간 암)의 식물생장상에서 발아 및 생육하였다.
3. 종자 휴면 타파 처리
표면이 소독된 종자를 발아 배지에 치상 후 4℃에서 저온 습윤 처리 (3일, 암조건)하여 생리적 휴면 타파를 수행하였으며, 다른 휴면 타파 방법들의 효과를 비교하는 대조구로 이용하였다. 물리적 휴면 타파는 표면이 소독된 종자를 멸균된 필터페이퍼와 2ml의 멸균수가 첨가된 페트리디쉬 위에 올리고 현미경으로 관찰하여 가로 방향으로 30~50%를 절단하여 수행하였고 (Lee et al., 2011), 새로운 발아 배지에 치상하였다. 종피 연화를 통한 화학적 휴면 타파는 표피 소독된 종자를 H2SO4 50%에 각각 15분, 30분 침지하거나 수산화나트륨 (NaOH) 30%에 5분 침지하여 수행하였다. 화학 처리 후에는 잔류한 약품을 제거하기 위해 멸균수로 2회 세척한 후 치상하였다. 프라이밍 처리가 발아율과 발아속도에 미치는 영향을 대조구의 휴면 타파 시점과 맞추어 비교하기 위해, 대조구는 다른 휴면 타파 처리보다 3일 먼저 실시하였으며 모든 처리구는 동일한 조건에서 동일 기간 생육시켰다.
조합 휴면 (물리·생리적) 타파 방법으로 발아 배지에 치상된 종자를 4℃와 20℃에서 각각 3일간 습윤 처리한 후 앞서 기술한 물리적 방법을 병행하였다. 휴면 타파 처리된 종자들은 새로운 발아 배지에 재치상하였다.
4. 종자 절단 전 저온 처리 기간에 따른 발아율과 발아 속도 비교
표면 소독된 종자를 발아배지에 치상한 후, 4℃에서 각각 3일, 5일, 7일간 저온 습윤 처리를 수행하였으며, 저온 습윤 처리된 종자는 앞서 기술한 물리적 방법으로 종자의 일부를 제거하였다. 각 자원의 종자 발아율은 일주일 동안 매일 동일한 시각에 조사하였다.
5. 발아율 및 발아 특성 분석
최종 발아율은 각 프라이밍 처리가 끝난 시점을 기준으로 2주 경과되었을 때 조사하였으며, 각각의 처리는 각 자원 별로 10립씩 3반복으로 수행하였다. 발아 여부는 자엽의 개방 여부를 기준으로 판정하였으며, 발아율 [Percent germination: PG=(N / S)×100 (N: 총 발아수; S: 총 공시 종자수)], 평균 발아일수 [Mean germination time: MGT= Σ (Ti × Ni) / N (Ti: 치상 후 조사일수; Ni: 조사당일 발아수; N: 총발아수)] 및 평균 발아속도 [Mean daily germination: MDG = N / T (N: 총 발아수; T: 총 조사일수)]를 조사하였다 (Han et al., 2014).
결과 및 고찰
1. 국내 자생 냉이 계통들의 종자 발아율 확인
야생에서 서식하는 식물의 종자는 1~5℃의 저온에서 휴면이 타파된다 (Jeon et al., 2013; Rezvani et al., 2014; Song et al., 2015). 전라북도 (K281355 [CB-8]), 충청남도 (K281356 [CB-9]), 경기도 (K281357 [CB-10]), 경상북도 (K281363 [CB-16]) 4개 지역 자생 냉이 종자는 발아 배지에 치상 후 4℃에서 3일간 저온 습윤 처리하였다 (Toorop et al., 2012). 이전 연구 (양영택, 2017)에서 가장 발아율이 높았던 온도 조건 20℃ (27% 발아율)을 적용하여 식물생장상에서 2주간 발아를 유도하고 각 계통의 발아율을 조사하였다 (Fig. 2A). CB-8, CB-9, CB-10, CB-16 계통의 발아율은 각각 60%, 40%, 20%, 20%로, 동일한 조건 하에서 계통에 따라 최대 40% 이상의 발아율 차이를 보였다 (Fig. 2B). 같은 종의 발아율을 비교한 이전의 연구들에서 구상나무 종자는 채집 지역에 따라 발아율의 차이를 보였으며, 우엉의 경우 계통에 따라 발아율의 차이가 있었는데, 이는 같은 종이라도 채집 지역과 계통에 따라 발아율이 다를 수 있다는 것을 의미한다 (Lee et al., 2003; Gang et al., 2017). 본 연구의 재료로 사용한 냉이 계통들간의 서식지 위도 차이는 1도 정도로 큰 차이가 없었으나 식물체의 모양과 발아율이 매우 달랐다 (Fig. 1, Fig. 2B and 2C). 이 결과는 국내에 자생하는 냉이 계통의 유전형이 지역별로 다를 수 있음을 보여준다 (Fig. 1).
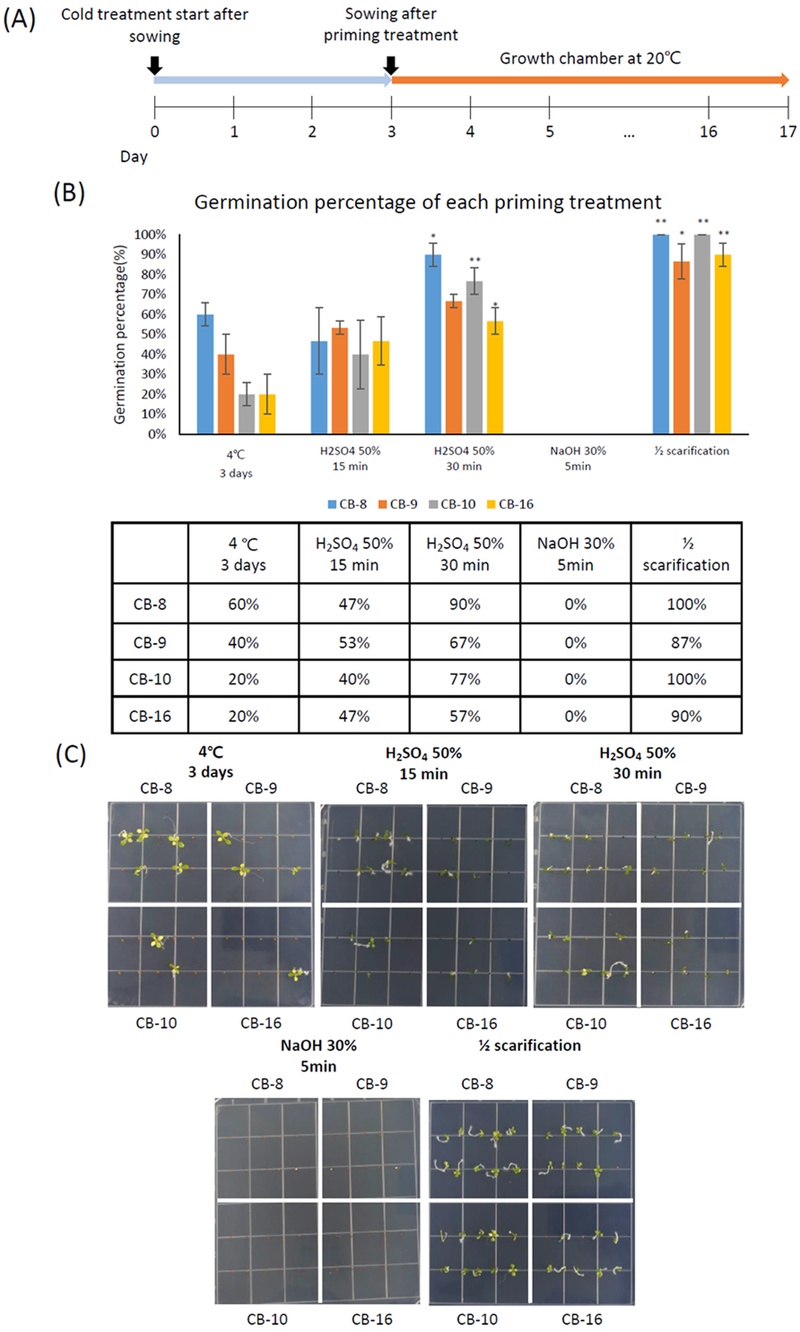
Germination of accession seeds under various priming treatments.(A) Timeline of seed priming treatments. (B) Germination percentage of accessions for each priming treatments (4℃ for 3 days, 1/2 scarification, 50% H2SO4 for 15 or 30 minutes, 30% NaOH for 5 minutes). Data are shown as means ± SD, with statistical significance assessed by Student’s t-test: *P < 0.05, **P < 0.01. (C) Germination status of accessions after 2 weeks for each priming treatments.
2. 휴면 타파 방법에 따른 발아율 향상
냉이 종자의 발아율에 다양한 프라이밍 처리 방법들이 미치는 영향을 확인하기 위해, 물리적 프라이밍 [1/2 scarification (종자 절단)]과 두 가지 화학적 프라이밍 (50% H2SO4, 30% NaOH) 처리를 하였다. 저온 (4℃) 습윤 처리한 CB-8, CB-9, CB-10, CB-16 계통의 발아율 (60%, 40%, 20%, 20%)과 비교하여 물리적 방법 (1/2 scarification)을 처리한 CB-8, CB-9, CB-10, CB-16 계통의 종자 발아율은 각각 100%, 87%, 100%, 90%로, 이는 계통별 발아율이 47~80% 향상되었고 통계적으로도 유의한 증가임을 보여주었다 (Fig. 2B and 2C). 50% H2SO4 용액에 30분간 침지 처리한 경우, CB-8, CB-9, CB-10, CB-16에서 각각 90%, 67%, 77%, 57%의 발아율을 보였으며, CB-9를 제외한 3개의 계통에서 통계적으로 유의하게 발아율이 증가하였다 (Fig. 2B and 2C). 50% H2SO4 용액에 15분간 침지 처리한 경우는 CB-8, CB-9, CB-10, CB-16에서 각각 47%, 53%, 40%, 47%의 발아율을 보였으나, 저온 습윤 처리와 비교하여 발아율이 향상되지 않았다 (Fig. 2B and 2C). 염처리는 종자를 불량 환경에 적응시켜 발아율을 향상시키기 위한 방법으로 사용되며, 잔디 종자는 25-30%의 KOH 용액에 30-40분간 처리 후 수세하여 음건한 후 파종하는 방법이 통용된다 (Han et al., 2014). 냉이 종자의 경우 30% NaOH에 침지 처리 하였을 때 발아가 전혀 되지 않았으므로, 염처리는 부적합한 조건으로 사료된다 (Fig. 2B and 2C). 이번 실험에서 50% H2SO4 30분 침지 처리와 1/2 scarification 처리, 특히 87%~100%의 발아율을 보인 1/2 scarification 처리가 냉이 종자의 발아에 효과적인 프라이밍 방법임을 확인하였다. 냉이 종자는 점액질 종피 종자에 비해 비점액질 종피 종자의 발아율이 더 높았는데 (Toorop et al., 2012), 1/2 scarification 처리로 종자의 수분 흡수를 방해하여 발아율을 저하시키는 원인인 불투성 점액질 종피가 물리적으로 제거된 것이 종자의 발아율을 현저히 향상시킨 것으로 사료된다. 또한 종자가 발아할 때 유근이 먼저 출연한 후 자엽이 종피를 뚫고 나오지만, 본 연구에서 1/2 scarification 처리된 냉이 종자의 경우 자엽이 먼저 출연 후 유근이 발달하였다. 이는 해당화 종자를 half-cut하여 발아율을 향상시킨 연구에서 보였던 유묘 발달과 유사한 과정으로 사료된다 (Lee et al., 2011).
저온 습윤 처리는 종자의 생리적 휴면을 타파하여 종자 발아율을 향상시키는데 냉이 종자에 대한 이전의 연구에서 저온 습윤 처리 기간이 길수록 종자 발아율이 향상되었다는 보고가 있다 (Rezvani et al., 2014). 휴면 타파를 위한 습윤 처리 온도의 경우 식물 종에 따라 다른데, 어수리 종자는 5℃에서 82%, 눈개승마는 15℃에서 93.3%, 삽주는 15℃와 20℃에서 100%, 백초향과 선학초는 20℃에서 가장 높은 발아율을 보였다 (Jeon et al., 2013; Song et al., 2015). 냉이 종자에 적합한 습윤 처리 온도 조건을 확인하기 위해 배지에 치상한 종자를 4℃와 20℃에서 각각 3일간 습윤 처리하였다. 습윤 처리 후, 종자 발아율 향상에 가장 효과적이었던 1/2 scarification 처리를 하였고 새로운 발아 배지에 재치상하여 2주 후 발아율을 비교하였다 (Fig. 3A). 그 결과, CB-9의 발아율은 3일간 20℃에서 습윤 처리 후 1/2 scarification 처리 시 67%의 발아율을, 4℃에서 3일간 습윤 처리 후 1/2 scarification 처리 시 93%의 발아율을 보였다 (Fig. 3B and 3C). 4℃ 처리가 20℃ 처리에 비해 종자 발아율이 26% 향상되었으므로, 4℃가 냉이 종자에 적합한 습윤 처리 온도로 확인되었다. 반면, CB8, CB-10, CB-16에서는 유의미한 차이가 관찰되지 않았다. 1/2 scarification을 통한 물리적 휴면 타파 방법이 냉이 종자 휴면 타파에 효과적인 방법이지만, CB-9와 같이 1/2 scarification으로도 발아율이 낮은 계통의 경우 1/2 scarification 전 4℃ 습윤 처리를 통해 발아율이 향상됨을 보여주었다. 선행 연구에서 Malus domestica, Juglans regia, Corylus avellana 종자의 휴면 타파를 위해 저온 처리를 하였는데, 이때 종자 내 abscisic acid 함량이 감소하며 gibberellin 함량이 증가하였고, 지질, 당, 단백질의 분해를 통해 발아에 필요한 아미노산과 전분 함량이 증가하여 발아율이 향상되었음이 보고되었다 (Chen et al., 2015). 본 연구의 결과에서도 1/2 scarification (종자 절단)만으로 냉이 종자의 발아율은 향상되나 (Fig 1B and 1C), 계통에 따라 생리적 휴면 타파가 필요하거나 수확 후 저장 기간이 짧아 종자의 충실도가 부족하면 선택적으로 1/2 scarification 처리와 4℃ 습윤 처리를 병행하여 발아율을 높일 수 있음을 보여주었다.
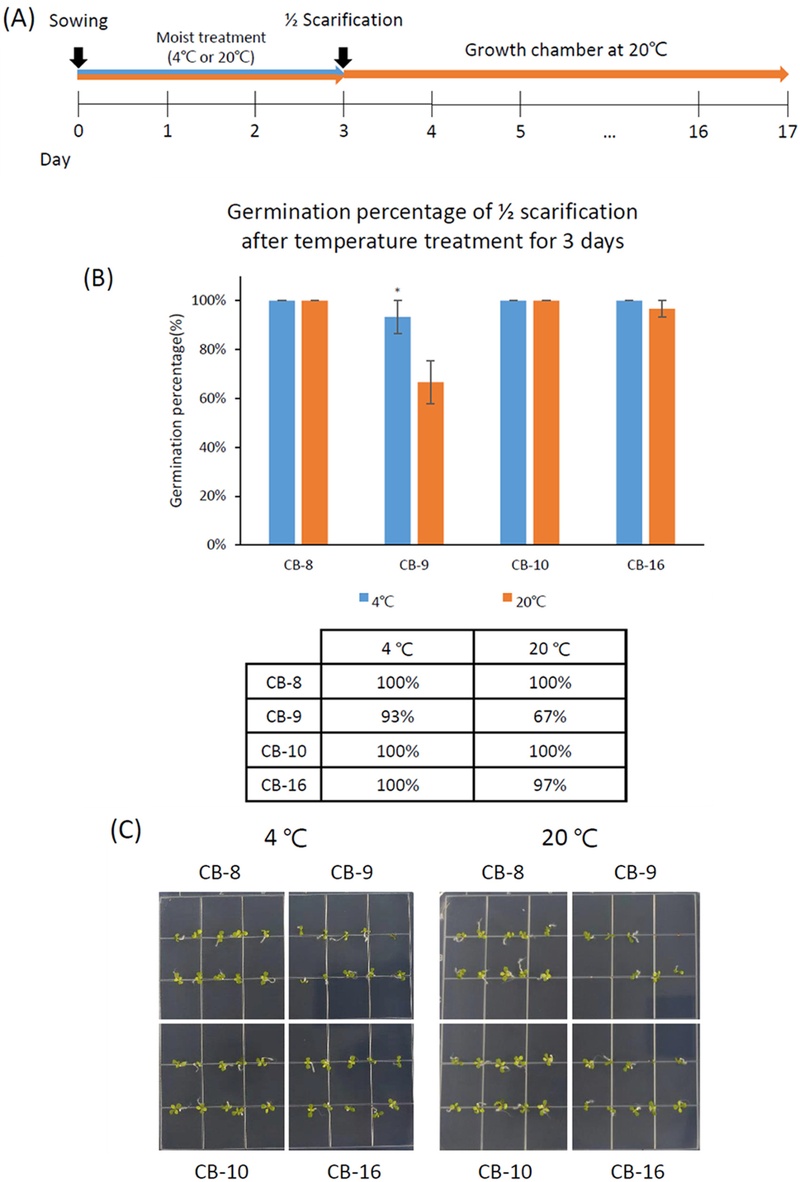
Germination of accession seeds after 1/2 scarification following moist treatment under two temperatures (4℃ and 20℃).(A) Timeline of priming treatment. (B) Germination percentage of 1/2 scarification after moist under two temperatures (4℃ and 20℃). Data are shown as means ± SD, with statistical significance assessed by Student’s t-test: *P < 0.05. (C) Seedlings of each accession after germination.
3. 저온 처리 기간 증가에 따른 발아 속도 비교
냉이 종자는 개체마다 발아 속도가 달라 파종 후 처음 발아한 종자와 마지막으로 발아하는 종자 간의 발아 시기 차이가 1개월이 되기도 한다. 이러한 이유로 냉이 수확 역시 긴 기간에 걸쳐 수확하게 되어 노동력이 분산되고 대량 재배에 불리하다. 눈개승마의 경우 저온 (20℃) 처리 기간이 길어질수록 발아 시작일이 앞당겨지고, 최종 발아까지 도달하는 기간이 짧아진다는 연구 결과가 있다 (Song et al., 2015). 저온 (4℃) 습윤 처리 기간이 냉이의 발아 속도에 미치는 영향을 확인하기 위해 1/2 scarification 처리 전 3일, 5일, 7일간 저온 습윤 처리를 하여 종자를 절단한 후에 발아 배지에 치상하였다 (Fig. 4A). 3일간 저온 습윤 처리한 경우 모든 종자의 발아까지 4-6일 (CB-8, CB-9, CB-10, CB-16 각각 4, 6, 6, 5일) 소요되었다. 그러나 5일간의 저온 습윤 처리에서는 2-5일 (CB-8, CB-9, CB-10, CB-16 각각 2, 5, 4, 4일), 7일간의 저온 습윤 처리의 경우에는 2-4일 (CB-8, CB-9, CB-10, CB-16 각각 2, 2, 4, 3일)로 단축되었다 (Fig. 4B). 각 계통의 평균발아일수 (MGT)를 비교한 결과, CB-8은 3일간 처리 시 2.23일에서 5일간과 7일간 처리시 2일로 평균발아일수를 0.23일 단축시켰으나 통계적으로는 유의미한 차이가 없었다. CB-9는 3일간과 5일간 처리에서 동일하게 2.86일 소요되었으나 나 7일간 처리시 2.1일로 평균발아일수가 0.76일 단축되었다. CB-10과 CB-16의 경우 3일간 처리시 각각 3.03, 3.1일 소요되었고, 5일간 처리시 3일간 처리와 비교하여 각각 0.8, 0.44일 단축되어 2.23, 2.66일 소요되었다. 7일간 처리시 3일간 처리와 비교하여 0.73, 0.87일 단축되어 2.3, 2.23일 소요되었다. CB-10과 CB-16은 저온 습윤 처리가 길어질수록 평균발아일수가 단축되었다 (Fig. 4C). 평균발아속도 (MD G)는 CB-8과 CB-10의 경우 3일간 처리 시 일일 평균 총 10개의 종자 중 각각 3.33개와 2.06개 발아하였고, 5일과 7일간 처리는 일일 평균 발아 종자 수가 각각 5개, 3.06개로 증가하였다. CB-9와 CB-16의 경우 3일간 처리에서 각각 1.67개, 2.17개, 5일간 처리에서 각각 2개, 2.5개 발아하였고, 7일간 처리에서 일일 평균 발아 종자 수가 각각 3.89개, 3.33개로 증가하였다 (Fig. 4D). 이 결과로 1/2 scarification 처리 전 저온 습윤 처리는 냉이 계통과 무관하게 종자 발아를 촉진시킬 수 있으며, 5일과 7일간의 습윤 처리로 종자의 발아를 좀 더 균일하게 할 수 있음을 보여주었다. 저온 습윤 처리 기간은 이후의 2주간의 냉이 유묘 생장에 영향을 주지 않았다. 저온 습윤 처리는 종자 내 대사를 활성화하여 식물생장호르몬을 변화시키고 아미노산과 전분의 함량을 증가시켜 외부 환경 요건이 충족되면 종자가 발아될 수 있도록 준비시키는 역할을 한다고 알려져 있다 (Rezvani et al., 2014; Chen et al., 2015; Park et al., 2019). 본 실험에서 저온 습윤 처리는 생물학적으로 발아 준비가 된 냉이 종자의 수를 증가시키고, 1/2 scarification 처리를 통해 발아에 필요한 수분 흡수를 가능하게 하여 발아를 촉진시킨 것으로 사료된다.
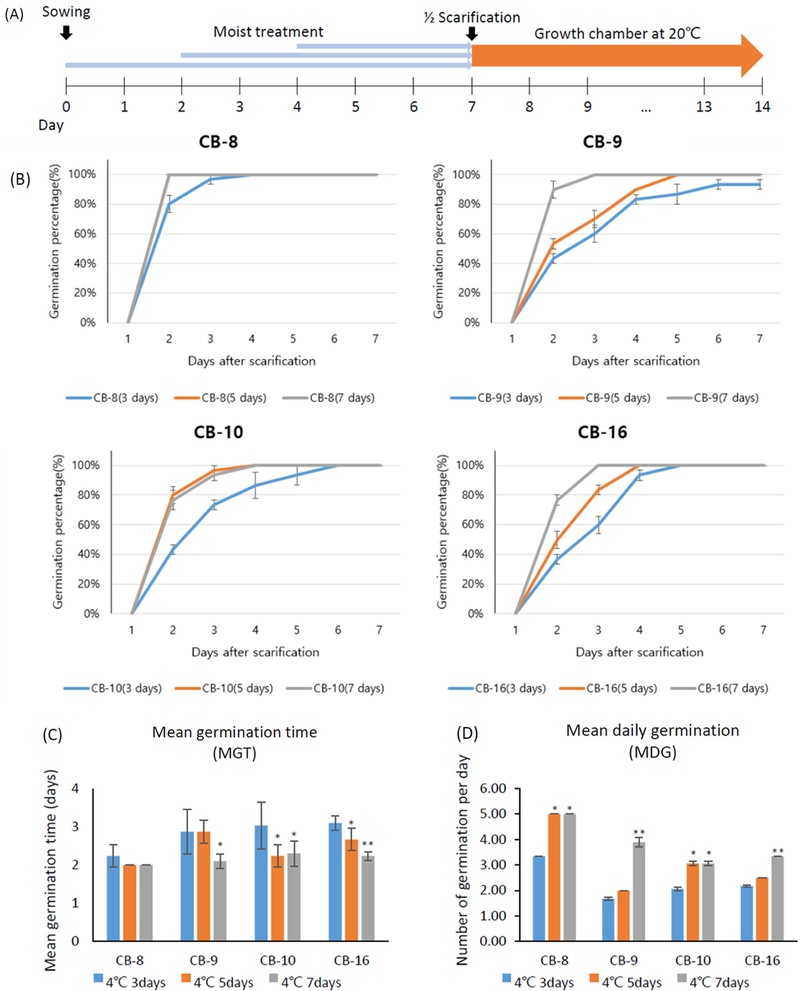
Germination period of accession seeds after moist treatment.(A) Timeline of each moist treatment and cumulative germination percentage assessment. (B) Cumulative Germination Percentage of Accession Seeds after 3-, 5-, and 7-Day Moist Treatment. (C) Mean germination time (MGT) of each accession seeds after 3, 5, and 7 days of moist treatment. MGT was calculated using the formula: MGT = Σ(Ti × Ni) / N, where Ti is the number of days after sowing, Ni is the number of seeds germinated on day i, and N is the total number of germinated seeds (D) Mean daily germination (MDG) of each accessions seeds after 3, 5, and 7 days of moist treatment. MDG was calculated using the formula: MDG = N / T, where N is the total number of germinated seeds and T is the total number of days observed. Data are shown as means ± SD, with statistical significance assessed by Student’s t-test: *P < 0.05, **P < 0.01.
본 연구에서는 냉이 종자의 휴면 타파 및 발아 균일화를 위한 효과적인 처리 조건을 제시하였다. 4℃ 저온 습윤 처리로는 계통 간 발아율 차이 (20~60%)를 보였으나, 1/2 scarification 처리는 계통에 관계없이 87~100%의 높은 발아율을 확보하였다 (Fig. 2B). 특히 1/2 scarification 전 7일간의 저온 습윤 처리를 병행할 경우 발아가 2–4일 이내에 완료되어 발아 속도와 균일성이 크게 향상되었다 (Fig. 4B and 4C). 이러한 처리 방법은 냉이 종자의 발아 안정성과 생육 균일성을 효과적으로 개선할 수 있는 실용적 기술로 판단되며, 안정적 재배 관리뿐 아니라 대사산물 연구 및 식·의약 소재 활용을 위한 기초 재료 확보에도 유용하게 활용될 수 있을 것으로 기대된다.
Acknowledgments
본 연구는 농촌진흥청 연구사업(과제번호: PJ01744503, PJ01740003)의 지원에 의해 이루어진 결과로 이에 감사드립니다.
References
-
Baskin JM and Baskin CC. (2004). A classification system for seed dormancy. Seed Science Research. 14:1-16.
[https://doi.org/10.1079/SSR2003150]

-
Chen SY, Chou SH, Tsai CC, Hsu WY, Baskin CC, Baskin JM, Chien CT and Kuo-Huang LL. (2015). Effects of moist cold stratification on germination, plant growth regulators, metabolites and embryo ultrastructure in seeds of Acer morrisonense(Sapindaceae). Plant Physiology and Biochemistry. 94:165-173.
[https://doi.org/10.1016/j.plaphy.2015.06.004]

-
Deng W, Hallett PD, Jeng DS, Squire GR, Toorop PE and Iannetta PP. (2015). The effect of natural seed coatings of Capsella bursa-pastoris L. Medik.(shepherd’s purse) on soil-water retention, stability and hydraulic conductivity. Plant and Soil. 387:167-176.
[https://doi.org/10.1007/s11104-014-2281-8]

-
Deng W, Jeng DS, Toorop PE, Squire GR and Iannetta PP. (2012). A mathematical model of mucilage expansion in myxospermous seeds of Capsella bursa-pastoris(shepherd's purse). Annals of Botany. 109:419-427.
[https://doi.org/10.1093/aob/mcr296]

-
Fu Y, Ma L, Li J, Hou D, Zeng B, Zhang L, Liu C, Bi Q, Tan J, Yu X, Bi J and Luo L. (2024). Factors influencing seed dormancy and germination and advances in seed priming technology. Plants. 13:1319. https://www.mdpi.com/2223-7747/13/10/1319, (cited by 2025 Nov 21).
[https://doi.org/10.3390/plants13101319]

-
Ha KH, Kim JA, Lee SC, Park SY, Kwon SJ, Lee SI and Lee JY. (2023). Current research status and potential applications of Capsella bursa-pastoris(L.) Medik. Korean Journal of Medicinal Crop Science. 31:377-387.
[https://doi.org/10.7783/KJMCS.2023.31.6.377]

-
Han JJ, Lee KS, Park YB, Yang GM and Bae EJ. (2014). Comparison of germination characteristics and various pre-treatment methods for enhancing germination on zoysiagrass. Weed & Turfgrass Science. 3:232-239.
[https://doi.org/10.5660/WTS.2014.3.3.232]

-
Hassan FE, Alyafei MA, Kurup S, Jaleel A, Al Busaidi N and Ahmed ZF. (2023). Effective priming techniques to enhance ghaf(Prosopis cineraria L. Druce) seed germination for mass planting. Horticulturae. 9:542.
[https://doi.org/10.3390/horticulturae9050542]

-
Jeon KS, Song KS, Yoon JH, Kim CH and Kim JJ. (2013). Effects of seed pretreatment and environment controls on germination of Atractylodes japonica seeds. Korean Journal of Medicinal Crop Science. 21:394-400.
[https://doi.org/10.7783/KJMCS.2013.21.5.394]

-
Kang GH, Hwang BY, Lee SH, Kim SH, Jo SE and Park EH. (2017). Germination characteristics of Abies koreana Wilson seed in subalpine coniferous forest by collecting location. Journal of Agriculture & Life Science. 52:133-141.
[https://doi.org/10.14397/jals.2018.52.1.133]

- Lee JH, Lim JH, Cheung JD and Suh DW. (2003). Major characteristics of burdock(Arctium lappa L.) native to Yeong-Nam region. Korean Journal of Plant Resources. 16:8-14.
- Lee JY, Lee JH, Ki GY, Kim ST and Han TH. (2011). Improvement of seed germination in Rosa rugosa. Korean Journal of Horticultural Science and Technology. 29:352-357.
- Park HB, Ko CH, Kim SY, Lee KC, Kim JH and Chung JM. (2019). Dormancy type and germination characteristics of seeds of Lonicera chrytsantha Turcz. Ex Ledeb(Caprifoliaceae). Korean Journal of Plant Resources, 32:457-462.
-
Penin AA, Kasianov AS, Klepikova AV, Omelchenko DO, Makarenko MS and Logacheva MD. (2024). Origin and diversity of Capsella bursa-pastoris from the genomic point of view. BMC biology. 22:52.
[https://doi.org/10.1186/s12915-024-01832-1]

-
Rezvani M, Zaefarian F and Amini V. (2014). Effects of chemical treatments and environmental factors on seed dormancy and germination of shepherd's purse(Capsella bursa-pastoris(L.) Medic.). Acta Botanica Brasilica. 28:495-501.
[https://doi.org/10.1590/0102-33062014abb3337]

-
Song KS, Jeon KS, Choi KS, Kim CH, Park YB and Kim JJ. (2015). Effects of storage duration with low temperature and wet condition, germination temperature and shading rate on germination of Aruncus dioicus var. kamtschaticus seeds. Korean Journal of Medicinal Crop Science. 23:370-378.
[https://doi.org/10.7783/KJMCS.2015.23.5.370]

-
Toorop PE, Campos Cuerva R, Begg GS, Locardi B, Squire GR and Iannetta PP. (2012). Co-adaptation of seed dormancy and flowering time in the arable weed Capsella bursa-pastoris(shepherd's purse). Annals of Botany. 109:481-489.
[https://doi.org/10.1093/aob/mcr301]
