
주기적인 질소 추비가 인삼(Panax ginseng)의 뿌리 비대 및 세포벽 관련 유전자 발현에 미치는 영향
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Although nitrogen (N) is a critical nutrient for the growth of Panax ginseng, its excessive application often induces physiological disorders. To establish an effective fertilization strategy, in this study, we investigated how periodic N topdressing affects root hypertrophy and cell wall-related gene expression.
We performed a 26-week pot experiment on 2-year-old ginseng plants treated with various urea concentrations (0, 2.5, 5.0, and 10.0 ㎏/10 a). In addition, we performed a field trial on 3-year-old ginseng plants from July to October (12 weeks) to compare split application frequencies. In the pot experiment, the 10.0 ㎏/10 a N treatment delayed leaf senescence and increased root weight by 28.5% compared to the control. In the field, split application (i.e., six times at 2-week intervals) was more efficient than less frequent application, increasing the yield and root hardness by 23.7% and > 10%. Real-time qPCR analysis performed using samples from the pot experiment revealed that N treatment rapidly upregulated EXPB3 and CESA6 within 24 h, indicating activated cell wall loosening and secondary wall synthesis.
Periodic N topdressing promoted secondary growth and improved root quality in P. ginseng by activating cell wall-related genes without causing salt injury. Split application of urea has been suggested as an optimal nutrient management strategy for maximizing ginseng yield and quality.
Keywords:
Panax ginseng, Cell Wall Gene, Nitrogen Top Dressing, Root Hardness, Root Hypertrophy, Secondary Growth, Split Application, Urea서 언
인삼 (Panax ginseng C. A. Meyer)은 두릅나무과 (Araliaceae)에 속하는 다년생 반음지성 식물로, 주요 약리 성분인 진세노사이드 (Ginsenoside)를 함유하여 항암, 면역 증강 피로 회복 등 다양한 생리활성을 나타내는 것으로 알려져 있다 (Kim et al., 2015; RDA, 2021). 일반적인 작물과 달리 인삼은 4 – 6년이라는 긴 재배 기간을 필요로 하는데, 이 과정에서 토양 내 양분 조건은 인삼의 지하부 비대와 품질을 결정짓는 가장 중요한 요인 중 하나로 작용한다 (Lee et al., 2014; Kim et al., 2025).
그중에서도 질소 (Nitrogen)는 식물의 생장과 발달에 필수적인 다량원소로서 단백질, 핵산, 엽록소 및 2차 대사산물의 구성 성분이 되며, 작물의 수량과 품질에 직접적인 영향을 미친다 (Li et al., 2025). 최근 보고에 따르면, 인삼에 있어 적절한 질산태 질소 (Nitrate)의 공급은 단순히 지상부 생육을 촉진할 뿐만 아니라, 형성층 줄기세포의 활성을 자극하여 지하부의 2차 비대 생장을 유도하는 핵심 신호로 작용함이 밝혀졌다 (Geem et al., 2023). 하지만 인삼은 타 작물에 비해 양분 요구도가 낮고 염류에 매우 민감하다는 생리적 특성을 지닌다. 과다한 질소 공급은 토양 염류 집적을 유발하여 적변삼 (Rusty root) 발생을 증가시키고, 뿌리 표피세포 붕괴 및 병해 저항성 감소를 초래해 상품성을 크게 떨어뜨릴 수 있다 (Farh et al., 2018; Luo et al., 2025). 반면, 질소 결핍 시에는 GATA 전사인자 등 관련 유전자 발현의 변화와 함께 생육이 억제되므로 (Liang et al., 2024), 결국 인삼 재배에 있어 적정 수준의 질소 관리는 생산성 확보를 위한 필수 선결 과제라 할 수 있다.
그러나 이러한 중요성에도 불구하고, 인삼의 질소 관련 기초 연구는 여전히 부족한 실정이다. 최근 모델 식물을 중심으로 질소 수송체 (NRT) 유전자의 발현과 질소 이용 효율 간의 상관관계가 활발히 구명되고 있으나 (Hu et al., 2015; Li et al., 2021), 아쉽게도 인삼에서는 사이토카이닌이나 지베렐린 등의 호르몬 신호 전달과 뿌리 비대 간의 관계 연구에 비해 질소 공급 형태와 그에 따른 분자생물학적 기작 연구는 상대적으로 미흡한 상황이다 (Hong et al., 2021; Geem et al., 2024).
국외의 경우, 질소, 인, 칼륨 비료를 복합 시비했을 때 3년생 인삼의 생육과 발달을 전반적으로 촉진 시켰으며, 특히 질소 50 g/㎡, 인 15 g/㎡, 칼륨 60 g/㎡ 처리 시 인삼 근경 (rhizome) 생체중과 진세노사이드 함량을 가장 증가시켰다는 보고 (Sun et al., 2022) 등 질소와 관련한 다양한 연구가 이루어지고 있다.
한편, 현재는 주로 예정지 관리 단계에서의 퇴비 투입과 같은 기비 (밑거름) 위주로 시비 관리가 이루어진다. 따라서 초기 퇴비의 과다 투입으로 인한 문제가 발생할 수 있으며, 기비만으로는 4년 이상의 장기 재배 기간 동안 작물이 필요로 하는 양분을 지속적으로 감당하기 어려우며, 특히 지상부 생장이 왕성한 시기에 양분 요구량과 토양 내 공급량 간의 불균형이 초래될 수 있다 (Lee et al., 2014). 이러한 문제로 인해 생육 기간 중 적절한 시기의 질소 추비 (Top dressing) 필요성이 대두되고 있으나, 최적 비료의 종류와 시비량에 대한 연구는 여전히 초기 단계에 머물러 있다.
요소 (Urea)는 질소 함량이 46%로 높아 경제적이며, 시비 초기 비이온성 (CO(NH2)2) 형태로 존재해 이온성 비료보다 염류·삼투 스트레스 위험이 상대적으로 낮다. 또한 뿌리로 흡수되거나 우레아제 (Urease)에 의해 가수분해되어 식물이 이용 가능한 질소원으로 동화된다 (Witte, 2011). 토양에서 암모늄태·질산태로 비교적 서서히 전환돼 생육 기간이 긴 작물에서 초기 스트레스를 완화하면서 지속 공급에 유리할 수 있다. 다만, 현행 인삼 재배 현장에서는 염류 장해에 대한 우려뿐만 아니라, 인삼산업법에 기반한 엄격한 안전성 관리 규정으로 인해 화학 비료의 사용이 제한되고 있으며, 대부분 유기질 퇴비에 의존하고 있는 실정이다. 그러나 유기질 비료는 분해 속도와 무기화 과정을 인위적으로 정밀하게 제어하기 어렵다는 특성이 있어, 인삼의 생육 단계별 정확한 양분 요구도와 생리적 임계점을 명확히 구명하는 데에는 근본적인 한계가 따른다. 이러한 기초 데이터의 부재는 향후 데이터 기반의 스마트 정밀 농업 실현과 생산성 증대를 어렵게 만드는 요인이 될 수 있다.
이에 본 연구는 요소 처리 시 인삼의 생장 특성과 품질을 조사하고 앞서 언급한 연구의 공백을 메우기 위해 Real-time qPCR을 이용한 질소 대사 및 스트레스 반응 관련 유전자들의 발현 양상을 심층 분석하였다. 이를 통해 인삼의 지하부 2차 비대 생장 기작을 해석하고, 인삼 생산성 효율을 향상시키기 위한 정밀 양분 관리 모델 수립을 위한 기초자료를 마련하고자 한다.
재료 및 방법
1. 식물 재료 및 재배 환경
2년생 인삼 포트 실험은 인삼특작부 인삼 환경조절온실에서 실시하였다. 온실 내부 환경은 냉·난방기 (PNW290PF9FR, LG, Korea)를 이용하여 제어하였으며, 설정 온도는 22℃로 하고 실험 기간 동안 20-24℃ 범위로 유지되도록 관리하였다. 흑색 차광망을 설치하여 광 투과율을 10-15%로 조절하였다. 재료는 3년생 인삼 (Panax ginseng C.A. Meyer)을 사용하였으며, 개체당 평균 무게 1.2 ± 0.2 g로 선별하여 사용하였다. 플라스틱 포트 (내경 49 × 33 × 31 ㎝)에 인삼용 상토 (황금뿌리, ㈜농경, Korea)를 높이 24 ㎝까지 채운 후 인삼을 이식하여 재배하였으며, 이식 2주 후부터 균일하게 생육된 개체를 선별하여 실험에 사용하였다. 실험은 1월부터 7월까지 약 26주간 진행되었다.
포장에서 수행한 실증 실험은 인삼특작부 경사식 해가림 시설이 설치된 인삼 재배 포장에서 수행되었다. 재래종 인삼 종자를 2022년 11월 칸 (1.62 ㎡)당 108–135립 재식밀도로 직파하였으며, 2025년에 3년생이 된 인삼을 실험 재료로 사용하였다. 이후 인삼 재배법을 참고하여 (RDA, 2021)으로 관리하였다. 실험 기간은 7월부터 10월까지 약 12주간 진행되었다. 본 실험 수행에 앞서 질소 처리 전 온실 및 포장 토양의 이화학적 특성을 조사한 결과는 Table 1과 같다.
2. 질소 추비 처리
본 실험에 사용된 질소 급원은 요소 (Urea, N 46%)를 이용하였다. 포트 시험의 처리 수준은 질소 성분량을 기준으로 무처리구 (Control, C0), 저농도 (2.5 ㎏/10a, N1), 중농도 (5.0 ㎏/10a, N2), 고농도 (10.0 ㎏/10a, N3)의 4수준으로 설정하였다. 질소 처리는 2년생 인삼 이식 후 활착이 완료된 2주 차부터 시작하여 4주 간격으로 총 6회 실시하였다. 처리 방법은 요소를 100 ℓ 당 35.15 (N1), 70.30 (N2) 140.60 (N3) g 녹여서 포트당 1 ℓ씩 토양 표면에 충분히 관주 (Soil drenching)하여 근권 내에 양분이 고르게 분포되도록 하였다.
포장 실험의 질소 처리는 지상부 생육이 안정화된 전엽기 이후 14주가 경과한 시점에 개시하였다. 무처리구 (Mock)를 대조구로 하여, 질소 시비량에 따라 5.0 ㎏/10a (A) 처리구와 10.0 ㎏/10a (B, C) 처리구로 구분하였다. 질소 이용 효율을 검증하기 위해 관주 횟수와 1회 요소 농도를 다르게 설정하였다. 관주 효율과 농도 균일성을 위해 두 가지 농도의 저장 용액 (Stock solution)을 100 ℓ 단위로 제조하여 사용하였다. 표준 농도 용액 (Solution I)은 100 ℓ 물에 요소 (Urea) 195.7 g을 용해하여 제조하였으며, 고농도 용액 (Solution II)은 100 ℓ 물에 요소 391.3 g을 용해하여 제조하였다. 모든 관주량은 구획 면적 (1.62 ㎡)당 3 ℓ로 고정하였다. 처리구 A (5.0 ㎏/10a)는 Solution I을 4주 간격으로 3회, 처리구 B (10.0 ㎏/10a)는 동일한 Solution I을 사용하되 관주 빈도를 2주 간격 6회로 늘려 총 질소 투입량을 조절하였다. 고농도 처리구 C (10.0 ㎏/10a)는 Solution II를 4주 간격으로 3회 관주로 1회 처리 농도를 높였다. 본 실험에 적용된 각 처리구별 구체적인 관주 용액의 조성 및 실험 조건은 Table 2와 같다.
3. 생육 특성 및 물성 조사
인삼의 생육 특성 조사는 농촌진흥청의 농업과학기술 연구조사분석기준 (NIAST, 2012)을 참고하여 수행하였다. 시기별 생육 변화를 정밀하게 분석하기 위해, 각 처리구당 건전한 개체 15주를 무작위로 선발 (Random sampling)하여 조사 시료로 활용하였다.
온실 실험은 질소 처리에 따른 생육 단계별 반응을 모니터링하기 위해, 처리 개시 후 4주 간격으로 총 6회 (6, 10, 14, 18, 22, 26주 차)에 걸쳐 조사를 수행하였다. 지상부 생육은 초장, 경장, 경직경, 엽장 및 엽폭을 조사하였다. 초장 (Plant height)은 뇌두 상단부터 잎의 가장 높은 끝부분까지의 수직 길이를 측정하였으며, 경장 (Stem length) 은 뇌두 상단부터 잎자루 (Petiole)가 분지되는 지점까지의 길이를 측정하여 구분하였다. 엽장 (Leaf length)과 엽폭 (Leaf width)은 개체당 가장 큰 잎을 기준으로 하였고, 줄기의 굵기인 경직경 (Stem diameter)은 디지털 버니어 캘리퍼스 (CD-15APX, Mitutoyo, Japan)를 이용하여 정밀 측정하였다. 지하부 생육은 뇌두 하단부터 주근 (Main root) 끝까지의 근장 (Root length)과 주근의 가장 굵은 부위인 근직경 (Root diameter)을 측정하였다. 식물체의 바이오매스량은 정밀 전자저울 (SPX2202KR, OHAUS, USA; Max 2200 g, d = 0.01 g)을 사용하여 지상부와 지하부의 생체중 (Fresh weight)을 각각 0.01 g 단위로 측정하여 비교 분석하였다.
포장 실험은 인삼의 비대 생장이 왕성해지는 생육 중·후반기의 특성을 규명하기 위해 18, 22, 26주 차에 시료를 굴취하여 조사를 진행하였다. 기본적인 지상부 및 지하부 생육 형질 (초장, 근장, 근중 등)은 온실 실험과 동일한 정밀 계측 장비를 사용하여 측정하였다. 특히, 질소 추비 수준이 인삼 뿌리의 조직감 및 세포벽 발달에 미치는 영향을 분석하기 위해 물성 (Texture) 분석을 추가로 수행하였다. 18, 22, 26주 차에 수확한 뿌리의 주근 중앙부를 대상으로 물성측정기 (TX-700, Lamy Rheology, France)를 이용하여 경도 (Hardness)를 측정하였다.
4. Total RNA 분리 및 정량적 실시간 PCR (qRT-PCR) 분석
인삼 뿌리 조직 (100 ㎎)으로부터 Total RNA는 IQeasy™ plus Plant RNA Extraction Mini Kit (iNtRON Biotechnology, Seongnam, Korea)의 Protocol B에 따라 추출하였다. 추출된 RNA의 농도와 순도는 NanoDrop 2000 (Thermo Scientific, Wilmington, DE, USA)을 이용하여 A260/A280 비율 (1.8–2.0)로 확인하였으며, 1.0% agarose gel 전기영동을 통해 18S 및 28S rRNA 밴드의 선명도를 확인하여 RNA의 안정성을 검증하였다.
cDNA 합성은 추출된 Total RNA 0.5 ㎍ 을 주형으로 iScript™ cDNA Synthesis Kit (Bio-Rad Laboratories, Inc., Hercules, CA, USA)를 사용하여 수행하였다. 반응액은 Total RNA 0.5 ㎍, 5× iScript Reaction Mix 4 ㎕, iScript Reverse Transcriptase 1 ㎕, 그리고 Nuclease-free water를 혼합하여 최종 부피 20 ㎕로 조성하였다. 역전사 반응은 C1000 Touch™ Thermal Cycler (Bio-Rad)를 이용하여 25℃에서 5분, 46℃에서 20분간 반응시킨 후, 95℃에서 1분간 처리하여 효소를 불활성화하였다.
유전자 발현 분석은 CFX96 Real-Time PCR Detection System (Bio-Rad)과 SsoAdvanced Universal SYBR Green Supermix (Bio-Rad)를 이용하여 수행하였다. PCR 반응액은 cDNA 1 ㎕, 10 pmol의 정방향 및 역방향 프라이머 각 1 ㎕, 그리고 2× Supermix 10 ㎕를 포함하여 최종 부피 20 ㎕로 조성하였다. 증폭 조건은 95℃에서 3분간 예비 변성 후, 95℃ 10초, 60℃ 10초, 72℃ 15초의 과정을 45회 반복하였으며, 반응 종료 후 65℃에서 95℃까지 0.5℃씩 상승시키며 융해 곡선 (Melt curve)을 분석하여 비특이적 증폭 여부를 확인하였다. 모든 실험은 3 반복으로 수행되었으며, 각 유전자의 상대적 발현량은 PgActin을 내부 표준 유전자(internal control)로 보정하여 2-ΔΔCt 방법 (Livak and Schmittgen, 2001)으로 산출하였다. 본 연구에 사용된 프라이머 염기서열은 Table 3에 제시하였다 (Hong et al., 2022; Geem et al., 2023; Geem et al., 2024).
4. 토양 화학성 분석
토양 시료는 온실 재배구의 경우 이식 후 2, 6, 10, 14, 18, 22, 26주 차에, 포장 재배구는 14, 18, 22, 26주 차에 각각 식물체 주위의 근권 토양 (Rhizosphere soil)을 채취하여 분석하였다. 채취된 시료는 그늘에서 일주일간 풍건 (Air-drying)한 뒤 2 ㎜ 체를 통과시켜 균질화하였고, 이 중 일부는 분쇄기 (SFM-555SP, SHINIL Electronics Co., Ltd., Cheonan, Korea)를 사용하여 미세 분말 형태로 조제하였다.
토양 이화학적 특성 분석은 농촌진흥청 토양화학분석법 (NIAST, 2000)에 준하여 실시하였다. 먼저 질산태 질소 (NO3-N)함량을 조사하기 위해 2 M KCl 용액으로 침출하고, 자동분석기 (Skalar San++, Skalar Analytical, Breda, Netherlands)를 이용한 Hydrazine 환원법으로 분석하였다. 토양 산도 (pH)와 전기전도도 (EC)는 풍건 토양과 증류수를 1:5 (w/v) 비율로 혼합하여 30분간 진탕한 후 각각의 측정기로 확인하였다. 유효인산 (Av.P2O5)은 Lancaster법으로 침출하여 분광광도계(720 ㎚)로 비색 정량하였으며, 치환성 양이온은 1 N NH4OAc (pH 7.0) 용액으로 침출 후 유도결합플라즈마 분광광도계 (ICP-OES; Integra XMP, GBC Scientific Equipment, Braeside, Australia)를 사용하여 분석하였다. 유기물 (OM) 함량은 Tyurin 법을 적용하여 측정하였다.
5. 통계 처리
실험 결과의 통계 분석은 R 프로그램 (Version 4.5.2, The R Foundation for Statistical Computing, Vienna, Austria)을 이용하여 수행하였다. 모든 데이터는 평균값 (Mean)과 표준편차 (Standard Deviation, SD)로 나타내었으며, 처리구 간의 유의성 검정은 분산분석 (Analysis of Variance, ANOVA)을 실시한 후, Duncan's Multiple Range Test (DMRT)를 이용하여 5% 유의 수준 (p < 0.05)에서 평균 간의 차이를 비교 분석하였다.
결과 및 고찰
1. 온실 및 포장 조건에서 질소 처리 및 분시 방법에 따른 인삼의 생육과 뿌리 물성 변화
온실 조건에서 요소 (Urea) 관주 처리에 따른 3년생 인삼의 26주간 생육 변화를 조사한 결과, 고온기인 18주 차를 기점으로 모든 처리구에서 지상부의 생체 활성이 감소하는 경향을 보였으나, 질소 처리 농도에 따라 그 감소의 폭과 시기에는 다소 차이가 있음이 관찰되었다. 무처리구 (C0)는 잎의 황화와 줄기 위축 등 노화 (Senescence) 징후가 비교적 빠르게 나타난 반면, 고농도 질소 처리구 (N3)는 생육 후기까지 상대적으로 양호한 생육 상태를 유지하는 양상을 나타내었다.
지상부의 형태적 변화를 구체적으로 살펴보면, 무처리구의 초장 (Plant height)은 18주 차에 28.50 ㎝로 정점에 도달한 후 감소세로 전환되어 26주 차에는 25.90 ㎝를 기록하였다. 이에 비해 저농도 (N1)와 중농도 (N2) 처리구는 무처리구 대비 노화 진행 속도가 지연되는 중간적인 양상을 나타내었다. 특히 N1과 N2 처리구는 줄기 직경과 엽면적 등 주요 형질에서 무처리구보다는 우수하고 N3 처리구보다는 다소 낮은 수치를 기록하여, 질소 공급량이 엽록소 유지와 광합성 효율에 비례적인 영향을 미침을 입증하였다. N3 처리구는 22주 차에 29.37 ㎝로 최대 생장을 보였으며, 이후 26주 차에도 27.46 ㎝를 유지하여 무처리구 대비 생육 기간이 연장되고 감소 폭 또한 완화된 경향을 보였다 (Fig. 1A). 줄기의 길이 (Stem length) 또한 무처리구는 26주 차에 13.88 ㎝로 급격히 위축된 반면, N3 처리구는 15.90 ㎝ 수준을 유지하였다 (Fig. 1B).
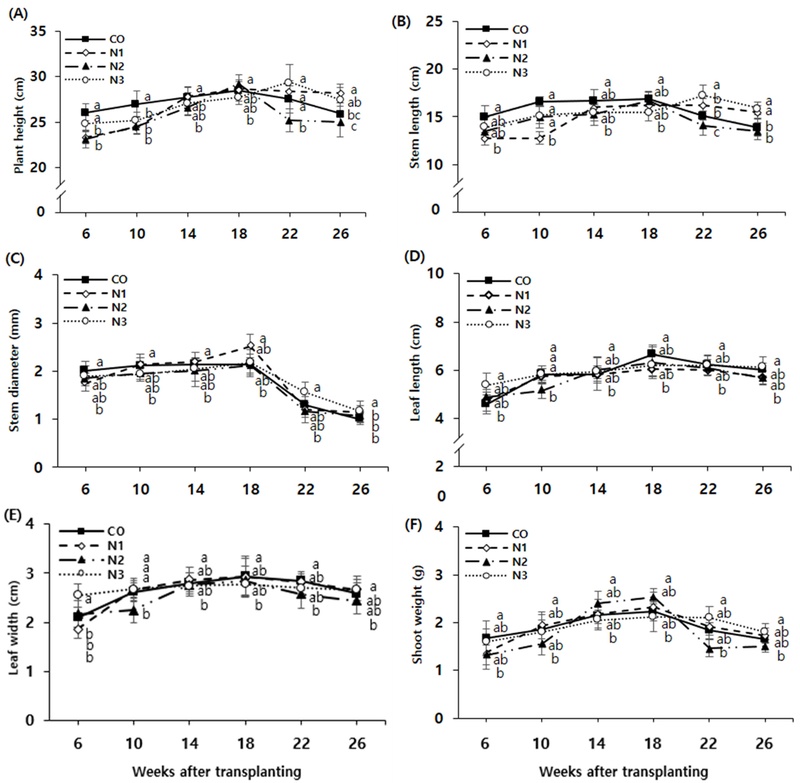
Time-course changes in shoot growth characteristics of 3-year-old ginseng in a greenhouse condition affected by nitrogen concentrations.Graphs show the changes in plant height (A), stem length (B), stem diameter (C), leaf length (D), leaf width (E), and shoot fresh weight (F) during the cultivation period. Measurements were taken at 4-week intervals from 6 to 26 weeks after transplanting under different urea concentrations: C0 (Control, 0 ㎏/10a), N1 (2.5 ㎏/10a), N2 (5.0 ㎏/10a), and N3 (10.0 ㎏/10a). Data are presented as means ± SD (n=15). Different lowercase letters indicate significant differences at p < 0.05 (Duncan’s multiple range test).
특히 줄기의 굵기를 나타내는 경직경 (Stem diameter)의 변화는 질소 공급이 조직의 구조적 유지에 긍정적인 영향을 미칠 수 있음을 시사한다. 생육 후기 건조 및 노화로 인해 줄기가 가늘어지는 현상이 관찰되었는데, 무처리구가 26주 차에 1.00 ㎜까지 감소한 것에 비해 N3 처리구는 1.16 ㎜를 나타내어 상대적으로 굵은 상태를 유지하였다 (Fig. 1C). 잎의 형질인 엽장 (Leaf length)과 엽폭 (Leaf width) 역시 26주 차 기준 N3 처리구가 각각 6.12 ㎝와 2.66 ㎝를 기록하여, 무처리구의 6.03 ㎝와 2.58 ㎝보다 다소 높은 수치를 보여주었다 (Fig. 1D, 1E).
이러한 지상부 기관들의 형질 유지는 전체적인 바이오매스의 변화로도 확인되었다. 지상부 생체중 (Shoot weight)을 측정한 결과, 무처리구는 18주 차 2.24 g 대비 26주 차에 1.66 g으로 뚜렷한 무게 감소한 반면, N1과 N2 처리구는 감소폭이 둔화되는 양상을 보였다. 하지만 N1과 N2 처리구는 생육 후기 바이오매스 유지 면에서 N3 처리구에는 미치지 못하였다. N3 처리구는 18주 차 2.12 g, 22주 차 2.10 g으로 높은 중량을 유지하였으며, 최종 26주 차에도 1.81 g을 기록하며 그 감소세가 비교적 둔화된 양상을 나타내었다 (Fig. 1F). 이는 적절한 질소 공급이 엽록소의 분해를 억제하고 광합성 기관의 기능적 수명을 연장시킴으로써, 생육 후기 지상부의 노화를 완화하는 데 기여한 것으로 판단된다 (Sakuraba, 2022).
이러한 지상부의 생육 활성 유지는 지하부인 뿌리의 생장에도 긍정적인 영향을 미친 것으로 보이며, 이를 온실과 포장 조건으로 나누어 비교 분석하였다. 온실 조건에서 뿌리의 길이 생장 (Root length)을 살펴보면, N3 처리구는 26주 차에 22.24 ㎝를 기록하여 무처리구인 24.28 ㎝와 유사하거나 다소 짧은 경향을 보였다 (Fig. 2A). 반면, 해가림 시설 포장 조건에서는 질소 분시 처리구 (B)가 28.76 ㎝를 기록하여 무처리구 (Mock)의 22.73 ㎝ 대비 뚜렷한 신장 효과를 나타내었다 (Fig. 2B). 이러한 상반된 결과는 온실 실험에 사용된 포트의 물리적 공간 제약이 뿌리의 수직 신장을 구조적으로 제한했기 때문으로 판단된다. 깊이가 확보된 포장 조건에서는 질소 공급에 따른 뿌리 신장 잠재력이 온전히 발현되었으나, 온실에서는 공간적 한계로 인해 길이 생장이 억제된 것으로 보인다.
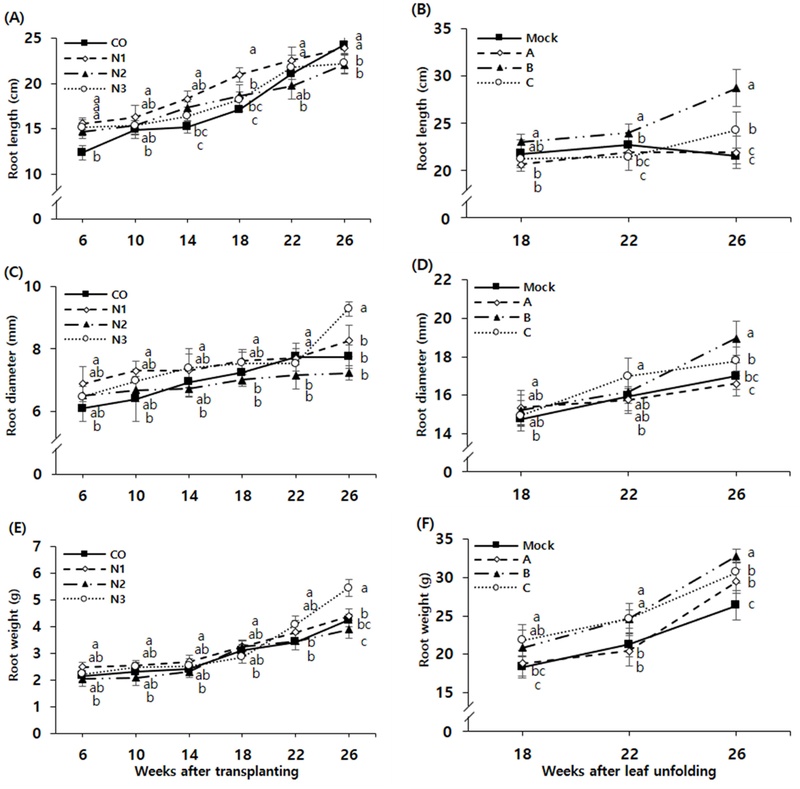
Effects of nitrogen treatments on the root growth characteristics of 3-year-old ginseng in greenhouse (A, C, E) and field (B, D, F) conditions.Graphs show the changes in root length (A, B), root diameter (C, D), and root fresh weight (E, F) during the cultivation period. For the greenhouse experiment (A, C, E), measurements were taken at 4-week intervals from 6 to 26 weeks after transplanting under different urea concentrations (C0, N1, N2, and N3). For the field experiment (B, D, F), measurements were taken at 4-week intervals from 18 to 26 weeks after leaf unfolding. Field treatments varied by total nitrogen amount and splitting frequency: Treatment A (5 ㎏, 3 times / 4 weeks), Treatment B (10 ㎏, 6 times / 2 weeks), and Treatment C (10 ㎏, 3 times / 4 weeks). The Mock group served as an untreated control. Data are presented as means ± SD (n=15). Different lowercase letters indicate significant differences at p < 0.05 (Duncan’s multiple range test).
뿌리의 굵기를 나타내는 근직경 (Root diameter)에서는 두 환경 모두에서 일관된 비대 효과가 확인되었다. 온실 조건의 N3 처리구는 26주 차 근직경이 9.28 ㎜로 무처리구의 7.75 ㎜ 대비 약 19.7% 높게 측정되었으며 (Fig. 2C), 해가림 시설 조건의 B 처리구 또한 18.94 ㎜를 기록하여 무처리구인 16.98 ㎜보다 약 11.5% 굵게 발달하였다 (Fig. 2D). 이는 온실의 포트가 가지는 물리적 공간 제약이 뿌리의 신장을 억제함에 따라, 질소 공급에 의한 생육 잠재력이 길이 생장보다는 비대 생장으로 집중되었을 것으로 추측된다. 또한 해가림 시설 B 처리구에서 나타난 우수한 생육 지표들은 소량의 비료를 자주 공급하는 분시 처리가 근권 내 질소 농도를 안정적으로 유지시켜 뿌리의 흡수 효율을 높이고, 신장과 비대 생장을 동시에 촉진하는 효과적인 재배 전략이 될 수 있음을 시사한다 (Seong et al., 2004). 이러한 뿌리생장은 최종적인 수량성 지표인 근중 (Root weight)의 증가로 확인되었다. 온실 조건에서 26주 차 기준 무처리구 (C0)는 4.24 g을 기록한 반면, 저농도 (N1)는 4.73 g, 중농도 (N2)는 5.01 g을 기록하여 질소 농도가 높아질수록 뿌리 비대가 순차적으로 촉진됨을 확인하였다. 최종적으로 고농도 (N3)는 5.45 g으로 가장 높은 수량성을 나타내었다 (Fig. 2E). 한편, 포장 실험에서는 시비량과 분시 방법에 따른 차이가 더욱 명확하게 관찰되었다. 저농도 처리구인 A (5.0 ㎏/10a)의 근중은 29.45 g을 기록하여 무처리구 근중 26.36 g 대비 약 11.7% 증수되는 경향을 보였다. 반면, 고농도 (10.0 ㎏/10a) 처리구인 B와 C는 각각 32.75 g과 30.63 g을 기록하여 무처리구 대비 약 24.2% 와 16.2%의 뚜렷한 증수 효과를 나타내었다. 특히, 동일한 총량의 질소를 공급하였음에도 불구하고 2주 간격으로 분시한 B 처리구가 4주 간격인 C 처리구보다 더 높은 수량성을 확보하여, 질소의 절대량뿐만 아니라 공급 주기 또한 뿌리 비대에 중요한 요인임이 확인되었다 (Fig. 2F).
결과적으로 온실 실험에서는 물리적 공간 제약이, 포장 실험에서는 환경적 변수가 존재했음에도 불구하고, 두 실험 모두에서 질소 공급량이 증가할수록 근비대와 근중이 뚜렷하게 증가하는 공통된 결과를 보였다. 따라서 재배 환경의 차이가 있더라도 적절한 수준의 질소 공급은 인삼 뿌리의 2차 생장 (Secondary growth)을 촉진하는 주요 요인으로 작용할 가능성이 높은 것으로 판단된다.
외형적 생장뿐만 아니라, 뿌리 내부 조직의 질적 특성에 미치는 영향을 구명하기 위해 시기별 인삼 뿌리 경도 (Hardness)를 측정하였다 (Fig. 3). 포장에서 시험한 26주 차의 뿌리 경도를 측정한 결과, 고농도 질소 처리구인 B와 C 처리구는 각각 9.65 N과 9.46 N을 기록하여 무처리구 (Mock)인 8.58 N 대비 10% 이상 유의하게 증가하는 양상을 나타내었다 (Fig. 3). 식물 조직의 물리적 경도와 기계적 강도는 1차 및 2차 세포벽을 구성하는 셀룰로오스 미세섬유와 다당류의 구조적 결합에 의해 결정된다 (Cosgrove and Jarvis, 2012). 특히 요소와 같은 암모늄태 질소 (NH4+)의 공급은 뿌리 조직 내에서 리그닌 생합성 경로를 자극하여 2차 세포벽의 축적과 목질화 (Lignification)를 유도하는 것으로 알려져 있다 (Yang et al., 2021). 이는 질소 추비가 단순히 수분 흡수에 의한 부피 팽창을 넘어, 내부 조직의 충실도를 높임으로써 상품성을 개선하는 데 긍정적인 영향을 미칠 수 있음을 시사한다.
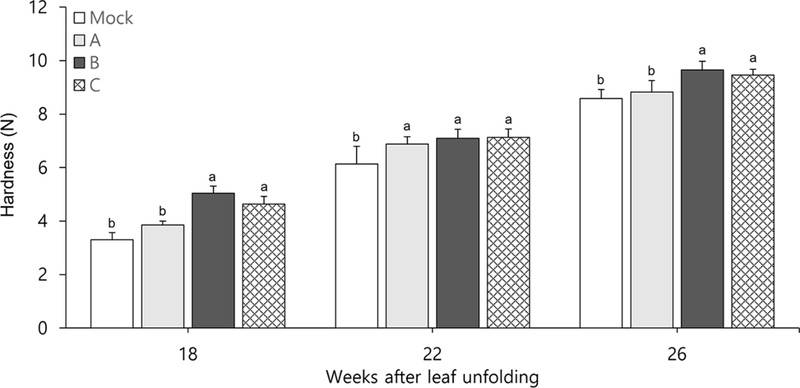
Changes in root physical properties (hardness) of Panax ginseng under different nitrogen fertilization methods in a field condition.Measurements were taken at 4-week intervals from 18 to 26 weeks after leaf unfolding. (Mock) Control (0 ㎏/10a); (A) Low nitrogen level (Total 5 ㎏10a); (B) High nitrogen level (Total 10 ㎏/10a) with 6-split applications at 2-week intervals; (C) High nitrogen level (Total 10 ㎏/10a) with 3-split applications at 4-week intervals. Data represent the mean ± SD (n=5). Different lowercase letters indicate significant differences at p < 0.05 by Duncan's multiple range test.
인삼 뿌리의 경도 향상은 조직의 치밀도를 보완하여 수확 및 세척 과정의 물리적 손상을 완화하고 상품화율을 높이는 데 기여할 것으로 보인다. 또한, 강화된 조직감은 저장 중 부패 저항성을 높여 신선도 유지에 도움을 줄 수 있으며, 특히 홍삼 가공 시 내공·내백 발생을 억제하여 등급 판정률을 향상시키는 요인이 될 것으로 기대된다. 결과적으로 이러한 물리적 특성의 개선은 수삼의 유통 경쟁력과 가공 부가가치를 높여 농가 소득 증대에 긍정적으로 작용할 것으로 사료된다.
본 연구 결과를 종합해 볼 때, 10 ㎏/10a 수준의 질소 추비는 지상부의 노화를 지연시켜 생육 기간을 확보함으로써 지하부로의 양분 축적을 극대화하였다. 특히, 2주 간격의 분시 (Split application) 처리는 앞서 확인된 생산성 증가 뿐만 아니라, 조직의 물성 강화에도 기여함을 확인하였다. 결론적으로, 전엽기 이후 생육 단계에 맞춘 주기적인 질소 공급은 인삼의 수량과 품질을 동시에 확보할 수 있는 효과적인 정밀 재배 기술로 판단된다.
2. 질소 처리 농도에 따른 세포벽 관련 유전자 발현 변화
앞선 생육 및 물성 조사에서 고농도 질소 처리구인 N3와 B, C 그룹은 대조구 대비 뿌리의 비대 생장뿐만 아니라 조직의 물리적 경도가 증가하는 경향을 보였다. 이러한 표현형의 변화가 분자 수준에서 어떠한 기작과 연관되어 있는지 알아보기 위해, 질소 신호 전달 및 세포벽 조절 핵심 유전자들의 발현 양상을 시간 경과에 따라 분석하였다 (Fig. 4).
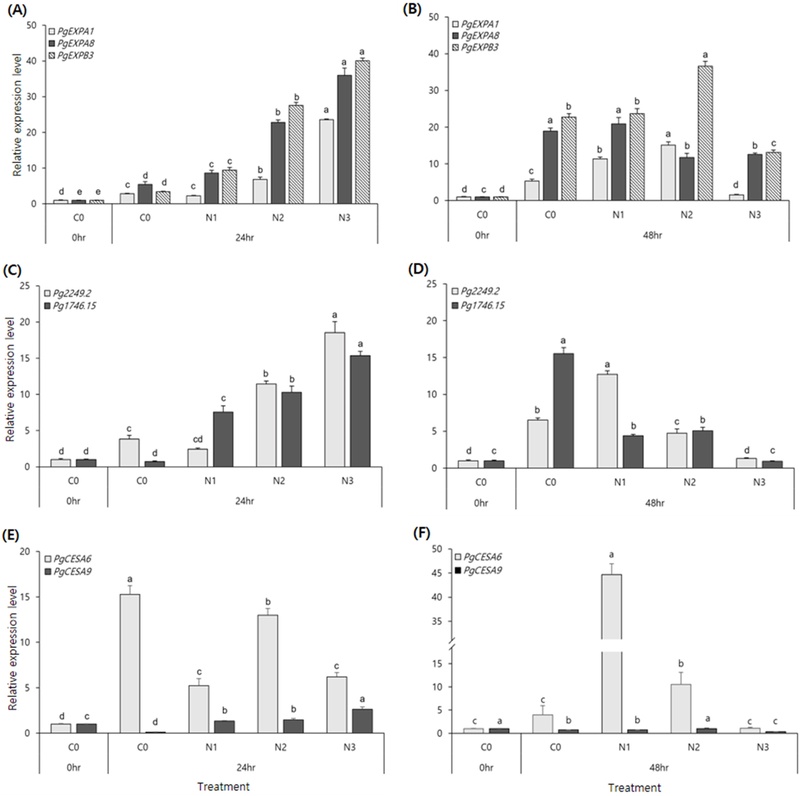
Relative expression levels of cell wall-related genes in Panax ginseng roots under different nitrogen concentrations.(A, B) Expression of Expansin genes (PgEXPA1, PgEXPA8, PgEXPB3) at 24 h (A) and 48 h (B) after treatment. (C, D) Expression of secondary cell wall biogenesis-related genes (Pg1746.15, Pg2249.2) at 24 h (C) and 48 h (D) after treatment. (E, F) Expression of cellulose synthase genes (PgCESA6, PgCESA9) at 24 h (E) and 48 h (F) after treatment. The expression levels were normalized to Actin and are presented as fold changes relative to the control (0 h). Data represent the mean ± SD (n = 3). Different letters indicate significant differences at p < 0.05 by Duncan's multiple range test. C0, Control; N1, 2.5 ㎏/10a; N2, 5.0 ㎏/10a; N3, 10.0 ㎏/10a.
일반적으로 식물은 토양 내 질산태 질소를 감지하고 이를 성장 신호로 변환하는 시스템을 보유하고 있는 것으로 알려져 있다. 모델 식물 연구에 따르면, 외부 질소 농도는 NRT1.1 센서에 의해 인지될 수 있으며, 이 신호는 SnRK2 계열 키나아제가 관여하는 조절 모듈을 통해 통합되어 전달되는 것으로 보고되었다 (Mu et al., 2025). 질소가 충분히 공급될 경우 성장 억제 인자인 SnRK2의 활성이 저해되고, 이에 따라 전사 인자인 NLP7이 활성화되어 핵 내로 이동할 가능성이 있다. 활성화된 NLP7은 하위의 NAC과 같은 2차 전사인자들을 발현 유도하는 조절 네트워크를 형성하는 것으로 추정된다 (Konishi and Yanagisawa, 2013; Marchive et al., 2013). 최근 인삼에서도 PgNAC41-2가 이러한 세포벽 합성 조절에 관여할 가능성이 제기된 바 있다 (Liu et al., 2023). 본 연구에서는 질소가 NLP7과 NAC 전사인자를 거쳐 순차적으로 신호를 전달하여 최종적으로 세포벽 합성을 조절한다는 일련의 과정이 인삼 뿌리의 비대 생장 과정에서도 유사하게 작동할 것이라는 가설을 세웠다. 이에 본 실험에서는 이러한 신호 전달 경로의 하위 단계에 위치하며 실질적인 물리적 변화를 담당하는 것으로 알려진 세포벽 이완 및 합성 유전자군의 발현 변화를 추적하여, 앞서 관찰된 뿌리 조직의 변화를 분자생물학적으로 해석하고자 하였다.
본 연구에서 세포벽 완화 단백질인 Expansin 유전자군 (PgEXPA1, PgEXPA8, PgEXPB3)의 발현을 분석한 결과, 질소 처리는 세포 신장의 즉각적인 신호로 작용하였다 (Krouk et al., 2010; Medici and Krouk, 2014). 특히 처리 후 24시간에 N3 처리구는 PgEXPB3 유전자를 대조구 대비 약 34배, PgEXPA8 유전자를 약 10배 이상 높게 발현시키며 타 처리구와 뚜렷한 차이를 보였다 (Fig. 4A). 이는 고농도의 질소 자극이 뿌리 세포벽의 물리적 장벽을 단시간에 큰 폭으로 이완시켜, 앞서 관찰된 뿌리 비대 생장을 위한 공간을 조기에 확보했음을 시사한다 (Cho and Cosgrove, 2000). 초기 24시간의 높은 발현율에 비해 48시간째의 발현량이 감소한 것은, 이미 구축된 세포 팽창 기반을 바탕으로 대사 효율을 최적화하려는 기작이 작용이 작용한 결과로 풀이된다. 즉, 세포가 항상성을 유지하기 위해 발현 수준을 스스로 조절했을 가능성이 크다.
특히 이러한 유전자 분석 결과는 앞서 관찰된 조직 경도 증가를 뒷받침하는 분자적 증거가 된다. 일반적인 세포 신장은 조직을 연하게 할 수 있으나, 본 연구에서의 질소 처리는 세포벽 이완과 동시에 구조적 강화를 위한 2차 세포벽 형성 시스템을 강력하게 활성화시키는 것으로 나타났다. 2차 세포벽 생합성 관련 전사체인 Pg1746.15와 Pg2249.2는 처리 후 24시간에 N3 처리구에서 각각 약 15배, 18배의 높은 발현을 보였는데 (Fig. 4C), 이는 질소 신호에 의해 활성화된 전사인자들이 세포벽 합성 유전자군을 자극한 결과로 추측되며, 인삼에서 PgNAC41-2와 같은 NAC 전사인자가 2차 대사 및 성장을 긍정적으로 조절한다는 선행 연구와 일치하는 결과이다 (Liu et al., 2023).
특히, 세포벽의 주요 골격이자 물리적 강도를 결정짓는 셀룰로오스 합성 유전자 PgCESA6 역시 N3 처리구에서 대조구 대비 약 24배 높게 발현되었다 (Fig. 4E). 이는 질소 공급이 단순히 세포를 부풀리는 데 그치지 않고, 확장된 세포벽에 셀룰로오스와 리그닌의 축적을 유도하여 조직의 치밀도를 높였음을 의미한다 (Stork et al., 2010).
결론적으로, 적절한 질소 공급은 Expansin 발현을 통한 부피 팽창과 PgCESA 발현을 통한 조직 경화를 시차를 두고 정교하게 조절하는 것으로 판단된다. 이러한 분자 기작은 질소 시비가 인삼 뿌리를 무르게 한다는 기존의 통념과 달리, 실제로는 세포벽 구조를 강화하여 내공 발생을 억제하고 고품질의 단단한 뿌리를 생산하게 하는 생리학적 원동력임을 시사한다.
3. 질소 처리 수준 및 분시 방법에 따른 근권 토양의 화학성 변화
인삼 재배 기간 중 질소 공급 수준과 분시 방법이 근권 토양의 화학적 특성과 양분 가용성에 미치는 영향을 구명하기 위해 온실과 포장 조건에서 시기별 토양 변화를 분석하였다. 온실 실험 결과, 질소 시비량이 증가할수록 토양 산도 (pH)는 유의하게 감소하는 반면 전기전도도 (EC)와 질산태 질소 (NO3-N) 함량은 증가하는 경향을 보였다 (Table 4). 26주 차 기준 N3 처리구의 pH는 5.55로 대조구 (5.73)보다 낮게 나타났는데, 이는 투입된 요소 비료가 토양 내에서 가수분해 및 질산화 (Nitrification) 과정을 거치며 수소 이온 (H+)을 방출하여 토양 산성화를 가속화시켰기 때문이다 (Barak et al., 1997; Guo et al., 2010). N3 처리구는 높은 EC와 NO3-N (20.38 ㎎/㎏) 함량을 유지하여 생육 후기까지 인삼의 양분 요구도를 충족시킨 것으로 판단된다.

Effect of nitrogen concentration levels on chemical properties of ginseng rhizosphere soil in greenhouse cultivation.
포장 실험 (Table 5)에서는 질소 비료 (10.0 ㎏/10a)를 동일한 양 투입하고 분시 횟수를 달리한 C 처리구 (3회 분시)와 B 처리구 (6회 분시) 간에 양분의 유효도 와 용탈 (Leaching) 양상에 뚜렷한 차이가 확인되었으며, 특히 토양 pH와 유효인산, 그리고 질산태 질소와 치환성 양이온 간의 상호작용이 처리구별 생육 차이를 설명하는 주요 요인으로 작용하였다. 저농도 질소 처리구인 A의 경우, 18주 및 22주 차 유효인산 (Av.P2O5) 함량이 B 처리구보다 낮게 측정되었다. 저농도 질소 처리구인 A는 18주 차부터 26주 차까지 pH 7.14 이상의 알칼리성 환경이 지속되었고, 이로 인해 유효인산 함량은 18주 차 525.04 ㎎/㎏에서 수확기 484.91 ㎎/㎏으로 점진적으로 감소하였다. 가용성 인산이 칼슘 (Ca2+) 이온과 결합하여 불용성인 인산칼슘 (Ca3(PO4)2) 을 형성하는 화학적 불용화가 촉진되었기 때문으로 해석된다. 반면, B 처리구는 분시 처리에 따른 질산화 작용으로 토양 pH를 6.8–6.9 범위로 안정화하였다. 이는 인삼 예정지 토양 화학성의 허용범위 (pH 6.5–7.0)에 부합하는 수치로 (RDA, 2024), 토양 내 인산이 불용화되지 않고 높은 유효도를 유지하는 데 결정적인 역할을 하였다.
또한 C 처리구와 B 처리구 사이에는 질소와 치환성 칼슘 (Ex. Ca)의 동반 용탈기작이 뚜렷하게 대조를 이루었다. 3회 분시한 C 처리구는 22주 차에서 26주 차로 경과하는 동안 질산태 질소 함량이 194.57 ㎎/㎏에서 20.49 ㎎/㎏으로 급격히 줄어들었으며, 이와 동시에 치환성 칼슘 함량 역시 6.51 cmol+/㎏에서 6.00 cmol+/㎏으로 유의하게 감소하는 경향을 보였다. 이는 토양 내 음이온인 질산염 (NO3-N)이 일시에 다량으로 용탈될 때 전기적 중성을 유지하기 위해 양이온인 칼슘 (Ca2+)을 동반하여 용탈시키는 기작에 기인한 것으로 판단된다 (Qiu et al., 2014).

Changes in chemical properties of ginseng rhizosphere soil according to nitrogen split application methods and growth stages in field cultivation.
반면, 2주 간격으로 6회 분시한 B 처리구는 생육 전 기간에 걸쳐 질소 성분을 소량씩 지속적으로 공급함으로써 잉여 질산염의 용탈을 최소화하였다. 이러한 시비 관리의 효율성은 칼슘 등 필수 양이온의 동반 유실을 억제하여 수확기까지 토양 내 칼슘 함량을 6.68 cmol+/㎏ 수준으로 예정지 토양의 칼슘 성분의 허용 범위 (5.0–6.5)를 다소 상회하나 (RDA, 2024) 안정적으로 유지하였다. B 처리구에서 관찰된 높은 치환성 칼슘 (Ex. Ca)의 유지는 앞서 확인된 뿌리 물성의 증가 (Fig. 3)를 설명하는 중요한 생화학적 근거가 된다. 칼슘 (Ca2+)은 식물 세포벽에서 펙틴 (Pectin) 사슬 사이를 결합시키는 ‘가교 (Cross-linking)’ 역할을 하여 세포 간 결속력을 강화하고 조직의 붕괴를 막는 핵심 인자이다 (Hepler, 2005). B 처리구에서 관찰된 안정적인 칼슘 함량은 앞선 유전자 분석 (Fig. 4)에서 나타난 CESA6 등 일부 세포벽 성분 합성 유전자의 상향 조절과 함께 세포벽 구조 유지에 긍정적인 영향을 미쳤을 것으로 사료된다. 비록 세포벽 형성이 다양한 유전자군의 복합적인 조절을 받는 과정이나, 본 실험 결과는 칼슘의 보존과 관련 유전자의 발현 패턴이 펙틴 매트릭스 결합력 및 조직 치밀도 유지에 일정 부분 기여할 가능성을 시사한다.
즉, 소량 다회 분시는 토양의 급격한 화학적 변화를 방지하고 생육 후기까지 질소와 칼슘같이 필수 무기성분의 가용성을 높게 유지함으로써, 양적 생육 증대뿐만 아니라 질적 조직 강화를 위한 최적의 근권 환경을 조성한 것으로 판단된다. 이러한 결과는 분시 처리가 뿌리 비대 및 수량 증대에 기여한다는 도라지 연구 결과 (Seong et al., 2004)와 일치하며, 고품질 인삼 생산을 위해서는 단순한 질소 공급량을 넘어 토양 내 양이온 균형까지 고려한 정밀한 시비 전략이 필수적임을 시사한다.
본 연구를 통해 주기적인 질소 추비가 인삼의 2차 생장과 뿌리 비대를 유도하고, 같은 농도의 질소 성분이라면 분할 시비가 생육이나 토양 화학성의 변동성 측면에서 좀 더 효과적이라는 것을 확인하였다. 다만, 질소 추비에 따른 주요 약용 성분인 진세노사이드 함량 변화 분석 및 이들 간의 상관관계 구명에는 한계가 있었다. 외형적 생육 증가, 진세노사이드 함량과 어떠한 상관관계를 갖는지 구명하기 위한 정량 분석이 요구된다 (Sun et al., 2022). 또한 현행 인삼산업법에서 재배 기간 중 화학 비료의 사용은 엄격히 제한되고 있기 때문에 본 연구 결과를 토대로 추비 시 사용할 수 있는 유기물 적용 기준을 마련하고, 이를 기반으로 한 정밀 양분관리 기술을 개발하고 현장에 적용하는 추가 연구가 필요하다. 더불어 전자현미경 및 프로테오믹스 등 조직화학적 분석을 병행하여, 유전자 발현이 실제 조직 물성 강화로 실현되는 생리학적 기작을 밝히는 후속 연구가 필요하다.
Acknowledgments
본 연구는 농촌진흥청 시험연구사업(PJ017165)의 지원에 의해 이루어진 것으로 이에 감사드립니다.
References
-
Barak P, Jobe BO, Krueger AR, Peterson LA and Laird DA. (1997) Effects of long-term soil acidification due to nitrogen fertilizer inputs in Wisconsin. Plant and Soil. 197:61-69.
[https://doi.org/10.1023/A:1004297607070]

-
Cho HT and Cosgrove DJ. (2000) Altered expression of expansin modulates leaf growth and pedicel abscission in Arabidopsis thaliana. Proceedings of the National Academy of Sciences. 97:9783-9788.
[https://doi.org/10.1073/pnas.160276997]

-
Cosgrove DJ and Jarvis MC. (2012) Comparative structure and biomechanics of plant primary and secondary cell walls. Frontiers in Plant Science. 3:204.
[https://doi.org/10.3389/fpls.2012.00204]

-
Farh MEA, Kim YJ, Kim YJ and Yang DC. (2018) Cylindrocarpon destructans/Ilyonectria radicicola-species complex: Causative agent of ginseng root-rot disease and rusty root symptom. Journal of Ginseng Research. 42:9-15.
[https://doi.org/10.1016/j.jgr.2017.01.004]

-
Geem KR, Kim J, Bae W, Jee MG, Yu J, Jang I, Lee DY, Hong CP, Shim D and Ryu H. (2023) Nitrate enhances the secondary growth of storage roots in Panax ginseng. Journal of Ginseng Research. 47:469-478.
[https://doi.org/10.1016/j.jgr.2022.05.009]

-
Geem KR, Lim Y, Hong J, Bae W, Lee J, Han S, Gil J, Cho H and Ryu H. (2024) Cytokinin signaling promotes root secondary growth and bud formation in Panax ginseng. Journal of Ginseng Research. 48:220-228.
[https://doi.org/10.1016/j.jgr.2023.11.002]

-
Guo JH, Liu XJ, Zhang Y, Shen JL, Han WX, Zhang WF, Christie P, Goulding KWT, Vitousek PM and Zhang FS. (2010) Significant acidification in major Chinese croplands. Science. 327:1008-1010.
[https://doi.org/10.1126/science.1182570]

-
Hepler PK. (2005) Calcium: A central regulator of plant growth and development. The Plant Cell. 17:2142-2155.
[https://doi.org/10.1105/tpc.105.032508]

-
Hong CP, Kim J, Lee J, Yoo SI, Bae W, Geem KR, Yu J, Jang I, Jo IH, Cho H, Shim D and Ryu H. (2021) Gibberellin signaling promotes the secondary growth of storage roots in Panax ginseng. International Journal of Molecular Sciences. 22:8694.
[https://doi.org/10.3390/ijms22168694]

-
Hong J, Geem KR, Kim J, Jo IH, Yang TJ, Shim D and Ryu H. (2022) Prolonged exposure to high temperature inhibits shoot primary and root secondary growth in Panax ginseng. International Journal of Molecular Sciences. 23:11647.
[https://doi.org/10.3390/ijms231911647]

-
Hu B, Wang W, Ou S, Tang J, Li H, Che R, Zhang Z, Chai X, Wang H, Wang Y, Liang C, Liu L, Piao Z, Deng Q, Deng K, Xu C, Liang Y, Zhang L, Li L and Chu C. (2015) Variation in NRT1.1B contributes to nitrate-use divergence between rice subspecies. Nature Genetics. 47:834-838.
[https://doi.org/10.1038/ng.3337]

-
Kim K, Yun YB, Park M and Um Y. (2025) Correlation between soil properties and growth of wild-simulated ginseng for site suitability assessment. Korean Journal of Soil Science and Fertilizer. 58:432-441.
[https://doi.org/10.7745/KJSSF.2025.58.4.432]

-
Kim YJ, Zhang D and Yang DC. (2015) Biosynthesis and biotechnological production of ginsenosides. Biotechnology Advances. 33:717-735.
[https://doi.org/10.1016/j.biotechadv.2015.03.001]

-
Konishi M and Yanagisawa S. (2013) Arabidopsis NIN-like transcription factors have a central role in nitrate signalling. Nature Communications. 4:1617.
[https://doi.org/10.1038/ncomms2621]

-
Krouk G, Crawford NM, Coruzzi GM and Tsay YF. (2010) Nitrate signaling: Adaptation to fluctuating environments. Current Opinion in Plant Biology. 13:265-272.
[https://doi.org/10.1016/j.pbi.2009.12.003]

-
Lee SW, Jang IB, Hyun DY, Lee EH, Park KC, Yu J, Park HW and Kim GH. (2014) Analysis of growth characteristics and physiological disorder of Korean ginseng affected by application of decomposing plant residues in paddy-converted field. Korean Journal of Medicinal Crop Science. 22:427-434.
[https://doi.org/10.7783/KJMCS.2014.22.2.140]

-
Li K, Wan M, Han M and Yang L. (2025) The response of Panax ginseng root microbial communities and metabolites to nitrogen addition. BMC Plant Biology. 25:969.
[https://doi.org/10.1186/s12870-025-07031-6]

- Li M, Hou L, Zhang C, Wang M, Liu X, Korpelainen H and Li C. (2021) Genome-wide identification and expression analysis of the NRT gene family in poplar(Populus tomentosa) and functional analysis of PtoNRT2.5 involved in nitrate starvation response. Frontiers in Plant Science. 12:661635.
-
Liang H, Sun H, Shao C, Qian J, Lv B, Zhu J and Zhang Y. (2024) Genome-wide prediction and expression characterization of the GATA gene family under nitrogen and phosphate deficiency in Panax ginseng. Horticulturae. 10:282. https://www.mdpi.com/2311-7524/10/3/282, (cited by 2026 Feb 23).
[https://doi.org/10.3390/horticulturae10030282]

-
Liu C, Zhao M, Ma H, Zhang Y, Liu Q, Liu S and Wang Y. (2023) The NAC transcription factor PgNAC41-2 gene involved in the regulation of ginsenoside biosynthesis in Panax ginseng. International Journal of Molecular Sciences. 24:11946.
[https://doi.org/10.3390/ijms241511946]

-
Livak KJ and Schmittgen TD. (2001) Analysis of relative gene expression data using real-time quantitative PCR and the 2-ΔΔCt method. Methods. 25:402-408.
[https://doi.org/10.1006/meth.2001.1262]

-
Luo M, He Y, Zhu X, Li W, Peng X, Jiang J, Xu T, Meng X, Yang Z, He H and You J. (2025) Cell wall modification contributed to high aluminum retention in root epidermis for red skin root syndrome in Panax ginseng. Ecotoxicology and Environmental Safety. 303:118823.
[https://doi.org/10.1016/j.ecoenv.2025.118823]

-
Marchive C, Roudier F, Castaings L, Bréhaut V, Blondet E, Colot V, Meyer C and Krapp A. (2013) Nuclear retention of the transcription factor NLP7 is a rapid primary nitrate response that involves phosphorylation. Current Biology. 23:771-778.
[https://doi.org/10.1038/ncomms2650]

-
Medici A and Krouk G. (2014) The primary nitrate response: a multifaceted signalling pathway. Journal of Experimental Botany. 65:5567-5576.
[https://doi.org/10.1093/jxb/eru245]

- Mu X, Gu X, Ni L, Sun Y, Wen T, Li J, Song W and Chen X. (2025) Nitrogen deficiency-induced SnRK2.4/2.10 phosphorylation of NLP7 promotes root growth in Arabidopsis. Journal of Integrative Plant Biology. 67:123-135.
- NIAST(National Institute of Agricultural Science and Technology). (2000) Methods of soil chemical analysis. National Institute of Agricultural Science and Technology, Suwon, Korea.
- NIAST(National Institute of Agricultural Science and Technology). (2012) Research and investigation standards for agricultural science and technology. National Institute of Agricultural Science and Technology, Suwon, Korea.
- Qiu SJ, Ju XT, Ingwersen J, Qin ZC, Li L, Streck T and Christie P. (2014) Role of chemical fertilizer and manure in soil nitrogen accumulation and leaching in an intensive greenhouse vegetable system. Nutrient Cycling in Agroecosystems. 100:351-363.
- RDA(Rural Development Administration). (2021) Standard farming manual for ginseng(Panax ginseng). Rural Development Administration, Jeonju, Korea.
- RDA(Rural Development Administration). (2024) Ginseng. Rural Development Administration, Jeonju, Korea.
-
Sakuraba Y. (2022) Molecular basis of nitrogen starvation-induced leaf senescence. Frontiers in Plant Science. 13:1013304.
[https://doi.org/10.3389/fpls.2022.1013304]

- Seong JD, Kim GS, Kim HT, Park CB and Kim SM (2004) Effect of split application of nitrogen fertilizer on growth and yield in Platycodon grandiflorum A. DC. Korean Journal of Medicinal Crop Science 12:437-441.
-
Stork J, Harris D, Griffiths J, Williams B, Beisson F, Li-Beisson Y, Mendu V, Haughn G and DeBolt S. (2010) CELLULOSE SYNTHASE9 serves a nonredundant role in secondary cell wall synthesis in Arabidopsis epidermal testa cells. Plant Physiology. 153:580-589.
[https://doi.org/10.1104/pp.110.154062]

-
Sun J, Luo H, Yu Q, Kou B, Jiang Y, Weng L and Xiao C. (2022) Optimal NPK fertilizer combination increases Panax ginseng yield and quality and affects diversity and structure of rhizosphere fungal communities. Frontiers in Microbiology. 13:919434. https://www.frontiersin.org/journals/microbiology/articles/10.3389/fmicb.2022.919434/full, (cited by 2026 Feb 23).
[https://doi.org/10.3389/fmicb.2022.919434]

-
Witte CP. (2011) Urea metabolism in plants. Plant Science. 180:431-438.
[https://doi.org/10.1016/j.plantsci.2010.11.010]

-
Yang D, Bi C, Li F, Zhang L and Li Y. (2021) Transcriptome and proteomics analysis of wheat seedling roots reveals that increasing NH4+/NO3- ratio induced root lignification and reduced nitrogen utilization. Frontiers in Plant Science. 12:797260.
[https://doi.org/10.3389/fpls.2021.797260]
