인삼 주요 재배지별 지상부 곰팡이병 발생 현황 및 약제 저항성 검정
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Major above-ground fungal diseases of ginseng (including Alternaria blight, gray mold, and anthracnose), promoted by warm and humid conditions, reduce ginseng yield and quality. In this study, we surveyed disease occurrence in 2025 across major ginseng-producing regions in Korea, and evaluated the dominant pathogens and their fungicide resistance.
We conducted field surveys from May to September in 5–6-year-old ginseng fields in Cheorwon, Yeoncheon, Punggi, Jinan, Geumsan, and Eumseong, using five 3.3-m2 plots per region. We defined disease incidence as the proportion of diseased leaves. We first detected Alternaria blight in May, which increased throughout summer. Gray mold occurred sporadically from May to June and increased from July onward. Anthracnose appeared early in the season and became widespread by June. Internal transcribed spacer sequencing of 714 fungal isolates detected similar proportions of Alternaria panax and Alternaria alternata among the Alternaria blight isolates, with regional differences in dominance. Colletotrichum panacicola was the predominant anthracnose isolate, whereas we identified all gray mold isolates as Botrytis cinerea. Fungicide resistance assays indicated that more than 90% of Alternaria spp. and Colletotrichum spp. isolates were resistant to azoxystrobin, and B. cinerea isolates exhibited resistance to polyoxin B and boscalid.
The results of this study highlight early and widespread outbreaks under warm and humid conditions and emphasize the need for integrated region-specific disease management and fungicide resistance management programs.
Keywords:
Panax ginseng, Above Ground Fungal Diseases, Alternaria Blight, Anthracnose, Gray Mold, Fungicide Resistance, ITS Sequencing서 언
고려인삼 (Panax ginseng C. A. Mey.)은 인삼속 (Panax) 식물로 주로 우리나라와 북한, 중국에서 재배되고 있다. 2024년 재배면적은 10,585 ha, 농가 수는 15,877호로 특용작물 중 가장 높은 비중을 차지하고 있다. 또한 인삼류 수출액은 249백만 달러로 농산물 수출액의 약 3.3%를 차지하는 경제적으로도 중요한 작물 중 하나이다 (MAFRA, 2025).
인삼은 잎, 줄기 등 지상부에서 광합성을 통해 식물에 필요한 에너지를 생산하며, 이 에너지는 뿌리의 생장과 활성 물질 축적에 직접적인 영향을 미친다. 따라서 지상부의 생육 상태는 인삼의 생산량과 품질에 큰 영향을 준다. Kim 등 (2023)은 지상부 질적 형질의 생육 상태를 통해 지하부 수량을 예측할 수 있음을 보고하였다. 또한 지상부에는 상당량의 사포닌이 존재해 잎의 사포닌은 뿌리보다 약 4∼5배, 줄기보다 9배 이상 높아 다양한 산업적 활용 가능성이 높은 주요 자원으로 주목받고 있다 (Chang, 2003; Choi et al., 2009).
인삼은 한 번 정식하면 4∼6년간 동일포장에서 재배되는 작물로 병해 발생이 번하며 (Song et al., 2021), 현재까지 약 38 종의 병해가 보고되어 있다 (Kim et al., 2008). 이 중 점무늬병 (alternaria blight), 잿빛곰팡이병 (gray mold), 탄저병 (anthracnose)은 인삼 지상부에 발생하는 주요 병해로 생육과 생산량에 직접적인 피해를 준다.
인삼 점무늬병은 주로 Alternaria panax Fr. 병원균에 의해 발생하며, 강우가 잦고 다습한 환경에서 피해가 심하다. 4월 하순부터 5월 상순에는 연약한 줄기의 상처 부위에서 발생하고, 6월 상순에는 잎에 부정형 갈색 병반이 형성되며, 이후 엽맥을 따라 확산되어 7∼8월 고온기에 대량 발생한다 (Lee et al., 2012; Putnam, 2025). 병원균은 공기 중 비산 또는 강우 시 빗물에 의해 전반되어 발병한다 (Kim et al., 1980).
인삼 잿빛곰팡이병 병원균인 Botrytis cinerea Pers.는 1976년 국내에서 처음 보고되었으며, 기주범위가 넓은 다범성균으로 다양한 작물에 잿빛곰팡이병을 유발한다 (Cho et al., 2008). 병원균은 장마철인 6월 중순 이후 확산되며, 인삼의 잎, 열매, 줄기의 지제부 등을 침입하고, 병반 상에 회색의 분생포자와 검은색의 균핵을 형성한다 (Lee et al., 1990). 분생포자는 1차적으로 죽은 조직에 부생적으로 침입한 후 비산하여 줄기 및 두둑 상면 틈으로 침입하며, 뇌두 또는 지하부 줄기에서 균핵 상태로 잠복해 출아를 방해한다 (Cho, 2024).
인삼 탄저병은 1922년 처음 보고되었으며, 주로 Colletotrichum panacicola Hori에 의해 잎, 줄기, 열매에 모두 발생하고 늦봄부터 피해가 나타난다 (Chung and Bae, 1979; Han et al., 2004; Kim et al., 2010). 발생 초기에는 잎에 연한 갈색 반점이 형성되며, 점차 확산되어 부정형의 큰 병반을 형성한다 (Myung et al., 2024). 병원균은 빗방울에 의해 전반되고, 6∼7월 이후 고온 다습한 조건에서 급격히 발생한다 (Cho, 2024). 또한 토양 표면에 존재하다 빗방울 등에 의해 튀어 줄기 또는 잎으로 전염되며, 토양 및 식물체 조직에서 월동 후 적합한 환경에서 재발생한다 (Freeman et al., 1998; Lim et al., 2014).
인삼은 동일 포장에서 다년간 재배되므로 병원균 방제를 위해 동일 성분 혹은 유사 작용기작의 약제 사용이 반복되는 경향이 있다. 이로 인해 약제 저항성 병원균 출현에 대한 우려가 증가하고 있다. 선행 연구에서 인삼 잿빛곰팡이병원균은 폴리옥신 B 수화제에 대해 95% 이상의 저항성을 나타내었으며, 플루디옥소닐 액상수화제에 대해서는 감수성을 유지하는 것으로 보고되었다 (Lee et al., 2019). 또한 Myung 등 (2024)은 인삼 점무늬병과 탄저병 병원균에서 피라클로스트로빈 저항성 분리주가 확인된 반면, 플루아지남과 프로클로라즈에 대해서는 저항성이 나타나지 않았다고 보고하였다. 현재 국내에서 인삼 지상부 곰팡이병의 약제 저항성에 대한 체계적 조사는 부족하며, 현장에서는 기존 방제 약제의 감수성 저하가 점차 문제로 대두되고 있다.
따라서 본 연구는 인삼 재배지에서 발생하는 주요 지상부 병원균을 대상으로 약제 저항성 여부를 조사하고 저항성 병원균의 발생 양상을 파악함으로써, 병원균 별 효율적인 병해 관리 전략 수립을 위한 기초자료로 활용하고자 한다.
재료 및 방법
1. 조사 지역 및 조사 방법
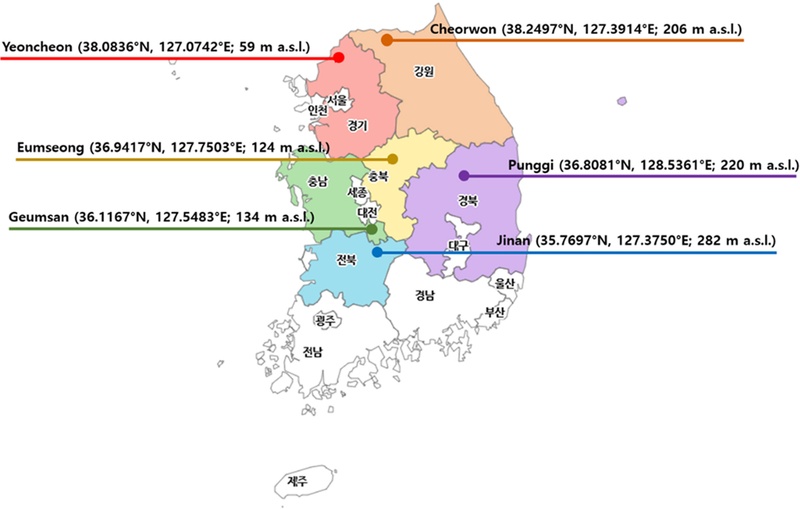
국내 주요 인삼 재배지의 지상부 병 발병 현황을 조사하기 위하여 2025년 지 인삼 특화작목시험장이 소재한 6개소 (강원 철원, 경기 연천, 경북 풍기, 전북 진안, 충남 금산, 충북 음성)에서 조사를 수행하였다 (Fig. 1).
인삼의 주요 지상부 병해인 점무늬병, 잿빛곰팡이병, 탄저병을 조사 대상으로 선정하였으며, 각 병해의 증상은 Fig. 2와 같다. 모든 지역에서 5년생 및 6년생 포장을 대상으로 5월부터 9월까지 매월 25일 전후에 조사를 실시하였다. 조사구는 3.3 m2 (90 ㎝ × 180 ㎝)를 기준으로 연생별 5 구간을 선정하여 동일 지점에서 반복 조사하였다. 매월 지역별 동일 지점에서 점무늬병, 잿빛곰팡이병 및 탄저병에 대해 발병률을 조사하였다. 발병률은 3.3 m2 당 발병잎수/전체잎수×100로 계산하여 백분율로 나타냈다.
2. 병원균 분리 및 동정
인삼 재배지에서 지상부 병 증상을 보인 잎을 채취한 후, 이병 부위에서 병원균을 분리하였다. 채취된 잎은 세척 후 병반 조직을 약 0.5 ㎝ 크기로 절단하였다. 절단된 절편은 70% ethanol에 1분, 1% NaOCl solution (Yuhan Co., Hwaseong, Korea)에 1분 침지하여 표면 소독을 실시하였고, 멸균 증류수로 3회 이상 세척하였다. 소독된 조직은 potato dextrose agar (PDA, Becton Dickinson and Company, Franklin Lakes, NJ, USA) 배지에 치상하고, 15-20℃에서 7일간 배양하였다. 배양된 조직에서 자란 균사는 분리하여 새로운 PDA 배지에 계대 배양하고 순수 배양하여 실험에 사용하였다. 분리된 균주는 20℃에 배양하여 약제 저항성 분석 실험에 이용하였으며, 장기 보관 균주는 20% glycerol 용액을 사용하여 –80℃에 저장하였다.
인삼 이병 부위에서 분리된 병원균은 먼저 광학현미경 (Leica Microsystems Ltd., Wetzlar, Germany)을 이용하여 분생포자 형태를 관찰해 1차 동정을 실시하였으며, PDA 배지에서의 균총 생육 및 분생포자 형태는 Fig. 3과 같다. 이후 분자생물학적 동정을 위해 internal transcribed spacer (ITS) 영역을 증폭하여 염기서열을 분석하였다. 배양된 균주는 grinding buffer (20 mM EDTA, 0.1 M Tris-Cl, 1.4 M NaCl)와 BCSTM Folder (Biocube system Inc., Suwon, Korea)를 이용하여 genomic DNA를 추출하였다. ITS 영역 증폭은 ITS1 및 ITS4 primer를 사용하여 PCR 장비 (Bio Rad T100 Thermal Cycler, Singapore)로 수행하였다 (95℃ for 2 min; 35 cycles of 95℃ 20 s, 55℃ for 40 s and 72℃ for 1 min; final extension at 72℃ for 5 min). PCR 산물의 염기서열은 MEGA version 12 프로그램 (Kumar et al., 2024)을 이용해 정렬하였으며, 품질이 낮거나 불분명한 염기가 포함된 서열은 분석에서 제외하였다. ITS 염기서열이 NCBI (The National Center for Biotechnology Information, Bethesda, MD, USA)에 등록된 해당 종의 ITS 서열과 99.0∼100.0%의 상동성을 보일 경우 동일 종으로 동정하였다.

Colony morphology and microscopic characteristics of above-ground pathogenic isolates from ginseng.(A) Alternaria panax (alternaria blight), (B) Botrytis cinerea (gray mold), and (C) Colletotrichum panacicola (anthracnose) cultured on PDA; (D) A. panax showing muriform conidia with 3-7 transverse septa (35-50 × 14-22 μm), (E) B. cinerea with ellipsoid, aseptate conidia (9-14 × 6-12 μm), and (F) C. panacicola showing cylindrical to falcate, aseptate conidia (16-26 × 3-6 μm) observed under a light microscope.
3. 생명정보 등록
확보된 ITS 염기서열 총 498점을 NCBI의 GenBank에 등록하였으며 부여받은 번호는 다음과 같다; PX481862∼PX482010, PX482056∼PX482107, PX482186∼PX482252, PX956320∼PX956411, PX956450∼PX956470, PX956489∼PX956504, PX956506∼PX956561, PX957526, PX957528∼PX957556, PX957558∼PX957571, PX963209
4. 약제 저항성 분석
2025년 조사 포장에서 수집한 이병 식물체로부터 분리한 병원균을 약제 저항성 분석에 사용하였다. 분리된 병원균은 점무늬병, 잿빛곰팡이병 및 탄저병을 대상으로 하였으며, 병해별로 국내 인삼 재배지에서 일반적으로 사용되는 약제를 선별하여 균주별 약제 감수성을 평가하였다. 점무늬병원균 (Alternaria spp.)과 탄저병원균 (Colletotrichum spp.)에 대해서는 동일한 4종의 화학 약제를 사용하였다: 아족시스트로빈, 메트코나졸, 이미녹타딘트리스알베실레이트, 플루아지남. 잿빛곰팡이병원균 (Botrytis spp.)에 대해서는 플루디옥소닐, 펜헥사미드, 보스칼리드, 폴리옥신 B 등 4종의 약제를 적용하였다.
각 병원균은 PDA 배지에서 순수 배양한 후, 인삼에 권장되는 농도의 시험 약제 4종을 각각 첨가한 PDA 배지 (처리구)와 약제를 첨가하지 않은 PDA 배지 (무처리 대조구)에 접종하여 재배양하였다. 접종한 배지는 20℃에서 7일간 배양한 후 균총을 촬영하였으며, ImageJ software (version 1.54) (National Institutes of Health, Bethesda, MD, USA)를 이용하여 균총의 면적을 정량화하였다. 약제 처리에 따른 생장 억제 정도는 무처리 대조구 대비 처리구의 균총 면적을 비교하여 균사 생장 억제율 (%)로 산출하였다. 약제 저항성은 다음 공식으로 계산하였다: 균사 생장 억제율 (%) = {(무처리구 균총 면적 - 처리구 균총 면적) / 무처리구 균총 면적} × 100. 균사 생장 억제율이 95% 미만일 경우 저항성으로, 95% 이상일 경우를 감수성으로 판정하였다.
5. 통계 분석
본 연구에서 시행한 모든 통계 분석은 IBM SPSS Statistics (version 29.0, IBM Corp., Armonk, NY, USA) 프로그램을 사용하여 수행하였다. 지역별 병원균 종 구성 비율의 유의성을 검정하기 위해 카이제곱 검정 (Chi-square test)을 실시하였으며, p < 0.001 수준에서 통계적 유의성을 검정하였다.
결과 및 고찰
1. 시기별 및 지역별 지상부 병 발생 양상
2025년 인삼 특화작목시험장 6개소를 대상으로 5월부터 9월까지 지상부 주요 병해인 점무늬병, 잿빛곰팡이병, 탄저병의 발생 현황을 조사하였다.
인삼 점무늬병은 일반적으로 6월 하순부터 발병이 확인되나, 조사한 해에는 5월 하순부터 풍기를 제외한 5 지역에서 조기 발생이 확인되었으며, 금산에서 0.9%로 가장 높은 초기 발병률이 나타났다 (Table 1). 6월 하순에는 전 조사 지역에서 점무늬병이 발생하였고, 풍기에서는 6월에 하순에 첫 점무늬병 발병을 관찰함과 동시에 가장 높은 발병률 (3.7%)을 보였다. 7월에는 점무늬병이 지속적으로 확산되어 철원 16.2%, 연천 13.6%, 진안 6.2%, 금산 3.7%, 음성 3.0%의 발병률이 나타났으며, 특히 풍기에서는 65.8%로 급격한 증가가 확인되었다. 8월 점무늬병은 풍기를 제외한 전 지역에서 발병률이 더욱 증가하여 연천 44.8%, 철원 35.6%, 진안 33.4%의 발병률을 보였다. 풍기의 경우 병이 동시다발적으로 발생하여 8월 이후 고사율이 76.9%에 이르렀고 (Table 2), 이에 따라 잎 수 감소로 상대적으로 발병률이 낮게 산출되었다. 특히 풍기 지역은 7월 말부터 극심한 낙엽 현상이 동반되었으며, 조사 시점에 잔존한 잎들을 대상으로 발병률을 조사함에 따라 수치상의 급격한 감소가 나타났다. 그 외 지역에서는 연천 58.3%, 풍기 22.5%, 진안 22.1%의 발병률이 관찰되었으며, 특히 금산은 61.4%로 급격한 증가가 확인되었다. 음성은 6.0%의 발병률을 보이며 조사 지역 중 가장 낮은 발병률을 보였다.
2025년에는 5-6월부터 고온·다습한 기상 조건이 형성되어 점무늬병의 초기 감염 시점이 예년보다 앞당겨졌을 가능성이 높다. 특히 풍기에서 7월 말 발병률이 급등한 현상은 장마기에 동반된 잦은 강우와 비산에 의한 2차 전염 확대로 설명될 수 있다. 또한 차광 수준, 통풍, 재식밀도 등 포장 관리 차이에 따른 포장 내 미기상 변화로 엽면 습윤 지속시간이 증가하여 병 발생이 촉진되었을 가능성도 있다. 한편, 풍기 지역에서 8월 발병률 (65.8%)이 전월 (22.5%) 대비 급격히 감소한 현상은 병의 완화가 아닌 감염 조직의 조기 탈락에 따른 수치적 변동으로 판단된다. 7월 말부터 시작된 동시다발적인 발병으로 인해 8월 고사율이 76.9%에 달하였으며, 이 과정에서 중증 감염된 잎들이 조기에 탈락됨에 따라 조사 시점에 생존해 있는 잎들만을 대상으로 산출되는 발병률 수치가 상대적으로 낮게 나타난 것이다. 즉, 이는 발병률 산정 시 분모인 전체 잎 수의 급격한 변동에 기인한 것이며, 실제 포장의 병 발생 양상은 고사율 데이터를 통해 확인할 수 있듯이 지속적인 증가 추세였음을 시사한다.
반면 음성 지역은 조사 기간 전반에 걸쳐 발병률이 상대적으로 낮았으며(9월 6.0%), 이는 해당 지역의 포장 미기상 및 재배 관리 조건이 점무늬병 발생을 억제하는 방향으로 형성되었거나, 초기 방제 약제 선택 및 통풍 관리 등 방제 체계가 비교적 효과적으로 작동했을 가능성을 시사한다.
잿빛곰팡이병에 대해 조사한 결과는 Table 3과 같다. 잿빛 곰팡이병은 5월 말 철원 (0.1%)에서 첫 발병이 확인되고, 6월에는 풍기 (0.2%)에서 추가로 발견되었다. 발병 시기는 다른 지상부 곰팡이병에 비해 늦었으며, 7월부터 점차 증가하여 철원 1.9%, 연천 0.3%, 진안과 금산 2.1%, 음성 0.6%의 발병률이 나타났다. 특히 7월 풍기에서는 17.2%로 높은 발병률이 확인되었다. 8월에는 잿빛곰팡이병이 급격히 확산되어 풍기 15.4%, 진안 15.2%, 금산 5.0%, 철원 3.2%, 음성 2.4%, 연천 2.3%의 발병률이 나타났다. 9월에는 금산에서 69.2%로 가장 높은 발병률을 보였고, 연천에서도 21.2%로 급격한 증가가 확인되었다. 그 외 풍기 22.1%, 진안 8.5%의 발병률이 관찰되었으며, 음성은 5.4%로 조사 지역 중 가장 낮은 수준이었다. 이러한 양상은 B. cinerea가 잔존 조직 또는 노화 조직을 기반으로 감염원이 축적되기 쉬워 생육 후반부 (8∼9월)로 갈수록 발병이 확대되는 병 발생 특성과 부합한다 (Petrasch et al., 2019; Ullah et al., 2024). 즉, 감염원이 누적되는 가운데, 기온이 다소 낮아지더라도 상대습도가 유지되거나 야간 이슬 및 차광 조건에서 결로로 인해 엽면 습윤 시간이 길어질 경우 병 발생이 급격히 증가할 수 있다. 특히 9월 금산에서의 급증 양상은 생육 후반의 조직 노화와 잔존 조직 증가, 지속적인 다습 조건이 중첩되면서 발병이 가속화되었을 가능성을 시사한다. 또한 지역별 강수 및 다습 지속 조건의 차이는 엽면 습윤과 병 확산을 좌우하는 주요 요인으로, 8∼9월 강수량이 상대적으로 높았던 지역 (금산, 철원, 연천)에서는 강우 후 다습이 지속되면서 병 확산이 촉진되었을 가능성이 있다. 따라서 잿빛곰팡이병의 지역 간 발병 차이는 생육 후반부의 감염원 축적과 강우 이후 다습 지속 및 엽면 습윤 시간 증가와 같은 미기상 조건이 복합적으로 작용한 결과로 판단된다.
탄저병에 대해 조사한 결과는 Table 4와 같다. 탄저병은 5월 연천 (0.5%), 진안 (1.0%), 금산 (0.1%)에서 조기 발병이 확인되었으며, 6월 하순에는 전 조사 지역에서 관찰되었다. 6월에는 연천에서 2.4%로 가장 높은 발병률이 나타났다. 7월은 음성을 제외한 전 조사 지역에서 급격히 증가한 발병률을 보였으며, 7월에는 음성을 제외한 전 지역에서 발병률이 급격히 증가하였으며, 특히 풍기에서는 40.8%로 점무늬병 및 잿빛곰팡이병과 함께 높은 발병률이 확인되었다. 8월에는 탄저병이 지속적으로 확산되어 연천 42.0%, 풍기 36.4%, 철원 33.4%, 진안 22.4%, 금산 4.7%, 음성 0.3%의 발병률이 나타났다. 9월에는 연천 (25.2%)과 풍기 (24.6%)에서 고사된 개체 증가로 8월 대비 발병률이 낮게 산출되었으나, 진안은 33.2%로 지속적인 증가가 관찰되었고, 금산에서는 80.4%로 급격한 발병 확대가 확인되었다. 음성은 2.6%로 조사 지역 중 가장 낮은 발병률을 보였다. 탄저병은 일반적으로 강우에 의한 병원균 비산과 고온다습 조건에서 2차 감염이 연속적으로 발생하는 병으로 알려져 있으며, 특히 6-8월 강우와 고습 조건이 누적될 경우 급증 양상이 뚜렷하게 나타난다 (Kwon and Lee, 2002; Jee et al., 2010). 본 조사에서도 7∼8월에 대부분 지역에서 발병률이 크게 증가한 점은 이러한 병 발생 특성과 부합한다. 또한 풍기에서 7월 발병률이 급등한 현상은 장마기 강우 빈도 증가에 따른 병원균 확산과, 차광·통풍·재식밀도 등 포장 내 미기상 차이에 따른 엽면 습윤 지속시간 증가가 복합적으로 작용했을 가능성을 시사한다. 반면 9월 연천과 풍기에서 발병률이 감소한 현상은 실제 병 발생 완화보다는 고사 및 낙엽 증가로 전체 잎 수가 감소하면서 발병률 산정 시 분모 변화에 따른 산출 편차가 일부 반영되었을 가능성을 고려하여 해석할 필요가 있다.
한편, 금산 지역은 8월까지 점무늬병 5.3%, 잿빛곰팡이병 5.0%, 탄저병 4.7%로 발병 수준이 낮게 유지되었으나, 9월에 각각 61.4%, 69.2%, 80.4%로 동시적인 급증 양상이 관찰되었다. 이러한 동시적 발병 확대는 특정 병원균의 단독 요인보다는, 선행 감염에 따른 식물체 생육 저하와 저항성 약화 상태에서, 강우 이후 다습 지속이 중첩되어 복합감염이 동시에 확대된 결과 판단된다.
2. 기상 조건과 병 발생 관계
곰팡이병은 일반적으로 고온다습한 조건에서 발생과 확산이 촉진되며, 특히 강우 후 높은 상대습도가 유지될 경우 병원균의 침입과 증식이 활발해지는 것으로 알려져 있다 (Huber and Gillespie, 1992; Velásquez et al., 2018). 따라서 기상 조건에 따른 병해 발생 양상을 분석하기 위해 지역별 기상 자료를 조사하였으며, 그 결과는 Table 5, 6과 같다. 조사 대상 6개 지역의 평년 (10년) 평균기온과 강수량, 그리고 2025년 지역별·월별 강수량은 기상청 날씨누리 데이터를 활용하였고 (KMA, 2025), 2025년 각 지역 해가림 시설 내 월별 기온은 데이터로거 (Lascar Electronics, Whiteparish, Wiltshire, UK)를 지상부 30 ㎝ 상단에 설치하여 측정하였다. 해가림 시설 내에서 측정된 기온은 노지 표준 관측값과 미기상이 다를 수 있으며, 차광에 따른 복사열 감소로 기온 조건이 상대적으로 낮거나 변동폭이 완화될 가능성이 있다.
조사 연도 5월의 평균기온은 16.3∼19.0℃로 지역에 따라 평년 (17.9℃) 대비 -1.6+1.1℃ 범위로 나타났으며, 특히 금산에서 평년보다 1.1℃ 높았다. 강수량은 전 지역에서 평년 (81.2 ㎜)보다 5.5∼51.9 ㎜ 많았다. 이러한 초기의 높은 기온과 강수 조건은 병원균의 초기 정착에 유리한 환경을 제공했을 것으로 해석된다. 이어 6월에는 모든 지역에서 평년 (22.1℃, 120.2 ㎜) 대비 기온과 강수량이 각각 22.2-24.1℃, 165.5∼464.0 ㎜로 동시에 증가하였으며, 간헐적이지만 강도가 큰 강우가 반복적으로 발생하였다. 이러한 불규칙한 폭우와 장기간의 고습 조건은 지상부 곰팡이병의 발병 시점을 앞당기고, 이후 병 발생 밀도를 빠르게 증가시키는 요인으로 작용했을 것으로 해석된다. 불규칙한 강우 패턴과 급격한 수분 증가는 지상부 병원균의 포자 생산과 비산, 2차 감염을 촉진하는 주요 요인이라는 점은 기존 연구에서도 보고된 바 있다 (Romero et al., 2022; Zhou et al., 2024). 따라서 2025년의 이례적으로 높은 초기 강수량과 기온 상승이 조사 포장 전반에서 지상부 병의 조기 발병과 확산을 유발한 주요 기상 요인으로 해석된다.
3. 지상부 병 분리 및 동정
2025년 수집된 지상부 병원균을 분리한 결과 총 716개 균주가 확보되었다 (Table 7). 이 중 점무늬병은 225균주였으며, 주로 Alternaria panax와 A. alternata로 동정되었다. 두 종의 비율은 각각 44.0%로 유사하게 나타났다. 잿빛곰팡이병 병원균은 143개 균주가 분리되었고, 모든 균주가 Botrytis cinerea (100.0%)로 확인되었다. 탄저병 병원균은 총 130균주가 수집되었으며, 이 중 Colletotrichum panacicola가 97.7%로 우점하였다. 그 외 C. gloeosporioides, C. fructicola이 소수 검출되었다.
점무늬병 병원균의 종 구성은 기존 보고와 차이를 보였다. 인삼 점무늬병의 주요 병원균은 일반적으로 A. panax로 알려져 왔으나 (Ohh, 1981; Kim et al., 2007; Kim et al., 2010), 본 조사에서는 두 종의 비율이 유사하면서 전체적으로 A. alternata가 근소하게 높은 경향을 보였다. 이는 최근 차광, 통풍 등 재배 환경 변화 또는 기후요인 변화에 따라 병원균 집단 구조가 변동되었을 가능성을 시사한다. 특히 A. alternata 종 복합체 (Species complex) 내의 특정 계통들이 숙주 특이적 독소 (Host-specific toxin) 생산 능력을 갖추며 다양한 작물에 적응하는 양상이 보고된 바 있다 (Woudenberg et al., 2015). 따라서 본 연구에서 확인된 병원균 구성의 차이는 환경 변화에 적응한 A. alternata 계통의 포장 내 정착 가능성을 시사하며, 향후 두 종 간의 명확한 구분을 위한 계통 분류학적 검토가 요구된다.
탄저병 병원균 구성에서도 기존 보고와 차이가 나타났다. 과거 연구에서는 인삼 탄저병의 주요 원인균으로 C. gloeosporiodies가 널리 보고되었으나 (Do and Kil, 2001; Lee et al., 2012; Kim et al., 2014), 본 조사에서는 C. panacicola가 우점하였다. 이러한 결과는 인삼 재배지 내 병원균 군집 구성의 물리적 변화일 가능성과 더불어, 분자계통학적 분석을 통해 정밀화된 Colletotrichum 속의 재정립 (Jayawardena et al., 2015) 에 따른 결과로 해석될 수 있다. 과거 주요 원인균으로 보고된 C. gloeosporioides는 형태적 유사성에 기반한 광범위한 종 집단이었으나, 최신 분류 체계에서는 인삼 특이적 계통들이 C. destructivum 종 복합체 내의 독립 종인 C. panacicola 등으로 세분화되었다 (Damm et al., 2014). 따라서 본 조사에서 나타난 종 구성의 차이는 실제 병원균 구성의 물리적 변화뿐만 아니라, 정밀해진 분류 체계 적용에 따른 결과임을 시사한다. 이러한 종 동정의 변화는 종별 생태적 특성이나 약제 반응성이 다를 수 있으므로, 향후 약제 반응성 및 방제 적기 연구 시 이와 같은 분류학적 변화를 고려하는 것이 매우 중요하다.
반면 잿빛곰팡이병에서 B. cinerea가 100%로 동정된 점은 해당 병원균의 분포가 안정적이며 생태적 지위 (ecological niche)가 명확함을 보여준다.
다만, 본 연구에서 수행된 종 동정은 균류의 표준 바코드인 ITS 영역을 기반으로 하였다. Alternaria 및 Collectotrichum 속과 같이 종 간 경계가 모호한 분류군에서는 ITS 단독 분석만으로 완벽한 종 수준 구분에 한계가 있을 수 있다. 따라서 본 결과는 ITS 서열에 기반한 잠정적인 동정 결과로 해석되어야 하며, 향후 명확한 계통 분류를 위해 GAPDH, actin, beta-tublin 등 다중 유전자 서열 (Multi-locus sequence typing, MLST)을 활용한 정밀한 종 동정과 분류학적 검증이 병행되어야 할 것으로 판단된다.
점무늬병은 잿빛곰팡이병과 탄저병에 비해 지역별 수집 균주 수가 많아, 지역 간 병원균 구성 차이를 비교할 수 있었다 (Table 8). 지역별 점무늬병 병원균의 종 구성 분포를 분석한 결과, 지역에 따라 우점하는 병원균의 종류가 통계적으로 매우 유의미한 차이를 보였다 (χ2= 61.90, df = 10, p < 0.001). 특히 철원에서는 A. alternata (45.8%)가 A. panax보다 다소 높은 비율을 보였으며, 연천에서는 두 종이 각각 46.2%로 동일한 비율을 나타냈다. 풍기와 진안에서는 A. alternata가 각각 54.0%, 69.2%로 우점하였고, 음성에서는 A. panax가 78.6%로 가장 높은 비율을 차지하였다. 이러한 지역 간 분포 차이는 지역적 환경 특성이 병원균 구성에 영향을 미쳤을 가능성을 시사한다. 특히 연천에서 두 종이 동일 비율로 확인된 점은, 해당 지역의 환경 조건이 두 종 간 경쟁에서 뚜렷한 우위를 형성하지 않는 중립적 환경일 가능성을 나타낸다.
이상의 결과와 같이 2025년 인삼 지상부 병원균 구성은 일부 병에서 기존 우점균과 차이를 보였으며, 이는 기후변화, 재배 환경 차이 및 지역 특성 등 다양한 요인에 의해 영향을 받았을 가능성을 시사한다. 따라서 이러한 변동이 일시적 현상인지, 장기적인 군집 구조 변화인지를 판단하기 위해서는 향후 다지역·다년도 추가 조사와 기후·환경요인의 정량적 분석이 필요할 것으로 판단된다.
4. 지상부 병원균의 약제 저항성 분석
수집된 인삼 지상부 점무늬병, 잿빛곰팡이병 및 탄저병 병원균을 대상으로 농가에서 주로 사용하는 약제를 이용하여 약제 저항성을 평가하였다. 점무늬병 병원균 192균주, 잿빛곰팡이병 병원균 102균주, 탄저병 병원균 105균주를 시험에 사용하였으며 결과는 Table 9과 같다.
점무늬병 병원균은 아족시스트로빈에 대해 98.4%의 저항성을 나타냈으며, 메트코나졸 45.8%, 이미녹타딘트리스알베실레이트 27.1%, 플루아지남 24.5%의 저항성이 확인되었다. 잿빛곰팡이병 병원균은 플루디옥소닐에 대해 8.8%의 저항성을 보였으나, 펜헥사미드 62.7%, 보스칼리드 91.2%, 폴리옥신 B 92.2%로 높은 저항성이 나타났다. 탄저병 병원균은 아족시스트로빈에 대해 96.2%, 이미녹타딘트리스알베실레이트에 대해 89.5%의 저항성을 보였으며, 메트코나졸과 플루아지남에 대해서는 상대적으로 감수성이 유지되었다. 본 연구에서 확인된 약제 저항성 양상은 인삼 지상부 병원균의 약제 반응성이 기존 농가 경험이나 방제 권고와 상이한 비율로 나타나고 있음을 보여준다. 특히 점무늬병과 탄저병 병원균에서 아족시스트로빈 저항성이 각각 98.4%, 96.2%로 높게 나타난 점은 해당 약제가 장기간 반복적으로 사용되면서 병원균 집단 내 내성 개체가 고정되었을 가능성을 시사한다.
잿빛곰팡이병 병원균에서 폴리옥신 B에 대한 높은 저항성 (92.2%)은 현장 방제 체계에 중대한 영향을 미칠 수 있다. 폴리옥신 B는 인삼 잿빛곰팡이병 방제를 위해 오랫동안 사용되어 왔으나, 본 조사에서는 대부분의 균주가 저항성을 보였다. 이는 동일 약제를 장기간 사용하는 관행이 병원균 저항성을 빠르게 고착화할 수 있음을 보여주는 사례이다.
약제 저항성은 특정 약제가 반복적으로 사용될 때 병원균이 유전적으로 적응하여 감수성이 감소하고 생존 능력을 획득하는 현상으로, 약제 처리 효과 저하와 병해 방제 실패를 초래하여 수량 감소 및 농가 경영비 증가로 이어질 수 있다 (Hollomon, 2015; Ishii and Holloman, 2015; Neils et al., 2021). 따라서 서로 다른 작용 기작을 지닌 약제를 교호 살포하고 동일 약제의 연속 처리를 지양하는 것이 중요하다 (Fernandez-Ortuño et al., 2013; Myung et al., 2024). 지역별 약제 사용 이력, 병 발생 환경, 분자 수준의 저항성 메커니즘을 통합적으로 분석하는 다년도 후속 연구가 수행된다면, 보다 지속 가능한 인삼 병해 관리 전략 수립에 기여할 수 있을 것으로 판단된다.
Acknowledgments
본 연구는 농촌진흥청 시험연구사업(PJ01602702)의 지원에 의해 이루어진 것으로 이에 감사드립니다.
References
- Chang HK. (2003). Effect of processing methods on the saponin contents of Panax ginseng leaf-tea. The Korean Journal of Food and Nutrition. 16:46-53.
- Cho DH. (2024). History of disease control of Korean ginseng over the past 50 years. Journal of Ginseng Culture. 6:51-79.
-
Cho HS, Jeon YH, Do GR, Cho DH and Yu YH. (2008). Mycological characteristics of Botrytis cinerea causing gray mold on ginseng in Korea. Journal of Ginseng Research. 32:26-32.
[https://doi.org/10.5142/JGR.2008.32.1.026]

- Choi JE, Li X, Han YH and Lee KT. (2009). Changes of saponin contents of leaves, stems and flower-buds of Panax ginseng C. A. Meyer by harvesting days. Korean Journal of Crop Science. 17:251-256.
- Chung HS and Bae HW. (1979). Ginseng anthracnose in Korea-factors affecting primary inoculum, growth of the pathogen, disease development and control. Korean Journal of Plant Protection. 18:35-41.
-
Damm U, O'connell RJ, Groenewald JZ and Crous PW. (2014). The Colletotrichum destructivum species complex-hemibiotrophic pathogens of forage and field crops. Studies in Mycology. 79:49-84.
[https://doi.org/10.1016/j.simyco.2014.09.003]

- Do ES and Kil GJ. (2001). Screening and utilization of antifungal plant against ginseng anthracnose(Colletotrichum gloeosporioides). Korean Journal of Plant Resources. 14:206-212.
-
Fernadez-Ortuño D, Grabke A, Li X and Peres NA. (2013). Fungicide resistance profiles in Botrytis cinerea from strawberry fields. Plant Disease. 97:340-347.
[https://doi.org/10.1094/PDIS-01-13-0012-PDN]

-
Freeman S, Katan T and Shabi E. (1998). Characterization of Colletotrichum species responsible for anthracnose diseases of various fruits. Plant Disease. 82:596-605.
[https://doi.org/10.1094/PDIS.1998.82.6.596]

-
Han KD, Alam S, Lee TS and Lee MW. (2004). Ginseng anthracnose caused by Colletotrichum dematium. Plant Pathology Journal. 20:196-199.
[https://doi.org/10.5423/PPJ.2004.20.3.196]

-
Hollomon DW. (2015). Fungicide resistance: Facing the challenge. Plant Protection Science. 51:170-176.
[https://doi.org/10.17221/42/2015-PPS]

-
Huber L and Gillespie TJ. (1992). Modeling leaf wetness in relation to plant disease epidemiology. Annual Review of Phytopathology. 30:553-577.
[https://doi.org/10.1146/annurev.py.30.090192.003005]

-
Ishii H and Holloman DW. (2015). Fungicide resistance in plant pathogens. Springer. Tokyo, Japan.
[https://doi.org/10.1007/978-4-431-55642-8]

-
Jayawardena RS, Hyde KD, Damm U, Cai L, Liu M, Li XH. Zhang W, Zhao WS and Yan JY. (2016). Notes on currently accepted species of Colletotrichum. Mycosphere. 7:1192-1260.
[https://doi.org/10.5943/mycosphere/si/2c/9]

-
Jee HJ, Shin SS, Lee JH, Kim WI, Hong SJ and Kim YK. (2010) Conidial disperse of the pepper anthracnose fungus Colletotrichum acutatum and its density on infected fruits. Research in Plant Disease. 16:101-105.
[https://doi.org/10.5423/RPD.2010.16.1.101]

- Kim HJ, Cheong SS, Kim DW, Park JS, Ryu J, Bea YS and Yoo SJ. (2008). Investigation into disease and pest incidence of Panax ginseng in Jeonbuk province. Korean Journal of Medicinal Crop Science. 16:33-38.
-
Kim J, Lee SW, Min JY, Bae YS, Shin MU and Kim SB. (2007). Development of control system with fungicides against disease of ginseng plant. Research in Plant Disease. 13:164-169.
[https://doi.org/10.5423/RPD.2007.13.3.164]

-
Kim WS, Lee JH, Kim YC and Chang SW. (2014). Control efficiency for ginseng anthracnose by eco-friendly organic materials. Korean Journal of Medicinal Crop Science. 22:270-275.
[https://doi.org/10.7783/KJMCS.2014.22.4.270]

-
Kim YC, Lee JH, Bae YS, Sohn BK and Park SK. (2010). Development of effective environmentally-friendly approaches to control Alternaria blight and anthracnose diseases of Korean ginseng. European Journal of Plant Pathology. 127:443-450.
[https://doi.org/10.1007/s10658-010-9610-4]

-
Kim YC, Lee JW, Kwon NY, Jung SM, Bang KH, Kim DH and Kim JU. (2023). Correlation between qualitative characteristics of aerial parts and root yield in ginseng. Korean Journal of Medicinal Crop Science. 31:57-64.
[https://doi.org/10.7783/KJMCS.2023.31.2.57]

- Kim YT, Kim HJ and Lee SG. (1980). Control test of leaf spot disease. Research Report(Cultivation Division), Korea Ginseng Research Institute. Suwon, Korea. p.375.
- Korea Meterological Administration(KMA). (2025). Korea Meteorological Administration. Seoul, Korea. https://www.kma.go.kr/eng/, (cited by 2025 Dec 3).
-
Kumar S, Stecher G, Suleski M, Sanderford M, Sharma S and Tamura K. (2024). MEGA12: Molecular evolutionary genetic analysis version 12. Molecular Biology and Evolution. 41:msae263.
[https://doi.org/10.1093/molbev/msae263]

-
Kwon CS and Lee SG. (2002) Occurrence and ecological characteristics of red pepper anthracnose. Research in Plant Disease. 8:120-123.
[https://doi.org/10.5423/RPD.2002.8.2.120]

-
Lee HJ, Park KC, Lee SH, Bang KH, Park HW, Hyun DY, Kang SW, Cha SW and Jeong IM. (2012). Screening of antifungal Bacillus spp. against alternaria blight pathogen (Alternaria panax) and anthracnose pathogen(Colletotrichum gloeosporioides) of ginseng. Korean Journal of Medicinal Crop Science. 20:339-344.
[https://doi.org/10.7783/KJMCS.2012.20.5.339]

- Lee JH, Yu YH, Kim YH, Ohh SH and Park WM. (1990). Morphological characteristics and pathogenicity of alternaria isolates causing leaf and stem blights and black root rot of Korean ginseng. Korean Journal of Plant Pathology. 6:13-20.
- Lee SH, Seo MW and Lee SW. (2019). Study of fungicide resistance and pathogenicity of Botrytis cinerea causing ginseng gray mold in Korea. Korean Journal of Medicinal Crop Science. 27:138.
-
Lim JS, Mo HW, Lee EH, Park KC and Chung CM. (2014). Suppressive effects of homemade environment-friendly materials on alternaria blight and anthracnose of ginseng. Korean Journal of Organic Agriculture. 22:705-718.
[https://doi.org/10.11625/KJOA.2014.22.4.705]

- Ministry of Agriculture, Food and Rural Affairs(MAFRA). (2025). Ginseng statistics report 2024. MAFRA. Sejong, Korea.
-
Myung KS, Abdullahi A and Kim HT. (2024). Changes in susceptibility of pathogens isolated from ginseng aerial parts to pyraclostrobin, fluazinam, and prochloraz. Korean Journal of Pesticide Science. 28:280-290.
[https://doi.org/10.7585/kjps.2024.28.3.280]

-
Neils AL, Brisco-McCann EI, Harlan BR and Hausbeck MK. (2021). Management strategies for alternaria leaf blight on American ginseng. Crop Protection. 139:105302.
[https://doi.org/10.1016/j.cropro.2020.105302]

- Ohh SH. (1981). Diseases of ginseng: Environmental and host effect on disease outbreak and growth of pathogens. Korean Journal of Ginseng Science. 5:73-84.
-
Petrasch S, Knapp SJ, Van Kan JA and Blanco-Ulate B. (2019). Grey mould of strawberry, a devastating disease caused by the ubiquitous necrotrophic fungal pathogen Botrytis cinerea. Molecular Plant Pathology. 20:877-892.
[https://doi.org/10.1111/mpp.12794]

- Putnam M. (2025). Ginseng(Panax spp.)–Alternaria leaf and stem blight. In Pscheidt JW and Ocamb CM.(senior editors). Pacific Northwest Plant Disease Management Handbook [online]. Oregon State University. Corvallis, OR, USA. https://pnwhandbooks.org/plantdisease/host-disease/ginseng-panax-spp-alternaria-leaf-stem-blight, (cited by 2025 Dec 17).
-
Romero F, Cazzato S, Walder F, Vogelgsang S, Bender SF and Heijen MG. (2022). Humidity and high temperature are important for predicting fungal disease outbreaks worldwide. New Phytologist. 234:1553-1556.
[https://doi.org/10.1111/nph.17340]

-
Song TH, Lee YW, Youn TH, Park EA, Shim ES, Lee JH and Kyung KS. (2021). Monitoring and risk assessment of pesticide residues in pre-harvest fresh ginseng(Panax ginseng C. A. Meyer) in chungbuk province in 2019. Korean Journal of Environmental Agriculture. 40:118-126.
[https://doi.org/10.5338/KJEA.2021.40.2.14]

-
Ullah I, Yuan W, Khalil HB, Khan MR, Lak F, Uzair M and Wu H. (2024). Understanding Botrytis cinerea infection and gray mold management: A review paper on deciphering the rose’s thorn. Phytopathology Research. 6:42
[https://doi.org/10.1186/s42483-024-00262-9]

-
Velásquez AC, Castroverde CDM and He SY. (2018). Plant-pathogen warfare under changing climate conditions. Current biology. 28:R619-R634.
[https://doi.org/10.1016/j.cub.2018.03.054]

-
Woudenberg JHC, Seidl MF, Groenewald JZ, Vries Mde, Stielow JB, Thomma BPHJ and Crous PW. (2015). Alternaria section Alternaria: Species, formae speciales or pathotypes? Studies in Mycology. 82:1-21
[https://doi.org/10.1016/j.simyco.2015.07.001]

-
Zhou J, Zhang X, Qu Z, Zhang C, Wang F, Gao T and Liang J. (2024). Progress in research on prevention and control of crop fungal diseases in the context of climate change. Agriculture. 14:1108. https://www.mdpi.com/2077-0472/14/7/1108, (cited by 2026 Feb 01).
[https://doi.org/10.3390/agriculture14071108]